Clear Sky Science · fr
Hydrogel viscoélastique amorçant des macrophages CAR pour le traitement de la fibrose pulmonaire
Transformer les nettoyeurs du corps en équipes de réparation de précision
La fibrose pulmonaire est une maladie pulmonaire dévastatrice dans laquelle le tissu pulmonaire normalement élastique est progressivement remplacé par une cicatrice rigide. Les patients peinent à respirer, et les traitements actuels ne font généralement que ralentir le déclin. Cette étude explore une idée nouvelle : convertir les cellules de nettoyage du corps, les macrophages, en « agents d’entretien intelligents » et renforcer ensuite leur puissance avec un gel mou spécialement conçu. Ces deux approches aident les cellules à traquer les responsables de la formation de cicatrices et même à assouplir le tissu rigide des poumons endommagés.
Quand la réparation devient nuisible
Dans des poumons sains, les fibroblastes contribuent à maintenir la trame délicate de collagène qui soutient les alvéoles. Dans la fibrose pulmonaire, ces cellules deviennent hyperactives et déposent d’épaisses fibres de collagène qui obstruent les espaces aériens. Les médicaments actuels peuvent atténuer ces processus mais les inversent rarement. Les auteurs se concentrent sur un marqueur de surface appelé protéine d’activation des fibroblastes (FAP), abondant sur les fibroblastes hyperactifs mais rare dans les tissus normaux. Si les cellules immunitaires pouvaient être entraînées à reconnaître la FAP, elles pourraient éliminer sélectivement les fibroblastes « hors de contrôle » qui alimentent la cicatrisation tout en épargnant les cellules saines alentour.
Reprogrammer les macrophages pour cibler les bâtisseurs de cicatrices
Les macrophages sont des cellules immunitaires mobiles qui phagocytent normalement cellules mortes, microbes et débris cellulaires. L’équipe les a équipés d’un récepteur antigénique chimérique (CAR) reconnaissant la FAP, créant ainsi des macrophages CAR (CAR‑Ms). En culture, ces CAR‑Ms avalaient efficacement des fibroblastes riches en FAP et les tuaient, tout en ignorant largement les cellules à faible expression de FAP. Ils dégradaient également des gels riches en collagène plus vigoureusement que des macrophages non modifiés, suggérant un double bénéfice : éliminer les cellules productrices de cicatrices et attaquer directement la matrice cicatricielle. Ces effets se sont vérifiés tant sur des lignées cellulaires standard que sur des macrophages primaires de souris, plus proches de la situation in vivo. 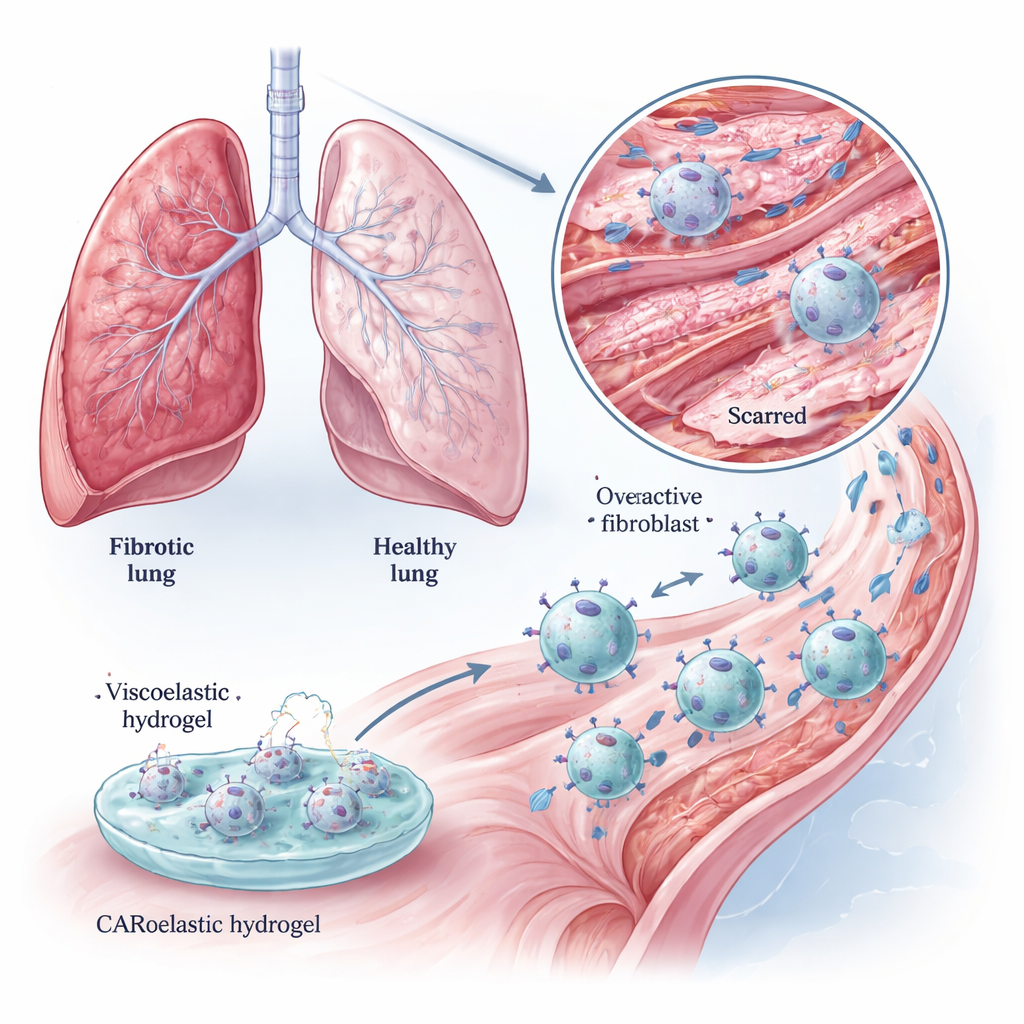
Amorcer les cellules immunitaires avec un gel mou et viscoélastique
L’ingénierie génétique des cellules est puissante mais complexe. Les chercheurs se sont donc demandés si un signal purement physique — un hydrogel viscoélastique et souple — pourrait également moduler le comportement des CAR‑Ms. Ils ont conçu un hydrogel gélatine‑alginate dont le « module de perte », une mesure de la façon dont il se relâche lentement sous contrainte, pouvait être finement réglé sans changer la rigidité globale. Lorsque les CAR‑Ms ont été brièvement cultivés sur des gels présentant la viscoélasticité adéquate, leur capacité à tuer les fibroblastes cibles a augmenté plus que sous stimulants chimiques usuels, et cet effet a persisté au moins deux jours. Ces « Gel‑CAR‑Ms » ont aussi activé des gènes liés à l’activation immunitaire et au remodelage tissulaire, tout en réprimant des gènes associés à la fibrose, suggérant que l’expérience du gel a imprimé chez les cellules une identité davantage anti‑cicatrice.
Comment une surface plus souple reprogramme le comportement cellulaire
Pour comprendre pourquoi le gel avait un effet, l’équipe a examiné l’état physique des récepteurs CAR à la surface cellulaire. Une sonde fluorescente a révélé que les CAR‑Ms amorcés sur hydrogel présentaient une tension membranaire plus faible — l’enveloppe externe de la cellule était plus relâchée. Dans ces conditions, les molécules CAR se dispersaient, passant de grappes serrées à des unités plus isolées et des paires. Des tests biochimiques ont montré que ces récepteurs dispersés favorisaient des configurations qui déclenchent plus facilement le signal intracellulaire, notamment via des voies comme ERK qui contrôlent l’activation et la capacité cytotoxique. Reproduire la baisse de tension avec une petite molécule a entraîné la même dispersion des récepteurs et une augmentation de la destruction de cellules cibles, soutenant l’idée que le relâchement mécanique de la membrane suffit à « pré‑armer » les cellules avant même leur rencontre avec les cibles. 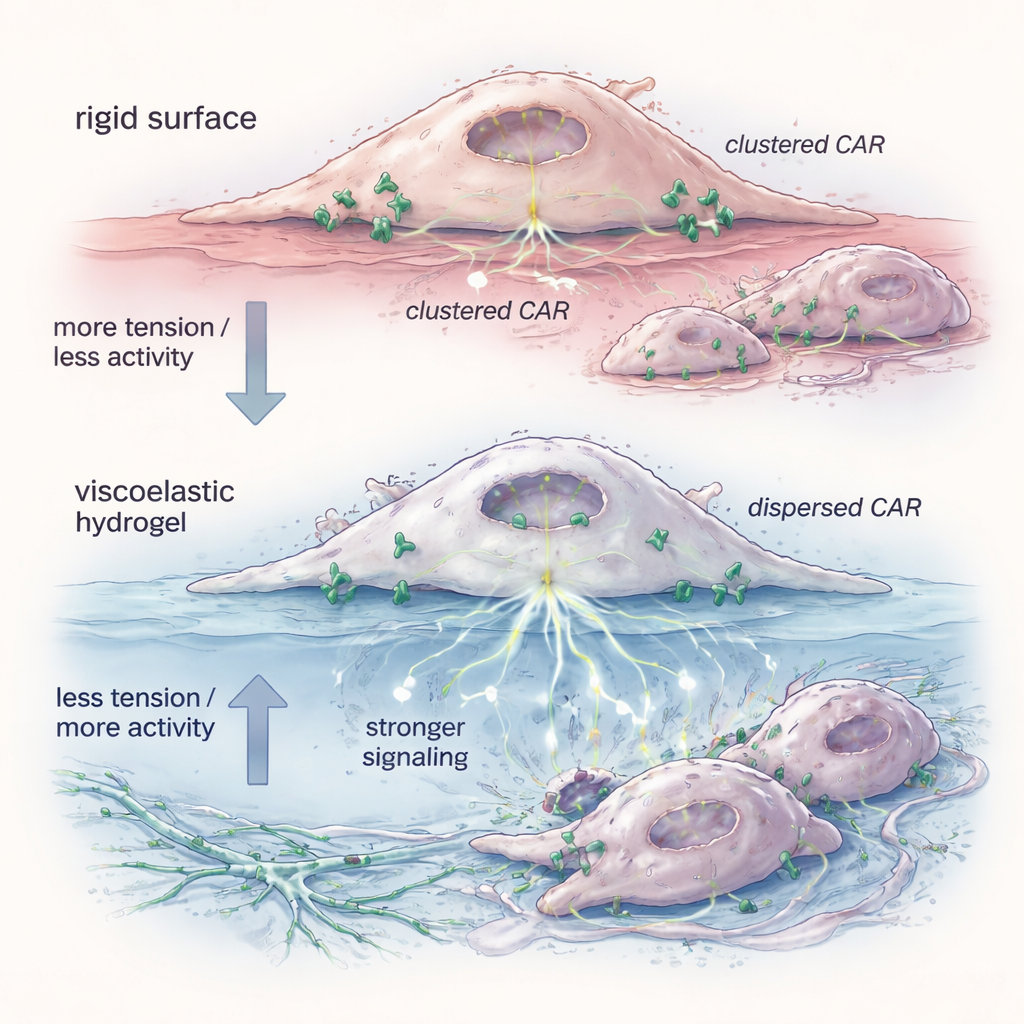
Réparer des poumons cicatriciels chez la souris
Le test ultime a été réalisé dans un modèle murin de fibrose pulmonaire induite par un médicament. Les animaux ont reçu soit des macrophages non modifiés, soit des CAR‑Ms standards, soit des Gel‑CAR‑Ms amorcés par hydrogel. Tous les groupes traités se sont améliorés par rapport aux témoins non traités, mais les Gel‑CAR‑Ms ont donné les meilleurs résultats : leurs poumons contenaient moins de collagène, des espaces aériens plus normaux et moins de fibroblastes FAP‑positifs. Les analyses génomiques du tissu pulmonaire ont montré que les Gel‑CAR‑Ms calmaient les signaux inflammatoires et réduisaient plus efficacement l’expression des gènes liés à la cicatrisation que les CAR‑Ms standards. Les cellules suivies ont persisté dans le poumon pendant au moins une semaine, et des contrôles de sécurité prolongés sur 12 semaines n’ont révélé ni lésions majeures d’organes, ni anomalies sanguines, ni signes d’auto‑immunité.
Une nouvelle orientation pour les thérapies cellulaires anti‑fibrose
Pour un public non spécialiste, le message clé est que la combinaison d’un ciblage cellulaire et de matériaux intelligents peut transformer des cellules immunitaires innées en outils de lutte contre la cicatrisation très efficaces, sans complexifier excessivement leur génétique. En reposant brièvement des macrophages ingénierés sur un gel souple et finement calibré, les chercheurs ont « pré‑réglé » mécaniquement leurs récepteurs de surface dans un état plus réactif. Chez des souris fibrosées, cela s’est traduit par une meilleure élimination des fibroblastes nuisibles, la dégradation de l’excès de collagène et une restauration partielle de la structure pulmonaire normale — sans problèmes de sécurité apparents. Bien que de nombreuses étapes restent à franchir avant des essais humains, cette stratégie suggère que l’affinement de l’environnement physique des cellules thérapeutiques pourrait un jour rendre les traitements des maladies pulmonaires fibreuses plus puissants et plus précis.
Citation: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Mots-clés: fibrose pulmonaire, thérapie par macrophages CAR, hydrogel viscoélastique, protéine d’activation des fibroblastes, Mécanobiologie cellulaire