Clear Sky Science · fr
Base moléculaire de l'inhibition de la méthylation de novo de l'ADN par TCL1A
Comment les cellules décident de ce qu’elles doivent garder en mémoire
Toutes les cellules de votre corps portent essentiellement le même ADN, et pourtant les cellules nerveuses, sanguines et cutanées se comportent très différemment. Une façon pour les cellules de « se souvenir » de leur identité consiste à ajouter des étiquettes chimiques à l’ADN, un processus appelé méthylation de l’ADN. Cette étude révèle, au niveau atomique, comment une petite protéine nommée TCL1A peut éteindre les enzymes qui inscrivent ces marques méthyl. Comme la méthylation de l’ADN et TCL1A sont tous deux liés au cancer et à des troubles de la reproduction, comprendre ce bras de fer moléculaire pourrait finir par inspirer de nouvelles thérapies.
La machinerie cellulaire d’étiquetage de l’ADN
La méthylation de l’ADN fonctionne comme un trait de crayon dans les marges du génome, aidant à silencier certains gènes et à stabiliser le génome au cours du développement cellulaire. Deux enzymes, DNMT3A et DNMT3B, sont les principaux « scribeurs » qui placent de nouvelles marques méthyl pendant le développement précoce et lorsque les cellules souches se spécialisent. Si ces enzymes sont mutées ou mal régulées, le motif des marques d’ADN peut être perturbé, contribuant à des syndromes du développement et à des cancers du sang. TCL1A est une protéine surtout connue pour son rôle dans les cancers des cellules immunitaires, où elle est souvent surproduite. Des travaux antérieurs laissaient entendre que TCL1A peut se lier à DNMT3A et DNMT3B et atténuer leur activité, mais personne ne savait exactement comment cette inhibition était obtenue.
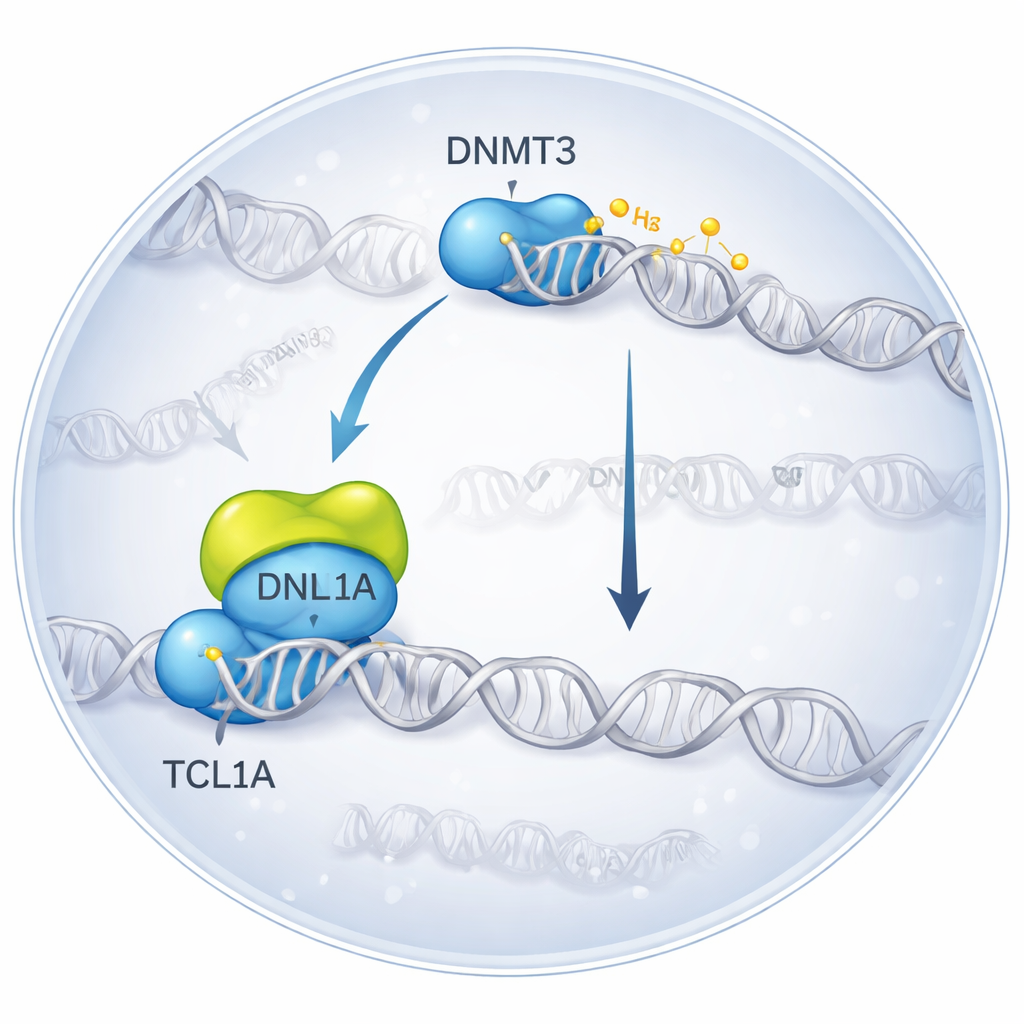
Figurer une rencontre moléculaire en 3D
Les chercheurs ont utilisé la cryo‑microscopie électronique, une technique qui image des molécules rapidement congelées, pour visualiser le complexe formé lorsque DNMT3A se lie à TCL1A. Ils ont constaté que deux molécules de DNMT3A s’apparient, et de chaque côté un dimère de TCL1A se fixe sur la partie catalytique de DNMT3A — la même région qui interagit normalement avec des protéines partenaires et l’ADN. Cette surface de liaison chevauche l’endroit où un autre partenaire, DNMT3L, se fixe habituellement pour stimuler l’activité de DNMT3A. Dans des tests biochimiques, l’ajout de TCL1A a fortement réduit la capacité de DNMT3A et DNMT3B à méthyler l’ADN, même en présence de DNMT3L, confirmant que le complexe structurel correspond à un état fortement inhibé.
Un changement de forme qui bloque l’enzyme
En regardant de plus près, l’équipe a observé que la liaison de TCL1A ne se contente pas de couvrir le site actif comme un couvercle. Au contraire, elle déclenche un changement subtil mais étendu de la conformation de DNMT3A. Deux régions flexibles de l’enzyme, connues sous le nom de boucle de reconnaissance de la cible et boucle catalytique, s’écartent des positions qu’elles occupent lorsque DNMT3A est liée à l’ADN. Dans la forme active, ces boucles s’appuient contre l’ADN et forment une poche pour une petite molécule carburant appelée SAM, qui fournit le groupe méthyle. Avec TCL1A attaché, la boucle catalytique se replie à la place dans la poche de SAM et la bouche, tout en rendant également plus difficile l’accès de l’ADN à l’enzyme. Des mesures d’affinité ont confirmé que DNMT3A associé à TCL1A ne peut plus se fixer détectablement ni à l’ADN ni au SAM.
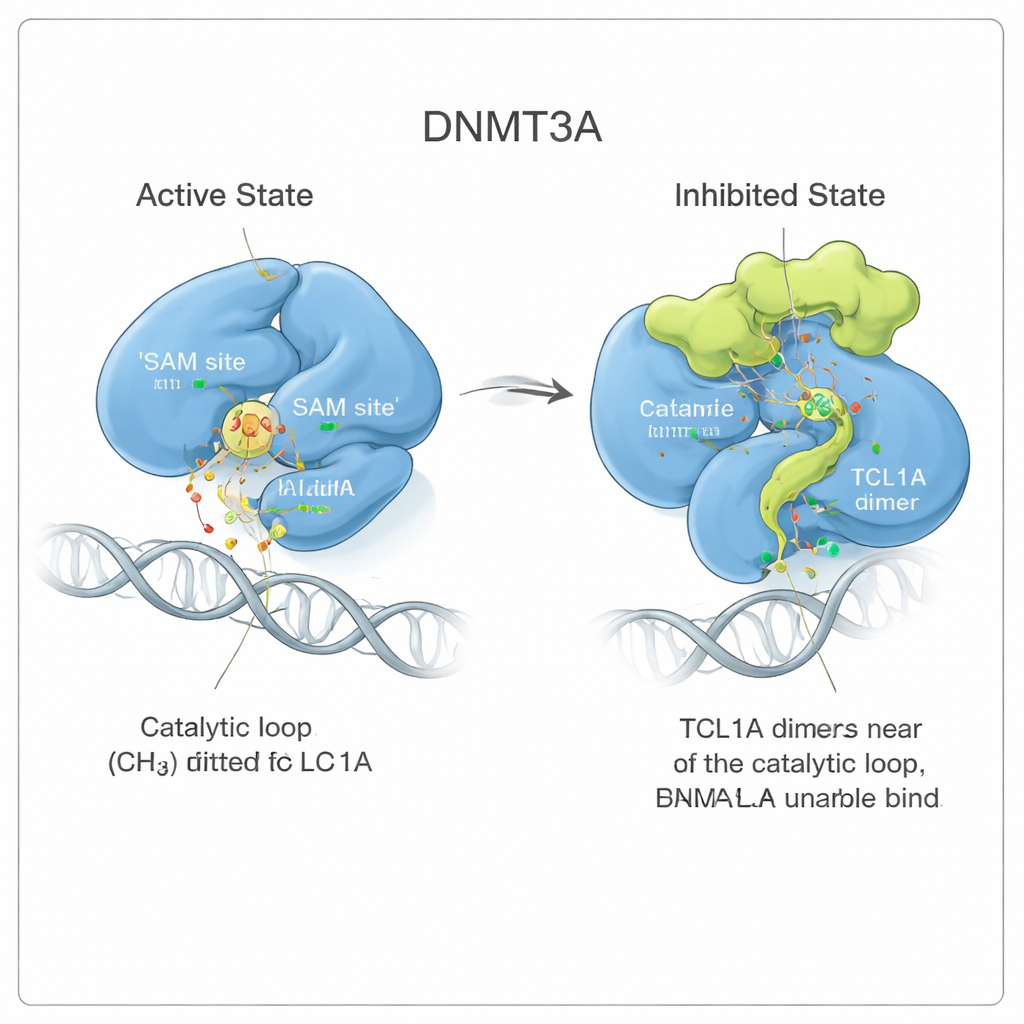
Observer un blocage dynamique en mouvement
Pour comprendre la stabilité de cette conformation inhibée, les auteurs ont réalisé de longues simulations de dynamique moléculaire, essentiellement des films basés sur la physique des molécules en solution. Lorsque DNMT3A était lié à son activateur DNMT3L, la boucle catalytique restait bien en place dans sa position active. En présence de TCL1A, cette boucle devenait beaucoup plus mobile, battant de l’aile mais occupant à plusieurs reprises la poche de SAM comme des algues tourbillonnant tout en obstruant toujours un drain. Ce mouvement constant a réduit l’espace disponible pour le SAM de plus d’un facteur dix, soutenant un modèle dans lequel TCL1A exploite la flexibilité naturelle de DNMT3A pour imposer une forme d’inhibition dynamique plutôt que rigide.
Conséquences pour les cellules en développement et la maladie
Les chercheurs ont ensuite cherché à savoir ce que ce blocage moléculaire signifie pour de vraies cellules. Ils ont modifié des cellules souches embryonnaires de souris pour produire la TCL1A humaine pendant une phase où les cellules accroissent normalement la méthylation de l’ADN au début de leur différenciation. Le profilage de la méthylation à l’échelle du génome a montré que les cellules surexprimant TCL1A n’acquéraient pas le niveau élevé habituel de méthylation de l’ADN, ressemblant de près aux cellules dont les gènes Dnmt3a et Dnmt3b avaient été tous deux inactivés. Une version mutante de TCL1A qui se lie mal aux enzymes DNMT3 avait peu d’effet, soulignant que l’interaction physique est essentielle. Ces résultats relient le mécanisme structural à des changements épigénétiques étendus à travers le génome.
Ce que cela implique pour la santé
Ensemble, ces travaux révèlent comment TCL1A peut agir comme un frein puissant sur les enzymes qui déposent de nouvelles marques de méthylation de l’ADN. En se fixant à une interface critique, TCL1A repositionne des boucles flexibles de DNMT3A et DNMT3B de sorte qu’elles ne peuvent plus lier leur matrice d’ADN ni leur carburant chimique, entraînant une perte globale des marques de méthylation dans les cellules. Lors du développement normal, ce type de contrôle fin peut aider à équilibrer le moment et l’endroit où la méthylation est ajoutée. Lorsque TCL1A est mal placé ou surproduit, comme dans certains cancers hématologiques et rares troubles de la reproduction, le même mécanisme peut perturber le programme épigénétique de la cellule. Comprendre cette interaction à résolution atomique ouvre la voie à la conception de molécules qui imiteraient ou neutraliseraient les effets de TCL1A, permettant potentiellement de restaurer des profils de méthylation de l’ADN sains.
Citation: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Mots-clés: Méthylation de l’ADN, DNMT3A, TCL1A, épigénétique, cancer