Clear Sky Science · fr
Méthodes d'apport d'échantillons pour la cristallographie des protéines par rayons X avec un accent particulier sur la consommation d'échantillon
Observer les molécules en action
La cristallographie aux rayons X permet aux scientifiques de voir l'arrangement des atomes dans les protéines, ces petites machines qui animent le vivant. Une approche plus récente, appelée cristallographie sérielle, va plus loin : elle peut capturer des « films moléculaires » de protéines en action, par exemple des enzymes traitant un médicament ou des protéines photosynthétiques scindant l'eau. Il y a toutefois un hic. De nombreuses protéines importantes sont difficiles à produire et à cristalliser, et les expériences actuelles peuvent consommer des milligrammes à des grammes de matière précieuse. Cet article de synthèse pose une question apparemment simple : comment amener des cristaux dans des faisceaux de rayons X puissants en gaspill ant le moins d'échantillon possible ?
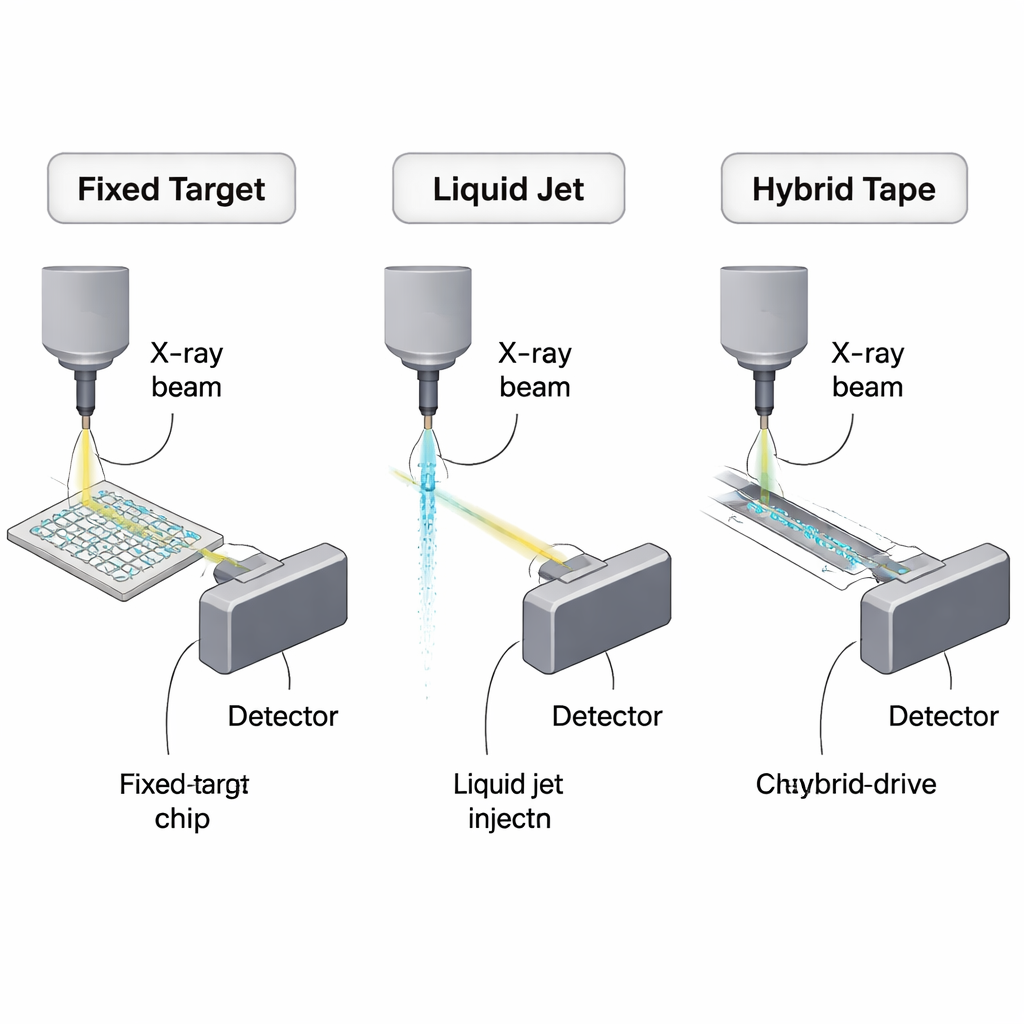
Pourquoi la cristallographie sérielle exige de meilleurs systèmes d'apport
La cristallographie traditionnelle reposait sur un seul gros cristal tournant dans un faisceau de rayons X. La cristallographie sérielle inverse la logique : au lieu d'un gros cristal, ce sont des milliers de microcristaux, chacun utilisé une seule fois, qui sont projetés ou balayés par des impulsions X ultrabrillantes provenant de synchrotrons ou de lasers à électrons libres X (XFEL). Cela permet la collecte de données à température ambiante et des « instantanés » rapides de réactions chimiques, mais cela implique aussi de renouveler constamment les cristaux à des débits correspondant aux trains d'impulsions X qui peuvent atteindre des millions d'impulsions par seconde. Une grande partie de la suspension de cristaux ne rencontre jamais réellement le faisceau et est éliminée, de sorte que réduire la consommation d'échantillon est devenu un défi technique et économique central pour le domaine.
Supports fixes : de minuscules puces qui exploitent chaque goutte
Une stratégie majeure consiste à immobiliser les microcristaux sur de petits supports solides appelés supports fixes. Plutôt que de pulvériser les cristaux devant le faisceau, les chercheurs les disposent en matrices sur des puces en silicium ou en polymère et déplacent la puce de manière à amener chaque cristal une fois dans la focalisation X. Dans une expérience de pensée optimiste, environ 10 000 microcristaux d'une protéine modèle pourraient, en principe, fournir un jeu de données complet en n'utilisant qu'environ 450 nanogrammes de protéine. Les dispositifs réels ne sont pas encore aussi économes, mais ils réduisent déjà les besoins à des dizaines de microgrammes voire quelques dixièmes de milligramme — des ordres de grandeur meilleurs que les premières expériences sérielles. La revue compare des maillages de silicium, des films polymères ultrafins et des puces plastiques multicouches, pesant leurs points forts (faible diffusion de fond, croissance de cristaux sur puce, compatibilité avec des études à température ambiante) contre des problèmes pratiques comme la déshydratation, la diffusion parasite due au matériau de la puce et le « volume mort » supplémentaire introduit par le pipetage manuel.
Jets liquides et flux visqueux : rapides mais gourmands
Une autre famille de méthodes maintient les cristaux en suspension dans un liquide et les fait passer continuellement à travers le faisceau. Les buses virtuelles gasodynamiques créent des jets d'une finesse extrême capables de suivre les trains d'impulsions rapides des XFEL, en faisant un outil de choix pour les études résolues dans le temps et les expériences « mix-and-inject » où les réactions sont déclenchées par un mélange rapide juste avant l'exposition. Cependant, comme les jets fonctionnent en continu, la majeure partie du flux ne rencontre jamais d'impulsion X. Même avec un réglage soigné, les expériences pratiques consomment bien plus de protéine que le minimum théorique — typiquement des dizaines à des centaines de microlitres de boue de cristaux concentrée. Pour atténuer l'effet, les chercheurs ont développé des conceptions plus efficaces, comme des buses à double flux qui gaînent le jet de cristaux avec un liquide sacrificiel, des injecteurs « MESH » par électrofilage fonctionnant à des débits plus faibles, et des extrudeuses haute viscosité qui poussent des cristaux incorporés dans des gels ou des phases cubiques lipidiques à des débits de microlitres par minute voire plus lents. Ces méthodes visqueuses sont particulièrement utiles pour les protéines membranaires fragiles et pour les études à température ambiante aux synchrotrons, mais leurs flux plus épais augmentent la diffusion de fond et sont moins adaptées aux sources X les plus rapides.
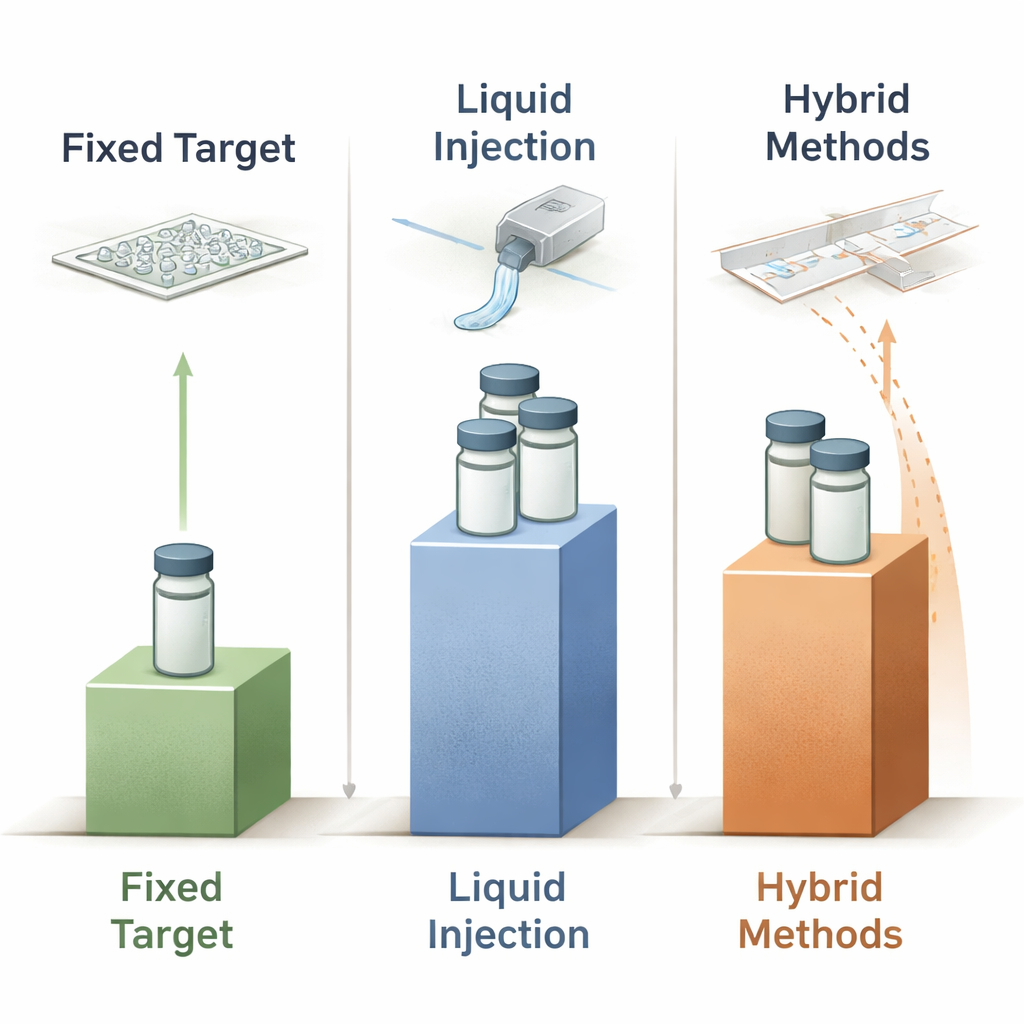
Gouttelettes, rubans et hybrides : caler chaque impulsion sur mesure
Une troisième classe, de plus en plus créative, d'approches « hybrides » combine des supports solides avec un apport liquide ou de gouttelettes contrôlé. Les systèmes à bande transporteuse, par exemple, déposent des gouttelettes ou de fines bandes liquides sur un film polymère mobile qui passe dans le faisceau ; en synchronisant le mouvement, il est possible d'explorer des étapes réactionnelles ou une exposition gazeuse à des délais définis. Les systèmes drop‑on‑demand vont plus loin, utilisant des dispositifs acoustiques ou piézoélectriques pour éjecter des gouttes de nanolitres voire de picolitres uniquement lorsqu'une impulsion X est attendue, réduisant drastiquement le gaspillage. Certains dispositifs mélangent une goutte de ligand dans une goutte contenant préalablement des cristaux déposée sur la bande juste avant qu'elle n'atteigne le faisceau, permettant l'enzymologie résolue dans le temps avec des réactifs soigneusement rationnés. D'autres hybrides, comme la méthode LAMA sur puce, ajoutent de minuscules gouttes de substrat directement sur des cristaux pré‑montés sur des puces à support fixe. Dans ces conceptions, la consommation de protéine rapportée couvre une large gamme — depuis des niveaux proches du milligramme jusqu'à quelques milligrammes pour des séries temporelles complètes — illustrant à la fois le potentiel et les défis d'ingénierie actuels pour synchroniser gouttelettes, cristaux et impulsions X.
Sommes‑nous proches du minimum théorique ?
En comparant des dizaines d'expériences publiées sur supports fixes, injecteurs liquides et systèmes hybrides, les auteurs montrent qu'aucune méthode existante ne s'approche du seuil idéal de 450 nanogrammes ; même les meilleurs dispositifs dépassent encore d'environ deux ordres de grandeur. Pourtant, des tendances claires se dégagent. Les supports fixes utilisent typiquement le moins de protéine et sont attractifs chaque fois que le mélange résolu dans le temps n'est pas essentiel ou peut être réalisé sur puce. Les jets liquides dominent toujours les études XFEL les plus exigeantes en résolution temporelle mais restent gourmands en échantillon, surtout lorsqu'un grand nombre de points temporels est requis. Les schémas hybrides goutte‑et‑bande offrent certains des plus importants gains relatifs, en particulier lorsque le timing des gouttelettes est étroitement synchronisé avec la source X. En regardant vers l'avenir, l'article soutient que des progrès supplémentaires viendront d'un meilleur contrôle microfluidique, de l'automatisation pour éliminer les étapes de manipulation gaspilleuses, et de l'utilisation de sources X compactes et de l'optimisation pilotée par les données pour co‑concevoir expériences et systèmes d'apport qui rapprocheront encore la consommation de protéines de la limite théorique.
Citation: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Mots-clés: cristallographie sérielle, cristallographie des protéines par rayons X, apport d'échantillon, laser à électrons libres X, microfluidique