Clear Sky Science · fr
La réduction de RAD23A prolonge la durée de vie et atténue la pathologie dans un modèle murin de protéinopathie à TDP-43
Pourquoi cette recherche importe pour les familles et les patients
De nombreuses formes de démence et de maladies des motoneurones, notamment la sclérose latérale amyotrophique (SLA) et la démence frontotemporale (DFT), impliquent des protéines dans les cellules cérébrales qui se replient mal, s’agglutinent et empoisonnent lentement les neurones. L’un des acteurs clés est une protéine appelée TDP-43, qui aide normalement à gérer l’ARN mais devient toxique lorsqu’elle s’agrège. Cette étude pose une question porteuse d’espoir : peut-on rendre les cellules cérébrales plus résistantes en diminuant une autre protéine, RAD23A, qui participe au traitement des protéines endommagées ? Les auteurs montrent chez la souris que l’abaissement de RAD23A peut prolonger la vie, améliorer la motricité et réduire les lésions cérébrales dans un modèle de maladie pilotée par TDP-43, suggérant une nouvelle stratégie thérapeutique.
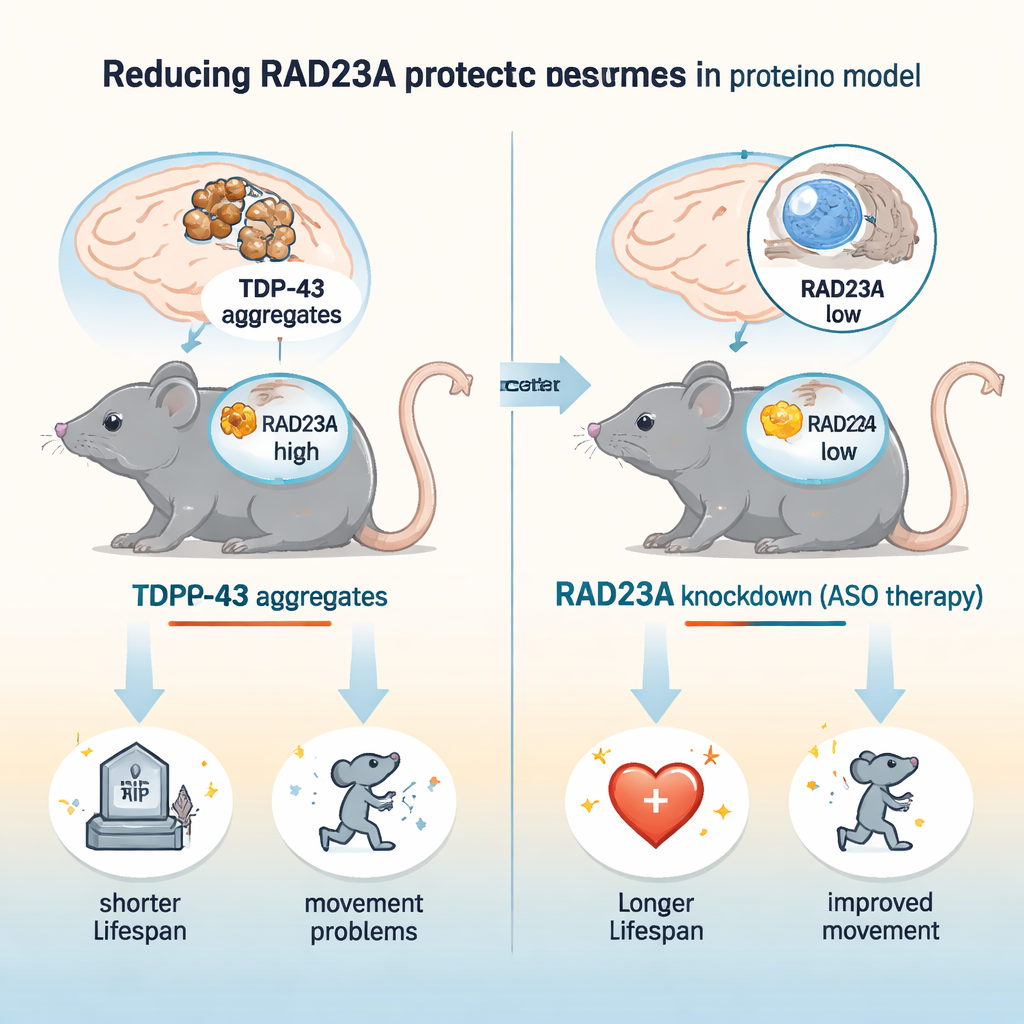
Un embouteillage de protéines dans les neurones malades
Les maladies neurodégénératives se caractérisent souvent par des amas de protéines mal repliées que le système d’élimination cellulaire ne parvient pas à dégager. Dans la SLA et la DFT, TDP-43 quitte le noyau, forme des agrégats collants et devient fortement marquée par l’ubiquitine, un signal qui oriente normalement les protéines vers le protéasome, le principal broyeur de la cellule. RAD23A est l’un des « navettes » capables de porter des cargos marqués par l’ubiquitine vers le protéasome. Pourtant, des travaux précédents chez des vers et des neurones en culture ont suggéré que la perte de protéines de type RAD23 pouvait en fait protéger contre les dommages induits par TDP-43, un paradoxe que cette étude a cherché à explorer dans un cerveau mammifère vivant.
Réduire RAD23A dans un modèle murin de TDP-43
Les chercheurs ont utilisé un modèle murin bien établi, appelé TAR4/4, qui surexprime la TDP-43 humaine dans les neurones et développe des troubles de la motricité, une courbure de la colonne, des tremblements et une mort précoce, reprenant des caractéristiques clés de la SLA/DFT. Ils ont diminué RAD23A de deux manières : en injectant à des nouveau-nés des oligonucléotides antisens (ASO) réduisant l’ARN Rad23a, et en croisant des souris porteuses d’un knockout génétique de Rad23a. Un seul traitement par ASO a réduit les niveaux de RAD23A dans le cerveau et la moelle épinière d’environ trois quarts. Chez ces souris TDP-43, l’inhibition de RAD23A a prolongé la durée de vie d’environ 50 % et retardé l’apparition et la sévérité des troubles de la marche, des tremblements, de la courbure spinale et du réflexe de serrage des postérieurs. Fait intéressant, une perte génétique complète de RAD23A n’apportait pas de bénéfice supplémentaire, ce qui suggère qu’une réduction partielle est optimale et qu’une absence totale à long terme peut déclencher des adaptations compensatoires.
Moins d’inflammation, meilleure gestion des protéines et un génome plus calme
L’examen microscopique du cortex moteur a montré que les souris TDP-43 perdaient des neurones et présentaient une forte activation des astrocytes et des microglies, les cellules de soutien et immunitaires du cerveau. La réduction de RAD23A a préservé le nombre de neurones et diminué les marqueurs d’inflammation et de mort cellulaire. Des analyses biochimiques ont révélé que la surexpression de TDP-43 surchargeait les cellules en protéines insolubles et marquées par l’ubiquitine et entraînait des sous-unités du protéasome dans ces agrégats, affaiblissant la capacité cellulaire à éliminer les protéines endommagées. La diminution de RAD23A a réduit la charge totale de protéines ubiquitinées, maintenu davantage de protéasomes dans le pool soluble et fonctionnel, et restauré plusieurs types d’activités du protéasome vers la normale. Parallèlement, l’inhibition de RAD23A a réduit à la fois les formes totales et agrégées de TDP-43, y compris un fragment particulièrement toxique de 25 kilodaltons, et a ramené TDP-43 du cytoplasme vers le noyau. Le séquençage global de l’ARN a montré que des milliers de changements d’expression génique déclenchés par TDP-43 étaient partiellement inversés lorsque RAD23A était réduit, en particulier les gènes impliqués dans la fonction neuronale, la production d’énergie mitochondriale et les voies d’élimination des agrégats comme l’aggréphagie.
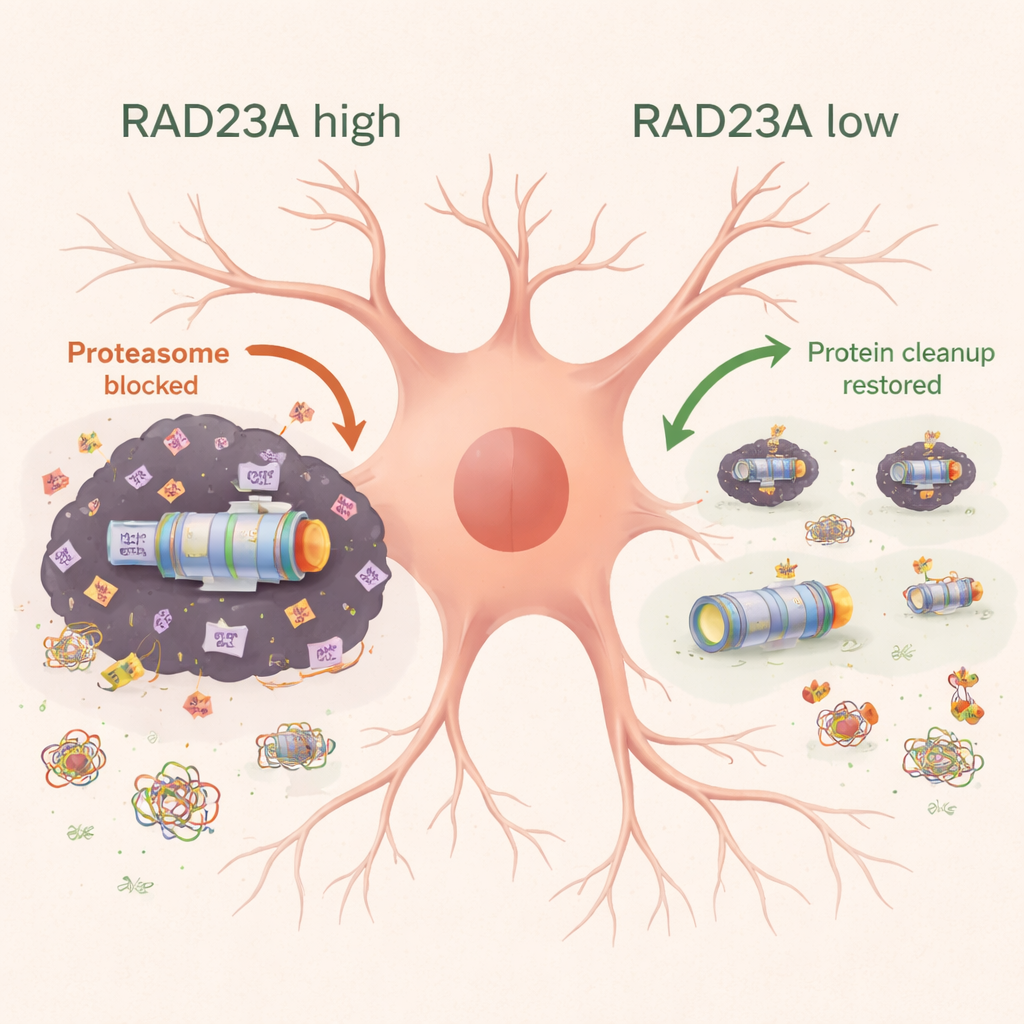
Remodeler le protéome « insoluble » caché
Pour examiner de plus près les agrégats récalcitrants qui résistent aux détergents ordinaires, l’équipe a utilisé la spectrométrie de masse aux isotopes lourds pour inventorier les protéines piégées dans la fraction insoluble du cortex de souris. L’expression de la TDP-43 humaine attirait des composants du protéasome, des protéines du cytosquelette et du transport, ainsi que d’autres machineries cellulaires. Lorsque RAD23A était réduit, la composition globale de ce protéome insoluble a changé : moins de protéines liées au protéasome et au transport étaient séquestrées, tandis que certaines protéines ribosomales et liées au stress augmentaient dans les agrégats. Il est notable que ce remodelage ne reflétait pas simplement des changements au niveau de l’ARN, ce qui suggère que RAD23A influence principalement la façon dont les protéines existantes sont réparties entre états solubles et agrégés, plutôt que la quantité de chaque protéine synthétisée.
Ce que cela pourrait signifier pour les thérapies futures
Ensemble, ces résultats présentent RAD23A comme un modulateur puissant du contrôle de la qualité des protéines chez les neurones en situation de stress. En abaissant partiellement RAD23A dans un modèle murin piloté par TDP-43, les auteurs ont réduit les amas protéiques toxiques, restauré l’activité des machineries d’élimination des protéines, atténué les changements d’expression génique nocifs, limité l’inflammation cérébrale et prolongé la vie et la fonction motrice. Parce que l’accumulation anormale de TDP-43 est fréquente dans les formes héréditaires et sporadiques de la SLA, de la DFT et de troubles apparentés, cibler RAD23A avec des médicaments antisens compatibles avec l’homme pourrait offrir un moyen de protéger les neurones sans bloquer directement TDP-43, une protéine essentielle. Bien qu’il reste beaucoup à tester dans d’autres modèles et chez l’homme, ce travail identifie RAD23A comme une nouvelle cible prometteuse sur une voie commune de la neurodégénérescence.
Citation: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Mots-clés: TDP-43, SLA, agrégation protéique, protéasome, thérapie antisens