Clear Sky Science · fr
Le centre nerveux de l’ingénierie des organes
Pourquoi connecter les organes importe
Les scientifiques se rapprochent de la fabrication d’organes de remplacement en laboratoire pour pallier la grave pénurie de cœurs, de foies, de reins et d’autres donneurs. Mais la plupart des organes artificiels se concentrent sur les vaisseaux sanguins et ignorent un autre ingrédient crucial : les nerfs. Cet article de synthèse explique pourquoi le câblage électrique du corps est essentiel à la croissance des organes, à leur fonctionnement quotidien et à la réparation, et comment les chercheurs apprennent à intégrer des réseaux nerveux dans les organes cultivés en laboratoire.
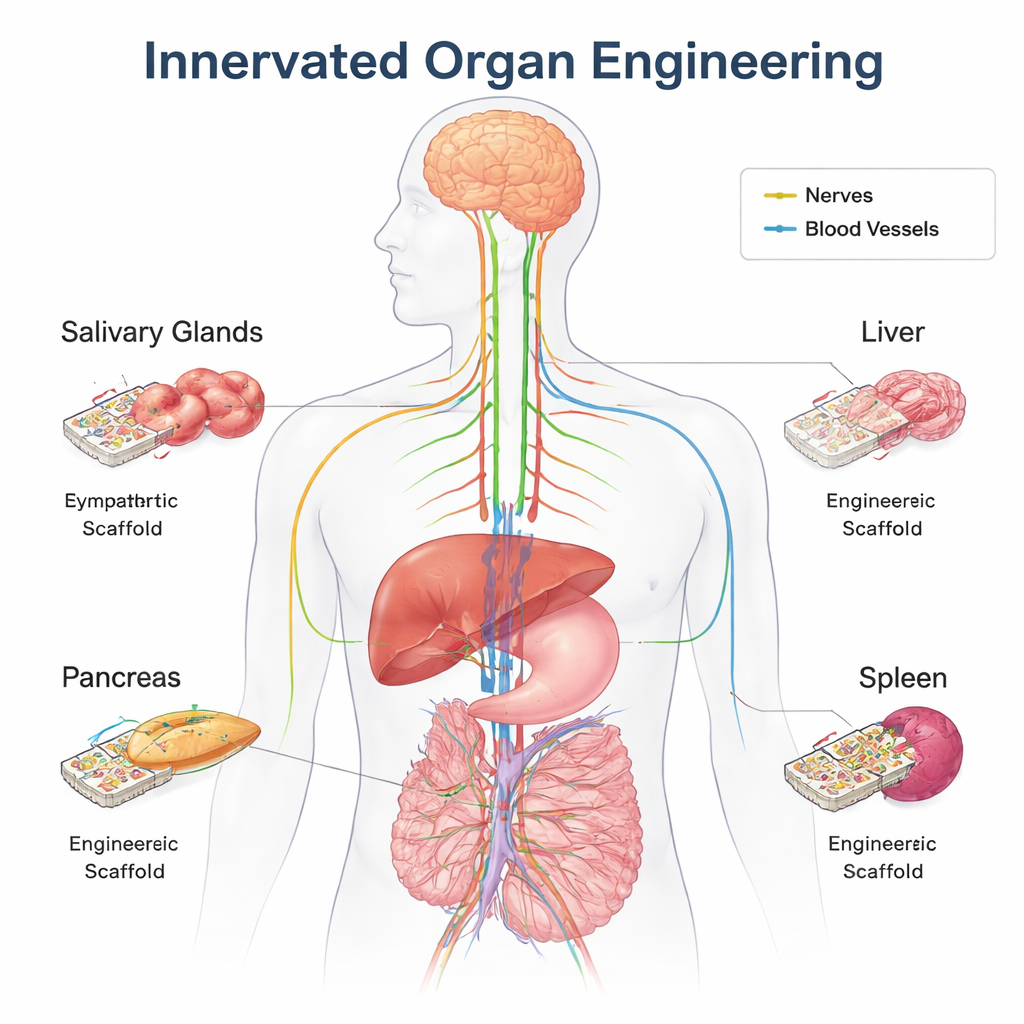
Le réseau de contrôle caché du corps
Chaque organe majeur est parcouru de fibres nerveuses qui dialoguent en permanence avec le cerveau et la moelle épinière. Par le biais du système nerveux autonome — les branches « combat-fuite » et « repos-digestion » — ces nerfs régulent discrètement la glycémie, la digestion, les réponses immunitaires, le flux sanguin, et plus encore. Ils le font en envoyant des messages chimiques tels que l’acétylcholine et la noradrénaline, et en détectant des changements comme l’étirement, la température ou le niveau de nutriments. Au-delà du contrôle quotidien, les nerfs contribuent aussi à façonner les organes avant la naissance, à guider la cicatrisation et à soutenir les cellules souches qui réparent les tissus. Dans de nombreux cas, les nerfs poussent le long des vaisseaux sanguins en suivant des indices de guidage similaires, de sorte que le câblage et la plomberie se développent ensemble.
Pourquoi les greffes supportent l’absence de nerfs — mais pas les organes de laboratoire
Les transplantations d’organes traditionnelles sont généralement implantées sans leurs nerfs d’origine. Un foie ou un rein transplanté peut fonctionner car il reçoit des hormones et d’autres signaux par la circulation sanguine, et au fil du temps de nouvelles fibres nerveuses peuvent repousser depuis le receveur. Cette « période de grâce » n’existe pas pour les organes conçus de toutes pièces. Ces constructions manquent typiquement de la pleine gamme de types cellulaires matures et de la matrice de soutien complexe présente dans un organe naturel. Des connexions nerveuses précises sont particulièrement importantes pour coordonner les nombreuses cellules spécialisées à l’intérieur d’organes comme le pancréas, le foie, les glandes salivaires et la rate. Les auteurs soutiennent que, pour l’ingénierie d’organes ascendante — où les organes sont assemblés à partir de petits éléments — l’innervation préprogrammée doit être considérée comme une exigence de conception plutôt que comme un ajout optionnel.
Comment les nerfs façonnent quatre organes clés
La revue examine en détail comment les nerfs influencent quatre organes exemples. Dans le pancréas, les fibres sympathiques et parasympathiques contribuent à sculpter l’architecture des îlots producteurs d’insuline pendant le développement et, plus tard, ajustent la libération d’insuline et de glucagon lorsque la glycémie augmente ou diminue. Dans les glandes salivaires, une entrée parasympathique précoce maintient en vie les cellules souches épithéliales et guide le ramification des canaux qui sécrètent finalement la salive ; la section de ces nerfs au mauvais moment perturbe la formation normale de la glande. Les nerfs du foie détectent les niveaux de sel, d’eau, de sucre et de lipides dans le sang et ajustent le métabolisme, la pression artérielle et la régénération après une lésion. Dans la rate, les fibres sympathiques communiquent directement avec les cellules immunitaires, atténuant ou amplifiant l’inflammation et aidant l’organisme à répondre aux infections et au stress. Dans ces organes, la perte ou le mauvais câblage des nerfs est associé au diabète, à des troubles digestifs, aux maladies du foie et à une immunité altérée.
Construire des organes avec un câblage intégré
Pour apporter l’innervation aux organes bioingénierés, les scientifiques combinent l’impression 3D avancée, des conceptions d’échafaudages ingénieuses et des cellules nerveuses dérivées de cellules souches. L’extrusion et l’impression biotechnologique par photopolymérisation peuvent placer différents types cellulaires et matériaux selon des motifs précis, tandis que des hydrogels et des polymères spécialisés sont ajustés pour supporter de longues fibres nerveuses ramifiées. Des études ont déjà créé des réseaux neuronaux imprimés, des unités nerf-muscle et de mini-tissus cérébraux qui présentent une activité électrique réaliste. Les auteurs proposent des plans pratiques pour des versions innervées du pancréas, de la glande salivaire, du foie et de la rate : isoler ou dériver les cellules organiques clés, les mélanger avec des neurones autonomes (sympathiques et parasympathiques) dans des bio-encres compatibles, les imprimer en structures en forme d’organe, et les faire mûrir dans des bioréacteurs pour que les nerfs puissent s’étendre dans le tissu avant l’implantation.
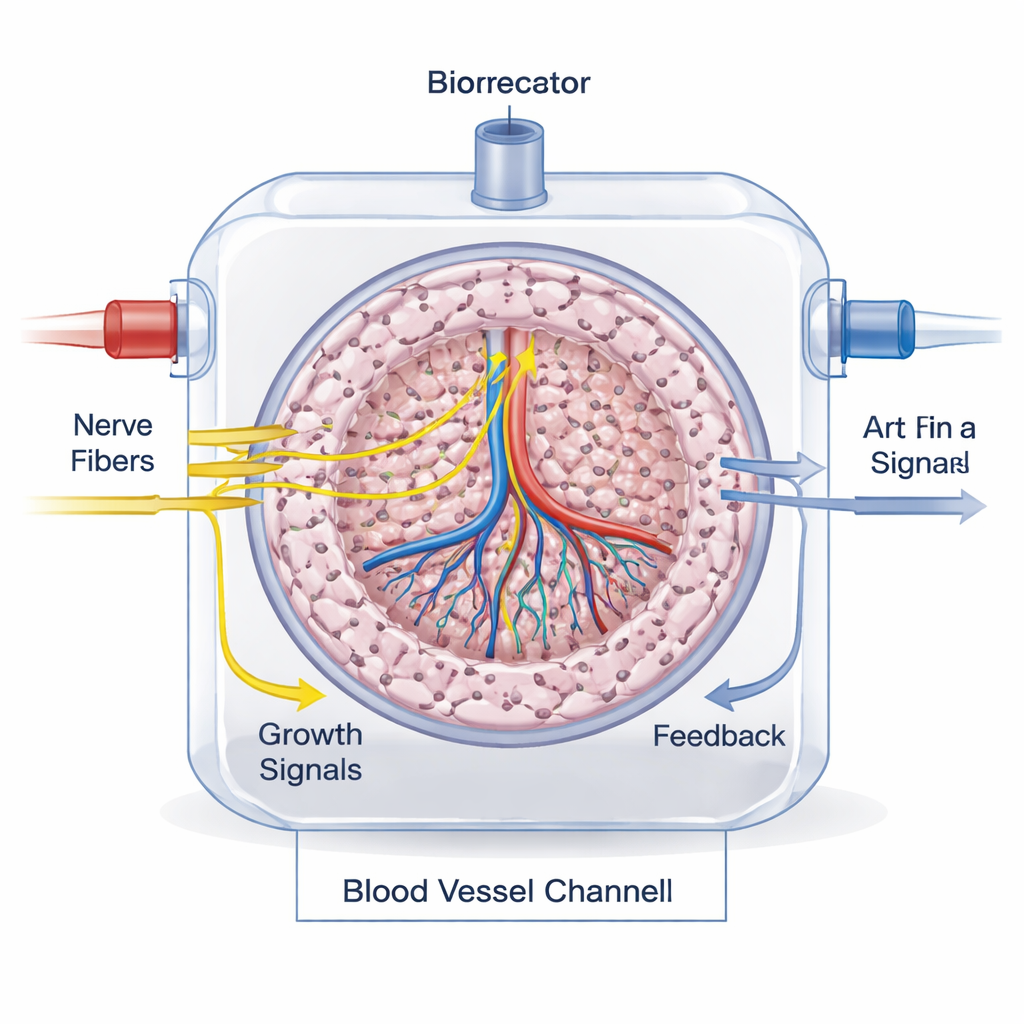
Mesurer si le câblage fonctionne
Vérifier que les nerfs sont véritablement intégrés et fonctionnels est un défi majeur. En laboratoire, les chercheurs marquent les protéines spécifiques des nerfs, mesurent les neurotransmetteurs par des tests biochimiques et utilisent l’imagerie en direct pour observer la croissance des axones et la réponse des cellules. Des plateformes microfluidiques « organe-sur-puce » aident à modéliser un flux sanguin réaliste et la signalisation nerf–organe. Chez l’animal et, éventuellement, chez le patient, l’innervation peut être suivie en combinant des colorations tissulaires, des traceurs nerveux et des méthodes d’imagerie modernes telles que l’IRM, le scanner et la TEP avec des composés radioactifs spécialisés qui mettent en évidence les fibres sympathiques ou parasympathiques.
De l’idée à la thérapie
L’article conclut que les nerfs ne sont pas une option de luxe mais une exigence centrale pour des organes artificiels véritablement fonctionnels. Pour passer des démonstrations prometteuses en laboratoire à de véritables thérapies, il faudra améliorer l’impression 3D à grande échelle de réseaux nerveux complexes, affiner les sources cellulaires (en particulier les neurones autonomes dérivés de cellules souches humaines) et développer des outils d’imagerie clinique pratiques pour surveiller l’intégration neuronale après implantation. Si ces obstacles sont franchis, la génération suivante d’organes conçus pourrait non seulement remplacer les tissus perdus mais aussi se connecter de façon transparente aux circuits de contrôle du corps, offrant des traitements plus fiables et plus fidèles à la physiologie pour le diabète, l’insuffisance hépatique, les troubles de la sécheresse buccale, les déficiences immunitaires et au-delà.
Citation: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Mots-clés: ingénierie des organes, innervation, biofabrication, impression 3D de tissus, système nerveux autonome