Clear Sky Science · fr
Histologie optique à super‑résolution des échantillons fixés au formol et inclus en paraffine : défis et opportunités
Voir davantage dans les échantillons tissulaires conservés
Des hôpitaux du monde entier conservent de fines lamelles d’organes de patients dans des blocs de cire afin que des maladies comme le cancer ou les lésions rénales puissent être étudiées pendant des années. Cet article de revue explique comment de nouveaux types de microscopes optiques transforment ces échantillons de routine en fenêtres puissantes sur la maladie, révélant des détails bien trop petits pour les microscopes hospitaliers standards. Ces avancées pourraient aider les médecins à détecter les maladies plus tôt, à mieux comprendre leur progression et à adapter les traitements de façon plus précise.
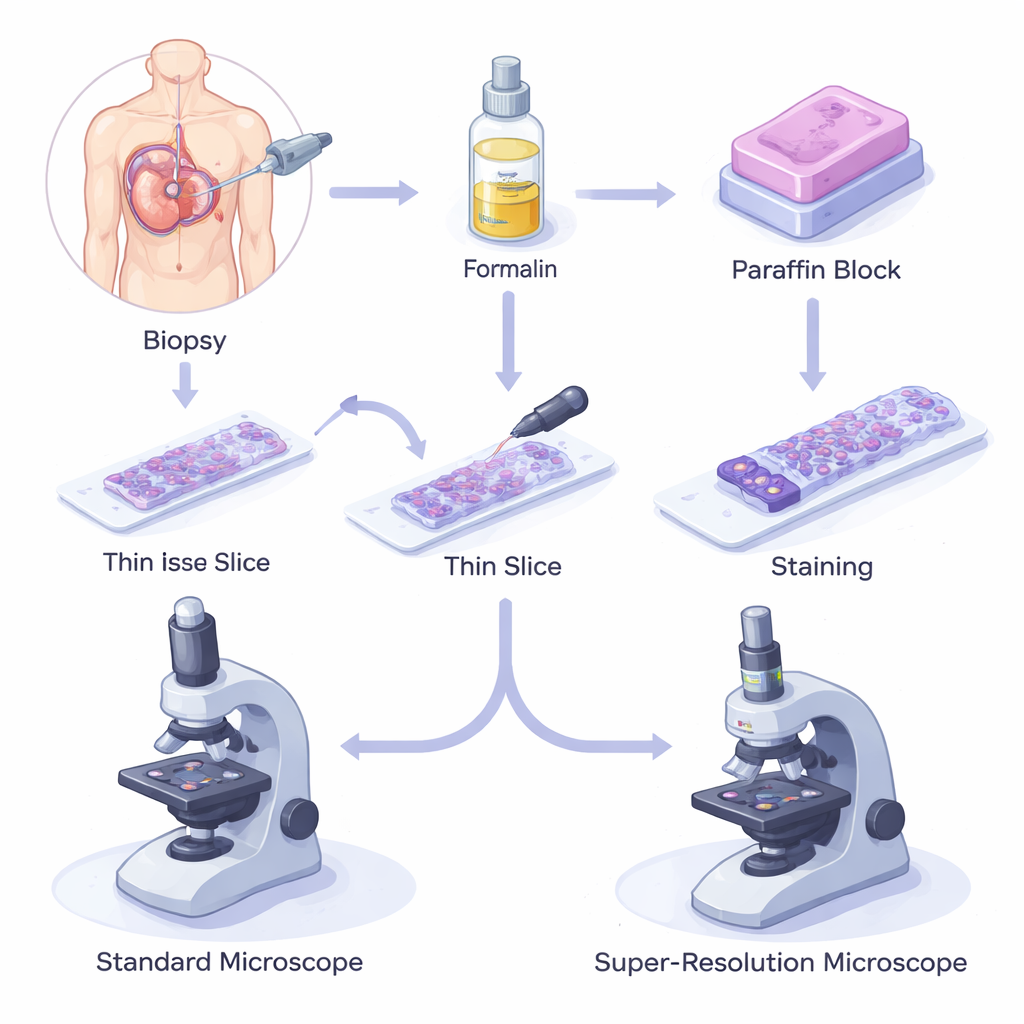
Comment les tissus conservés en cire alimentent la médecine moderne
Lorsqu’un patient subit une biopsie, un petit morceau de tissu est prélevé, fixé dans un produit chimique appelé formol pour arrêter la dégradation, puis inclus dans de la paraffine. Le bloc est découpé en sections aussi fines que des cheveux, déposées sur des lames de verre, colorées et examinées au microscope optique. La méthode dite « formalin‑fixed paraffin‑embedded » (FFPE) est peu coûteuse, fiable et peut préserver des échantillons pendant des décennies à température ambiante. En conséquence, des millions d’échantillons FFPE sont stockés dans des biobanques à travers le monde, soutenant tout, de la biologie fondamentale aux analyses avancées de gènes et de protéines, et formant l’épine dorsale du diagnostic et du pronostic modernes.
Pourquoi les microscopes ordinaires ne suffisent plus
Les microscopes optiques traditionnels sont limités par la physique de la lumière : les détails plus petits qu’environ 250 nanomètres se confondent. De nombreuses structures liées aux maladies — comme les filtres fins des reins, les connexions entre neurones ou de petites modifications de l’architecture de l’ADN dans le noyau — se situent en dessous de cette limite. Le flux de travail actuel combine souvent la microscopie optique standard pour une vue d’ensemble avec la microscopie électronique pour des détails nanométriques, mais cette approche est lente, coûteuse et nécessite une préparation d’échantillon complètement différente. Cliniciens et chercheurs recherchent donc un système unique et flexible capable d’analyser rapidement de larges zones tout en zoomant sur des caractéristiques à l’échelle nanométrique dans les mêmes sections FFPE qu’ils utilisent déjà.
Nouvelles façons d’affiner la vue
Au cours des deux dernières décennies, plusieurs familles de microscopes « à super‑résolution » ont franchi la barrière de résolution traditionnelle en utilisant des marqueurs fluorescents et des astuces optiques. Les méthodes de localisation de molécules uniques activent et désactivent les molécules pour en déterminer la position une par une ; l’illumination structurée projette des motifs lumineux striés sur le tissu et utilise le calcul pour récupérer des détails plus fins ; le déplétion par émission stimulée (STED) sculpte un minuscule point lumineux à l’aide d’un faisceau en forme de beignet ; et les approches basées sur les fluctuations analysent les scintillements subtils de l’image pour en déduire la structure. Une stratégie différente, appelée microscopie d’expansion, évite l’optique complexe en gonflant physiquement le tissu dans un gel, de sorte que des microscopes ordinaires peuvent voir des détails auparavant invisibles. Ces méthodes ont déjà été appliquées à des échantillons FFPE provenant du sein, du côlon, du pancréas, du rein, du cerveau, de la peau, du placenta et d’autres organes, révélant comment les mitochondries changent dans les tumeurs, comment les filtres rénaux dysfonctionnent et comment des agrégats protéiques se forment dans la maladie d’Alzheimer.
Obstacles sur la route d’une adoption courante
Malgré leur promesse, ces techniques ne sont pas encore prêtes à devenir des outils de routine dans la plupart des laboratoires de pathologie. De nombreux systèmes de super‑résolution sont lents, ne couvrent que des champs de vue réduits ou nécessitent des dizaines de milliers d’images pour reconstituer une seule image haute définition, ce qui est impraticable lorsqu’un pathologiste doit évaluer de grandes zones de tissu. Les tissus FFPE eux‑mêmes posent des défis optiques : ils diffusent la lumière, présentent une fluorescence intrinsèque et peuvent masquer les molécules à marquer, autant de facteurs qui peuvent produire des images floues ou des structures artefactuelles. Certaines méthodes exigent des colorants spéciaux, des tampons sur mesure ou des traitements chimiques en plusieurs étapes qui ne s’intègrent pas facilement aux flux de travail histologiques standard. De plus, les instruments commerciaux sont coûteux et complexes à utiliser, et les données générées exigent un traitement informatique intensif et un stockage important.
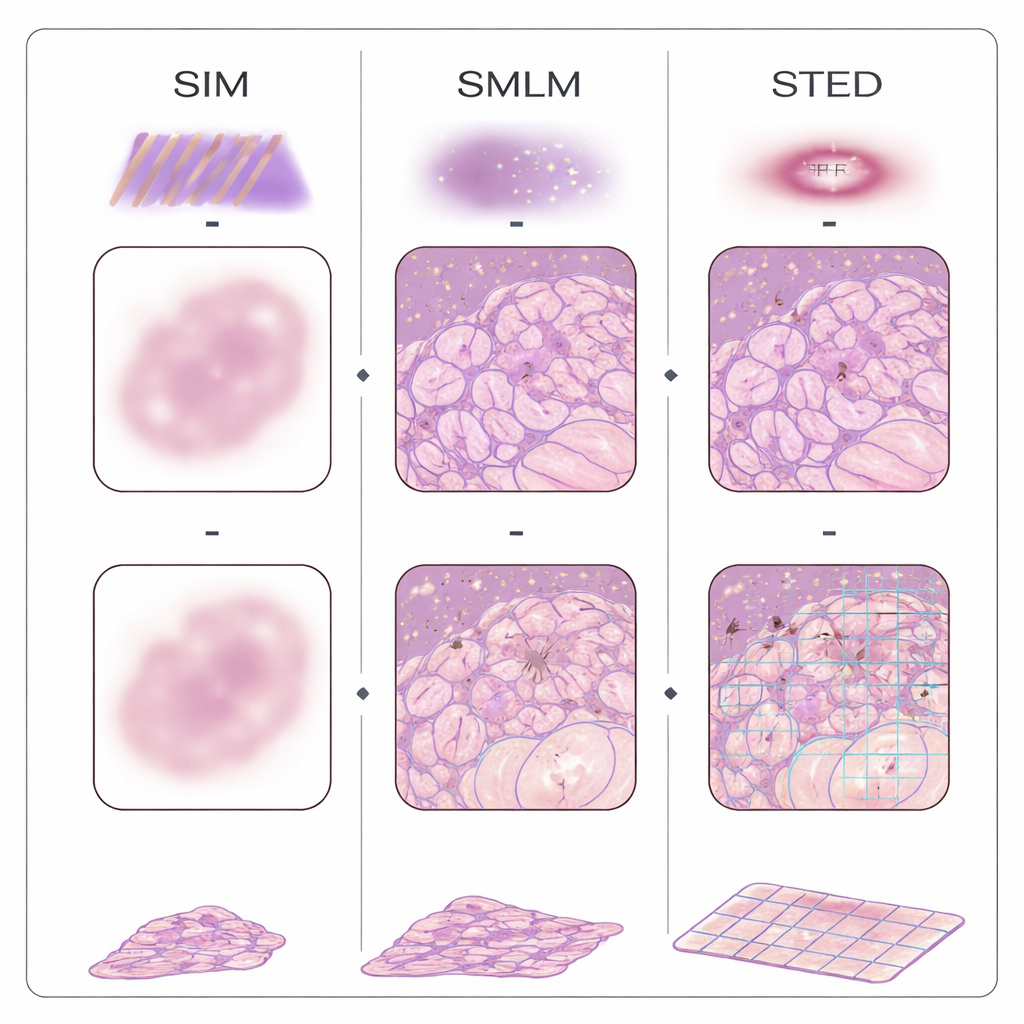
Associer optique intelligente et logiciel intelligent
Pour surmonter ces obstacles, les chercheurs combinent des optiques améliorées avec l’imagerie sans marqueur et l’intelligence artificielle. Des méthodes à haut débit limitées par la diffraction, telles que la ptychographie de Fourier et la microscopie optique non linéaire, peuvent scanner rapidement de larges sections FFPE, même non colorées, et fournir des cartes quantitatives de la structure tissulaire. Les plateformes de pathologie numérique capturent désormais des lames entières à haute résolution et utilisent l’apprentissage automatique pour détecter les tumeurs et évaluer des biomarqueurs comme HER2, Ki‑67 et PD‑L1. Des modèles d’apprentissage profond peuvent même transformer des images basse résolution en vues super‑résolues, réduisant potentiellement le besoin de certains matériels spécialisés tout en exploitant mieux les archives de biopsies existantes.
Ce que cela signifie pour les patients à venir
Les auteurs concluent que la véritable « histologie à super‑résolution » des échantillons FFPE — combinant un détail à l’échelle nanométrique, de la rapidité, un coût raisonnable et une compatibilité avec les routines de laboratoire actuelles — n’est pas encore pleinement réalisée, mais elle est à portée de main. À mesure que les méthodes optiques deviennent plus rapides et plus robustes, et que l’analyse basée sur l’IA mûrit, ces outils pourraient révéler de subtils changements précoces dans les tissus qui passent aujourd’hui inaperçus, améliorer la précision des diagnostics et orienter des décisions thérapeutiques plus personnalisées. À long terme, transformer chaque bloc de cire archivé en une carte haute définition de la maladie pourrait révolutionner la recherche et les soins cliniques.
Citation: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Mots-clés: microscopie à super‑résolution, tissus FFPE, pathologie numérique, imagerie optique, diagnostic du cancer