Clear Sky Science · fr
Les nanozymes repoussent les frontières de la biocatalyse
Petits auxiliaires qui accélèrent la chimie
De la fabrication de la bière à la digestion du dîner, nos vies dépendent d'aides invisibles appelées catalyseurs, qui accélèrent les réactions chimiques. Pendant plus d'un siècle, on a considéré que les catalyseurs biologiques n'étaient que des protéines fragiles, puis, plus tard, de l'ARN catalytique. Cette revue présente les « nanozymes » — de minuscules particules conçues qui se comportent comme des enzymes mais sont fabriquées à partir de matériaux robustes tels que les métaux, les oxydes et le carbone. Ils résistent à la chaleur, au froid et aux conditions agressives, et commencent à remodeler notre façon de penser la chimie dans les systèmes vivants, les maladies, l'industrie et même l'origine de la vie.
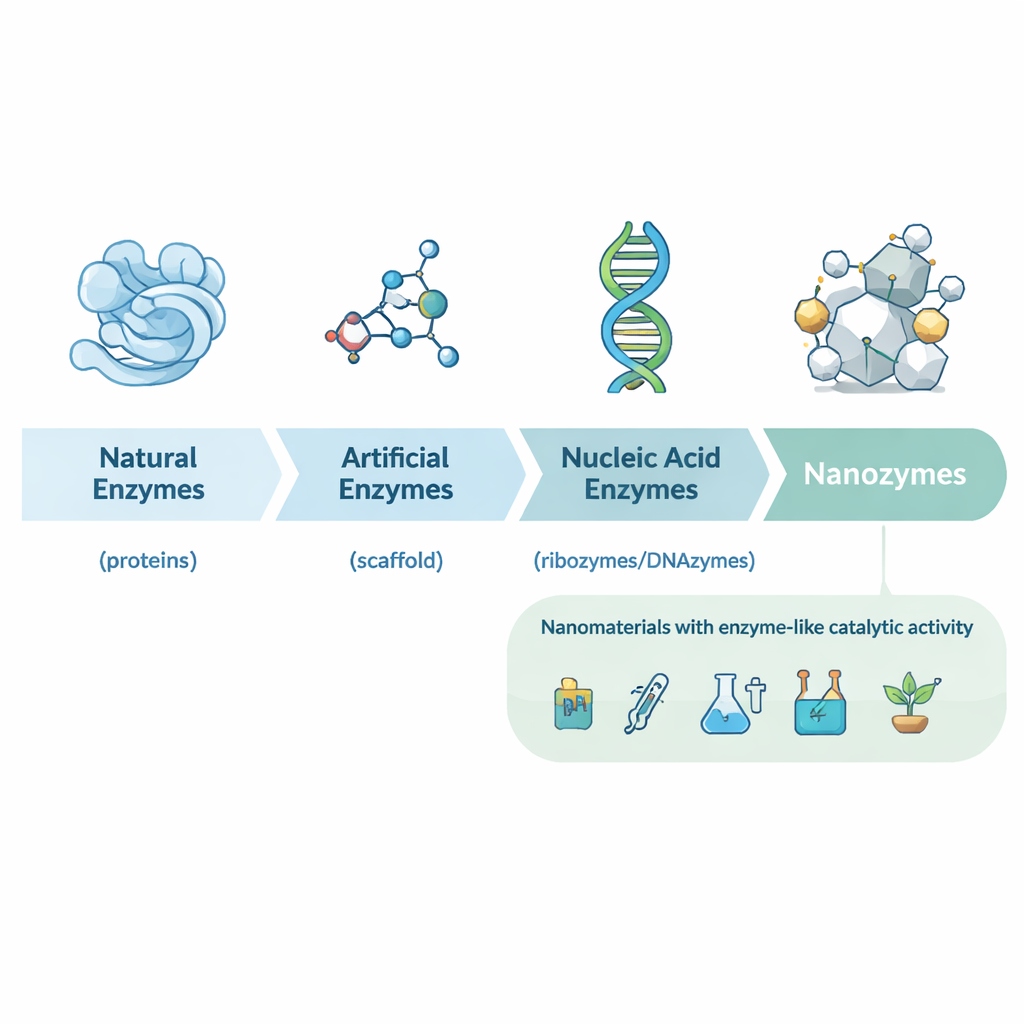
Des enzymes naturelles aux nanocatalyseurs conçus
L'article retrace d'abord l'histoire de la biocatalyse, depuis les premières découvertes d'enzymes protéiques dans la levure et les sucs gastriques jusqu'aux ribozymes (ARN catalytique) et à une large gamme d'enzymes artificielles construites à partir de petites molécules et d'anticorps. Ces catalyseurs traditionnels sont puissants mais souvent coûteux, instables et difficiles à produire en masse. Au début des années 2000, des chercheurs ont découvert que certains nanomatériaux — par exemple des nanoparticules d'oxyde de fer — pouvaient imiter le comportement d'enzymes classiques comme la peroxydase de raifort. Cela a conduit au concept de nanozymes : des particules à l'échelle nanométrique dont la structure propre confère une activité semblable à celle des enzymes, plutôt que d'être porteuses de protéines ou de petits catalyseurs moléculaires attachés.
Ce qui distingue les nanozymes
Contrairement aux enzymes, qui possèdent une poche active unique et précisément façonnée, les nanozymes exposent de nombreux points actifs à la surface. Ces points peuvent se situer aux arêtes cristallines, aux défauts ou aux interfaces entre deux matériaux, et, collectivement, ils peuvent convertir de nombreuses molécules simultanément. Un seul site actif sur un nanozyme est généralement moins efficace que celui d'une enzyme, mais une nanoparticule peut héberger des milliers de tels sites, de sorte que sa puissance catalytique globale peut rivaliser ou dépasser celle des enzymes naturelles. Leur activité peut également être modulée en changeant la taille, la forme, le dopage chimique et les revêtements de surface — comme on ajuste l'architecture et le câblage d'une petite machine. Étant fabriqués à partir de solides robustes plutôt que de protéines repliées et fragiles, les nanozymes continuent de fonctionner à des températures élevées, basses ou à des niveaux de sel qui désactiveraient rapidement la plupart des enzymes.
Comment fonctionnent les nanozymes et comment on les mesure
Les auteurs montrent que les nanozymes suivent souvent les mêmes règles cinétiques de base que les biochimistes appliquent aux enzymes, comme le comportement de Michaelis–Menten, où la vitesse de réaction dépend de la facilité avec laquelle un catalyseur lie et convertit son substrat. Mais il y a des nuances importantes. Une particule peut porter plusieurs types de sites actifs, de sorte qu'un seul nanozyme peut réaliser différentes réactions ou même des réactions contradictoires, comme à la fois produire et détruire des espèces réactives de l'oxygène. Cela peut produire des courbes cinétiques complexes « non manuels » qui cachent plusieurs processus sous une tendance lisse. La revue explique comment les chercheurs décomposent ces comportements, estiment le nombre réel de sites actifs et comparent l'activité globale de différents nanozymes en utilisant des unités standardisées, autant d'étapes cruciales pour transformer un matériau intrigant en un outil fiable.
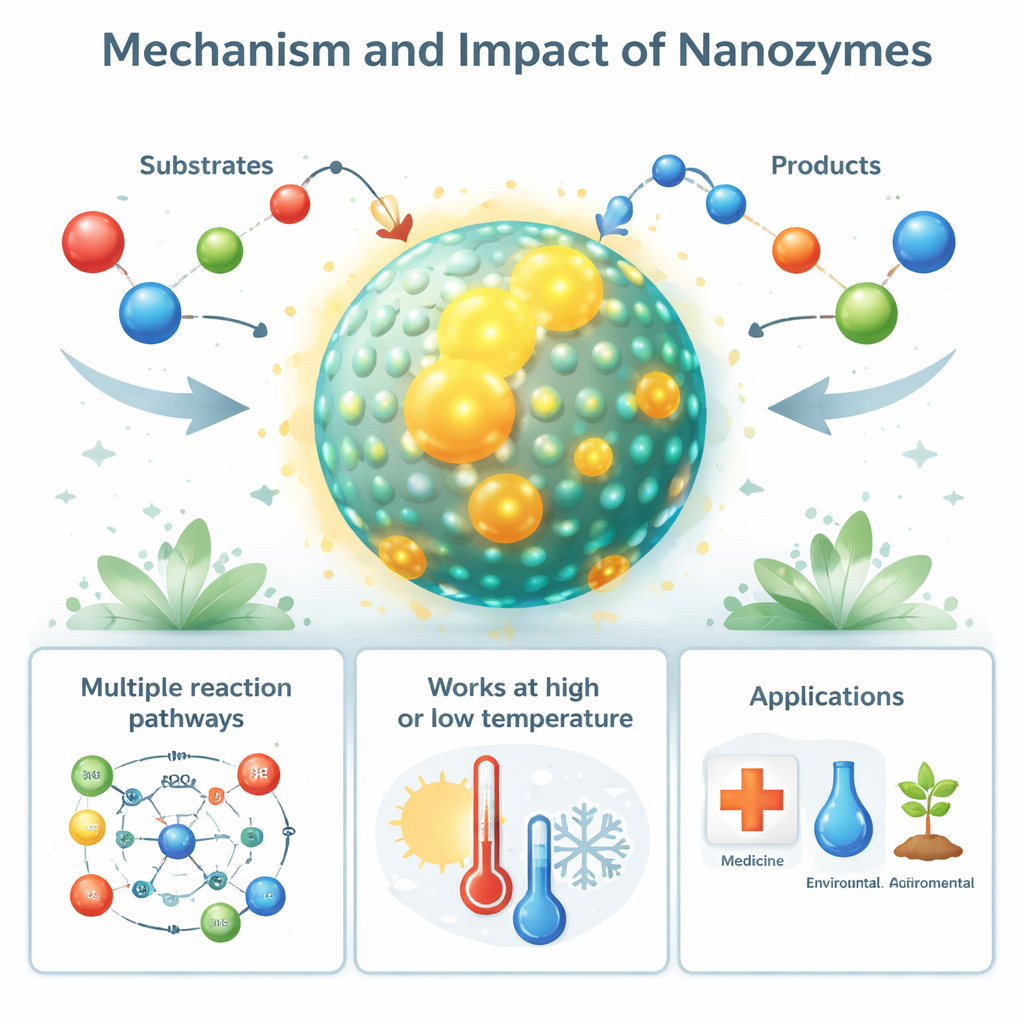
Des nanozymes naturels aux applications réelles
Fait intrigant, le comportement de type nanozyme n'est pas limité au laboratoire. Certaines nanostructures biologiques, comme des cages protéiques remplies de fer (ferritine) et des particules magnétiques chez les bactéries (magnétosomes), agissent comme des nanozymes naturels qui aident à contrôler les espèces réactives de l'oxygène nuisibles. Même des fibres protéiques associées à des maladies, comme les dépôts amyloïdes dans la maladie d'Alzheimer, peuvent adopter une activité peroxydase de type nanozyme qui endommage les cellules voisines. Du côté des applications, les nanozymes synthétiques sont utilisés comme substituts moins coûteux et plus robustes aux enzymes dans les tests diagnostics, les biosenseurs et les dosages industriels. Leur capacité à générer ou éliminer des espèces réactives de l'oxygène est exploitée pour tuer des cellules tumorales et des bactéries, protéger les tissus contre le stress oxydatif et aider les cultures à résister à la sécheresse, à la salinité et à la pollution.
Concevoir la prochaine génération de catalyseurs intelligents
En regardant vers l'avenir, les auteurs soulignent les défis clés : identifier précisément les structures atomiques qui servent de sites actifs, améliorer la sélectivité des réactions afin que les nanozymes n'agissent que là et quand on le souhaite, et garantir la sécurité et la stabilité à l'intérieur du corps. Ils citent l'imagerie avancée, les simulations au niveau quantique et l'apprentissage automatique comme des outils puissants pour prédire et optimiser les performances des nanozymes. Parce qu'ils peuvent fonctionner dans des conditions extrêmes, répondre à la lumière, la chaleur, le son ou des champs magnétiques, et parfois effectuer plusieurs réactions en séquence, ils pourraient soutenir de nouvelles thérapies, des technologies environnementales et des procédés industriels. La revue conclut que les nanozymes élargissent la définition même de la biocatalyse et pourraient même offrir des indices sur la façon dont des catalyseurs primitifs ont autrefois alimenté la chimie de la vie précoce.
Citation: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Mots-clés: nanozymes, biocatalyse, nanoparticules, mimétiques d'enzymes, espèces réactives de l'oxygène