Clear Sky Science · fr
Détection par nanopore de la conformation des protéines et des peptides pour des applications au point de soin
Pourquoi de minuscules formes de protéines pourraient changer votre prochain bilan
À mesure que les populations vieillissent, des maladies comme Alzheimer, Parkinson, les maladies cardiaques et le cancer deviennent plus fréquentes. Nombre de ces affections commencent lorsque des protéines vitales et de petits fragments protéiques (peptides) modifient subtilement leur forme bien avant l’apparition des symptômes. Les tests cliniques actuels mesurent généralement la quantité d’un biomarqueur plutôt que si sa conformation est normale ou altérée. Cet article explore une technologie appelée détection par nanopore, qui peut « sentir » électriquement la forme et la chimie de molécules protéiques individuelles, et soutient qu’elle pourrait devenir la base de futurs tests au point de soin, exécutés en quelques minutes sur un petit appareil.
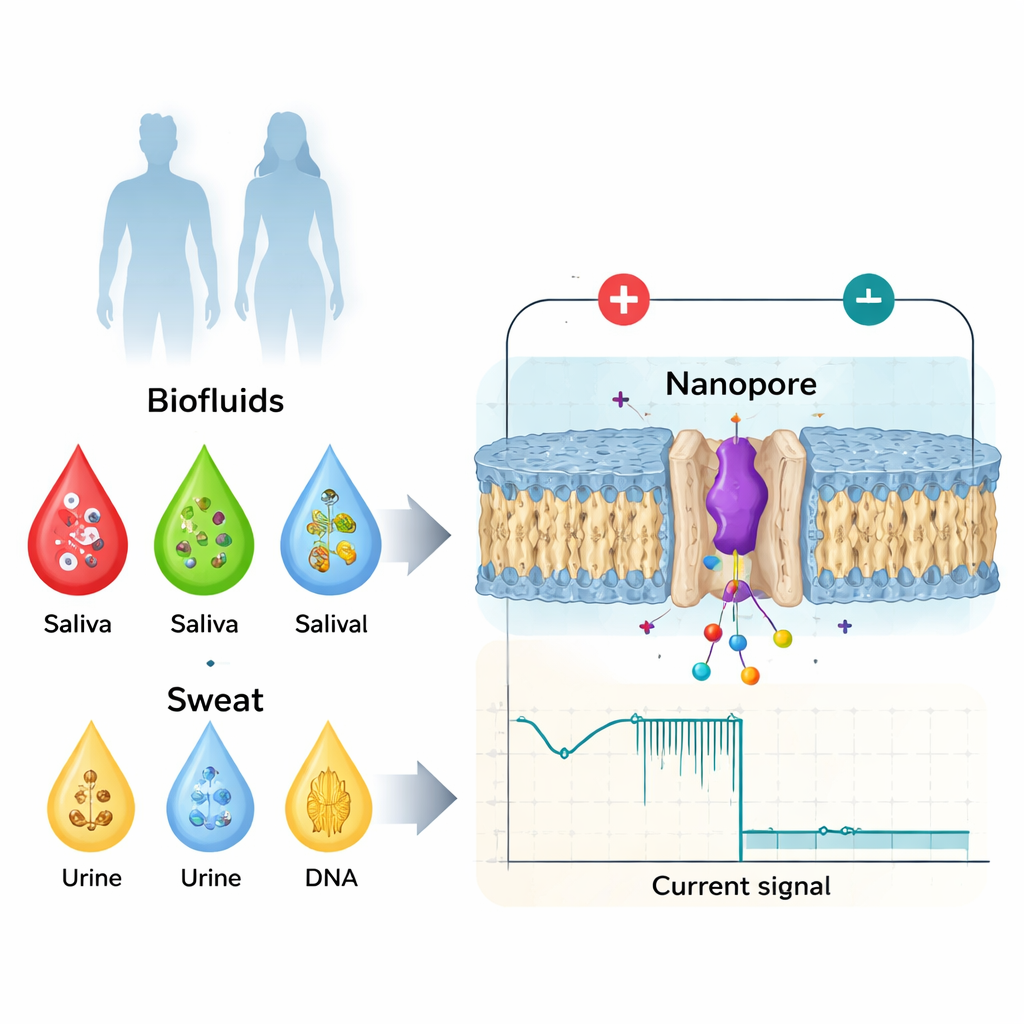
Des analyses sanguines simples aux biomarqueurs sensibles à la conformation
Les médecins utilisent déjà de nombreux biomarqueurs issus du sang, de la salive, de l’urine ou de la sueur — comme des protéines, des hormones ou de petites molécules — pour suivre la santé et la maladie. Traditionnellement, l’attention porte sur des changes macroscopiques : des copies supplémentaires d’une protéine, un ADN endommagé ou la présence d’un composant viral. Mais la biologie est plus subtile. Une même protéine peut être activée ou désactivée par de minuscules changements de son architecture, par des étiquettes chimiques ajoutées après sa synthèse, ou par des versions miroir de ses éléments constitutifs. Ces petites modifications peuvent altérer la liaison d’une protéine à ses partenaires, sa propension à s’agréger ou sa transmission de signaux, et sont liées à des problèmes de coagulation, des maladies neurodégénératives et le cancer. Les outils hospitaliers classiques comme la spectrométrie de masse, les tests à base d’anticorps et l’imagerie haute résolution sont puissants, mais coûteux, lents, nécessitent du personnel hautement qualifié et, en général, ne peuvent pas être déployés comme des dispositifs rapides et simples au point de soin.
Ce que fait différemment un nanopore
La détection par nanopore renverse le problème. Plutôt que de faire la moyenne sur des billions de molécules, elle examine chacune individuellement lorsqu’elle traverse un minuscule trou dans une membrane, large d’à peine quelques milliardièmes de mètre. Une tension est appliquée pour faire circuler des ions à travers le pore et créer un courant électrique stable. Lorsqu’une protéine ou un peptide entre dans le pore, il bloque partiellement ce courant. La profondeur de la chute de courant, sa durée et les détails fins de sa forme dépendent de la taille, de la charge et de la conformation (son repliement tridimensionnel) de la molécule. En concevant soigneusement le pore — en utilisant soit des protéines ingénierées soit des matériaux en état solide — les chercheurs peuvent confiner les biomolécules individuelles assez longtemps pour obtenir de riches « empreintes » électriques qui distinguent non seulement différentes protéines, mais aussi des variantes subtiles d’un même biomarqueur.
Lire, molécule par molécule, les changements pertinents pour la maladie
La revue met en lumière comment les nanopores ont déjà été utilisés pour résoudre des différences d’importance médicale que d’autres méthodes peinent à détecter. Ils peuvent différencier des peptides qui diffèrent d’un seul acide aminé, détecter des variantes de l’hémoglobine liées à la maladie directement dans le sang, et distinguer de courts peptides de type hormonal qui varient d’un seul élément constitutif ou même d’une forme miroir de cet élément. Les nanopores peuvent aussi sentir des modifications post-traductionnelles — de petites étiquettes chimiques comme des groupes phosphate, sucre ou sulfate — qui contribuent à contrôler si des protéines impliquées dans Alzheimer, Parkinson, la coagulation sanguine ou le cancer se comportent normalement ou pathologiquement. Dans certaines expériences, une enzyme unique ou une protéine de liaison est maintenue à l’intérieur du pore, et les changements de son signal électrique révèlent, en temps réel, comment elle se lie à des partenaires ou réalise des réactions, exposant potentiellement des voies dysfonctionnelles dans la maladie.
Vers des tests rapides au chevet
Parce que chaque événement de blocage correspond à une molécule, les dispositifs à nanopore peuvent être extrêmement sensibles, détectant parfois seulement quelques milliers de copies d’un biomarqueur dans un fluide complexe. Les auteurs discutent des stratégies pour surmonter les obstacles clés à l’utilisation clinique : augmenter le taux de capture des molécules rares, stabiliser les membranes ou utiliser des pores hybrides solide–biologiques, et recourir à l’apprentissage automatique pour classifier automatiquement des motifs électriques complexes en catégories diagnostiques claires. Ils montrent aussi comment des approches indirectes — telles que l’attachement d’étiquettes d’ADN ou de partenaires de liaison — peuvent amplifier des signaux faibles ou permettre la mesure simultanée de plusieurs biomarqueurs, tout en préservant beaucoup des détails conformationnels qui rendent les nanopores uniques.
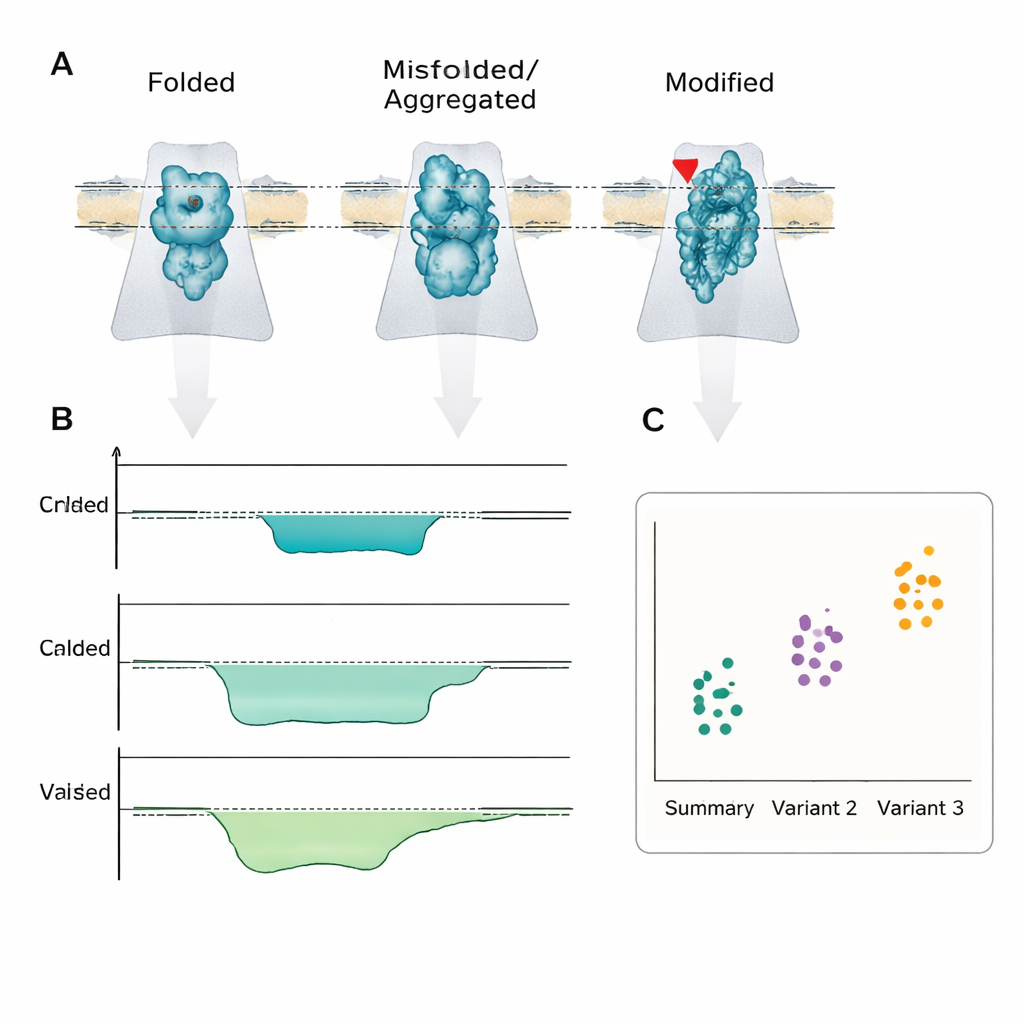
Ce que cela pourrait signifier pour les patients
Le message central est que la maladie est souvent déterminée moins par la quantité de protéine présente que par la forme ou la version chimique qui est en jeu. La détection par nanopore est l’une des rares technologies capables de lire directement ces différences au niveau de la molécule unique, assez rapidement et simplement pour être intégrée dans des appareils portables. Bien que des défis d’ingénierie et de standardisation subsistent, les auteurs soutiennent que, à l’instar des séquenceurs d’ADN à nanopore entrés en clinique, les capteurs de protéines et de peptides à nanopore pourraient à terme fournir des tests rapides au chevet qui non seulement indiquent « quelque chose ne va pas », mais révèlent aussi le repliement moléculaire ou la modification exacte à l’origine de l’état du patient.
Citation: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Mots-clés: détection par nanopore, biomarqueurs protéiques, diagnostics au point de soin, modifications post-traductionnelles, maladies de conformation