Clear Sky Science · fr
Un long chemin vers des génomes de plantes médicinales fiables et complets
Pourquoi les cartes de l’ADN des plantes comptent pour la santé humaine
Beaucoup des médicaments les plus puissants d’aujourd’hui — des anticancéreux comme le paclitaxel aux analgésiques comme la morphine, en passant par l’antipaludique artémisinine — proviennent des plantes. Pourtant, pour la plupart des plantes médicinales, les scientifiques ne disposent toujours pas d’un « manuel d’instructions » complet de leur ADN. Cette revue explique comment les nouvelles technologies génomiques transforment notre capacité à lire ces manuels, pourquoi les génomes végétaux actuels sont souvent incomplets ou comportent des erreurs, et comment des génomes véritablement précis pourraient débloquer de meilleurs médicaments, une production plus durable et une conservation améliorée d’espèces précieuses.
La promesse de lire les plans des plantes médicinales
Depuis des millénaires, les populations se sont appuyées sur des remèdes à base de plantes, et la pharmacologie moderne puise toujours largement dans les produits naturels végétaux. Ces molécules spécialisées — alcaloïdes, terpénoïdes, composés phénoliques et bien d’autres — sont synthétisées par des voies métaboliques complexes encodées dans l’ADN des plantes. Jusqu’à récemment, les chercheurs devaient reconstituer ces voies avec des outils lents et laborieux, comme le marquage isotopique et le clonage gène par gène. L’arrivée du séquençage d’ADN haute capacité et abordable a changé la donne. En février 2025, des génomes de 431 plantes médicinales (représentant 203 espèces) avaient été séquencés, offrant aux chercheurs une manière systématique de rechercher les gènes de ces voies, de comprendre la régulation des composés d’intérêt et d’explorer l’évolution de ces chimies.
Un boom du séquençage, mais de nombreux génomes imparfaits
Les technologies de séquençage longues lectures de PacBio et Oxford Nanopore, associées aux données courtes d’Illumina et à des méthodes de cartographie au niveau des chromosomes comme le Hi‑C, ont considérablement amélioré la qualité des génomes végétaux. Près de la moitié des assemblages de plantes médicinales ont été publiés au cours des trois dernières années seulement, et la plupart des génomes récents sont désormais construits à l’échelle chromosomique. Cependant, la revue montre que la quantité a devancé la qualité. Plus de la moitié des génomes existent uniquement sous une première version, beaucoup demeurent au stade de brouillon, et seules 11 plantes médicinales disposent d’assemblages « télomère‑à‑télomère » (T2T) sans lacunes qui capturent intégralement les centromères et autres régions répétitives. Les métriques standard comme le N50 (mesure de la contiguïté) et les scores BUSCO (mesure des gènes conservés) paraissent globalement encourageantes, mais elles peuvent masquer des lacunes critiques là même où se trouvent des gènes biosynthétiques clés.
Lacunes cachées là où devraient se trouver les gènes de la médecine
Pour évaluer l’utilité réelle des génomes actuels, les auteurs ont examiné des gènes de voies connus et validés expérimentalement dans neuf plantes médicinales bien étudiées. Même dans certains assemblages au niveau chromosomique, des enzymes importantes pour des composés tels que les ginsénosides du ginseng ou l’artémisinine d’Artemisia annua étaient soit complètement absentes, soit seulement partiellement représentées. Dans d’autres cas, les gènes étaient présents dans la séquence brute du génome mais absents ou tronqués dans les annotations officielles, ce qui les rend difficiles à repérer. Un exemple frappant vient de la plante productrice de coumarines Peucedanum praeruptorum : un ancien génome au niveau chromosomique avait cassé un gène clé et en avait manqué deux autres ; un nouvel assemblage T2T a non seulement restauré ces gènes, mais a aussi révélé que plusieurs d’entre eux se trouvent regroupés dans un amas de gènes biosynthétiques très compact. Ce type de carte de cluster est exactement ce dont les chercheurs ont besoin pour concevoir des plantes ou des microbes capables de produire des médicaments plus efficacement.
Pourquoi les génomes de plantes sont si difficiles à assembler
Les plantes médicinales posent des défis particuliers qui vont au‑delà de ceux rencontrés pour de nombreuses espèces cultivées. Leurs génomes présentent souvent de forts niveaux d’hétérozygotie (de nombreuses différences d’ADN entre les deux copies de chaque chromosome), de fréquentes polyploïdies (plusieurs jeux de chromosomes) et de grandes fractions d’ADN répétitif — des caractéristiques qui embrouillent les algorithmes d’assemblage et provoquent des cassures ou des erreurs d’assemblage. Environ un tiers des plantes médicinales séquencées ont des génomes contenant plus de 70 % de séquences répétitives, et plus d’un quart présentent une hétérozygotie très élevée. Produire des lignées fortement endogames ou isoler des tissus haploïdes peut aider, mais cela reste lent, coûteux ou biologiquement difficile pour de nombreuses espèces. De nouvelles stratégies qui assemblent séparément chaque haplotype parental, ainsi que des algorithmes plus puissants adaptés aux génomes riches en répétitions et polyploïdes, commencent à atténuer ces obstacles mais ne sont pas encore la norme.
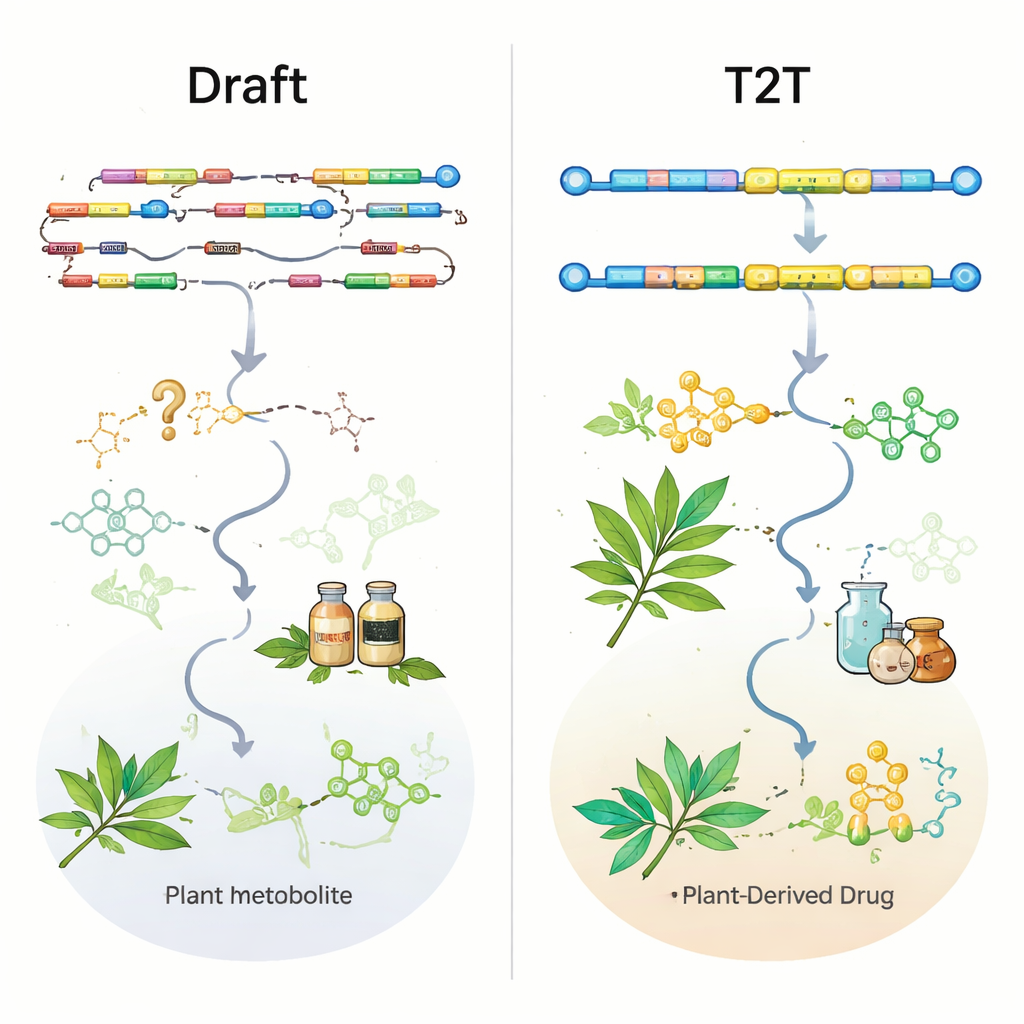
Des génomes aux nouveaux médicaments et orientations futures
Lorsque les génomes sont suffisamment bons, ils deviennent de puissants moteurs de découverte. Les chercheurs peuvent combiner les données de génome entier avec la transcriptomique, la métabolomique et la biologie synthétique pour identifier les enzymes, les gènes régulateurs et les amas de gènes biosynthétiques qui contrôlent la production de composés à forte valeur. Ces connaissances ont déjà permis la reconstruction de voies végétales complexes — telles que celles du vinblastine, du paclitaxel et de nombreux autres médicaments — dans la levure ou des plantes modèles, ouvrant la voie à une bioproduction stable et à grande échelle. Pour l’avenir, les auteurs préconisent un passage d’« un génome approximatif par espèce » à des assemblages multiples, de haute qualité, T2T et résolus en haplotypes, qui capturent la diversité intra‑spécifique, à l’instar des pan‑génomes en recherche sur les cultures. Coupler ces génomes de référence avec des re‑séquençages à grande échelle, un phénotypage avancé et les approches émergentes de transcriptomique unicellulaire et spatiale devrait éclairer comment l’environnement, le type cellulaire et les réseaux géniques interagissent pour façonner la chimie médicinale.
Ce que cela signifie pour les patients et la planète
Le message central de la revue est que des génomes de plantes médicinales fiables et complets ne sont pas un luxe ; ils constituent la base permettant de transformer des siècles de savoirs herbaires en thérapies modernes et précises. De meilleurs génomes aideront les scientifiques à trouver les étapes manquantes des voies médicamenteuses, à concevoir des approvisionnements plus sûrs et plus abondants de médicaments critiques, et à identifier des espèces alternatives capables de produire les mêmes composés. Ils guideront également la conservation et l’utilisation durable des plantes médicinales menacées, dont la plupart ne disposent toujours d’aucune ressource génomique. En bref, achever la cartographie précise de ces génomes pourrait accélérer la découverte de médicaments, stabiliser les chaînes d’approvisionnement et préserver la diversité botanique — autant d’enjeux qui, in fine, bénéficient à la santé humaine.
Citation: Cheng, LT., Wang, ZL., Zhu, QH. et al. A long road ahead to reliable and complete medicinal plant genomes. Nat Commun 16, 2150 (2025). https://doi.org/10.1038/s41467-025-57448-8
Mots-clés: génomique des plantes médicinales, amas de gènes biosynthétiques, génomes télomère-à-télomère, biosynthèse de produits naturels, biologie synthétique