Clear Sky Science · fr
Électronique inspirée du vivant : interfaces neuronales souples, biohybrides et « vivantes »
Dispositifs doux pour le système nerveux
Des interfaces cerveau‑ordinateur qui permettent à des personnes de déplacer des bras robotiques aux stimulateurs cérébraux profonds qui atténuent les symptômes de la maladie de Parkinson, les appareils qui communiquent avec nos nerfs passent rapidement de la science‑fiction à la réalité médicale. Pourtant, les dispositifs actuels restent, au fond, des pièces de métal et de silicium insérées dans des tissus aussi mous que de la gelée. Cette revue explique comment les scientifiques repensent ces outils pour qu’ils ressemblent davantage au corps lui‑même — plus souples, plus biologiquement actifs et même partiellement vivants — dans l’espoir de rendre les implants neuronaux plus sûrs, plus durables et capables d’aider le cerveau et les nerfs à se réparer.
Pourquoi les implants traditionnels montrent leurs limites
Les implants neuronaux conventionnels, tels que les arrays d’Utah et les sondes de stimulation profonde, sont fabriqués à partir de métaux rigides et de silicium. Ces matériaux sont des millions de fois plus raides que le tissu cérébral, qui se comporte davantage comme de la gelée que comme du verre. Ce décalage rend difficile la conformité des dispositifs aux mouvements et formes subtiles du cerveau. À mesure que le tissu se déplace à chaque battement de cœur et respiration, des électrodes rigides frottent et tirent, provoquant de petites lésions. Le corps reconnaît ces objets étrangers et déclenche une réponse immunitaire, les isolant derrière une cicatrice dense de cellules de soutien. Avec le temps, cette cicatrice augmente la résistance électrique entre l’appareil et les neurones voisins, dégradant la qualité du signal et limitant la durée pendant laquelle un implant peut fonctionner de manière fiable.
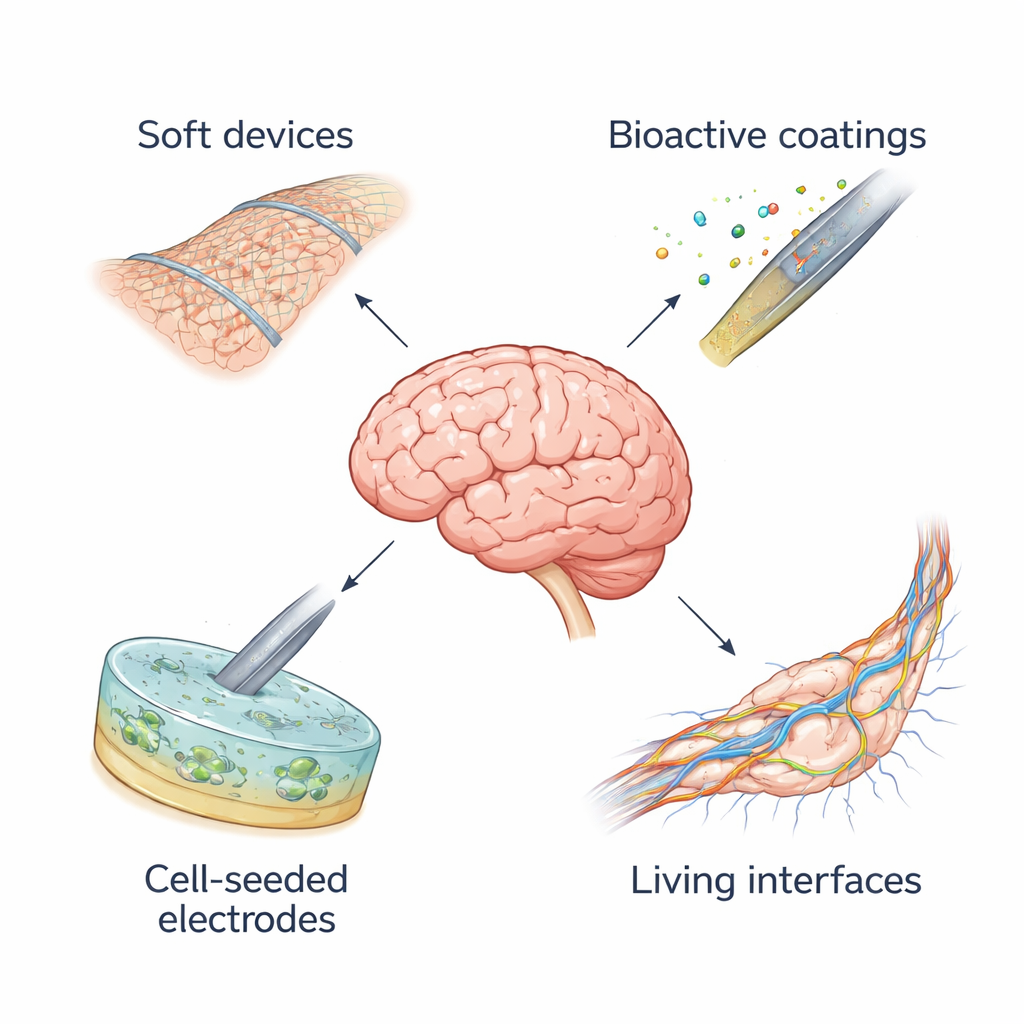
Des dispositifs souples qui suivent les mouvements du cerveau
Pour réduire ces dommages, les chercheurs conçoivent des électroniques « biomimétiques » — des dispositifs dont les propriétés physiques font écho à celles du tissu qu’ils touchent. Plutôt que des tiges épaisses et rigides, les ingénieurs fabriquent aujourd’hui des films ultra‑fins, des fibres flexibles et des structures en treillis ouvertes capables de se plier et de se courber comme des cellules vivantes. Des polymères souples, des caoutchoucs extensibles et des gels riches en eau aident à rapprocher la rigidité de celle du cerveau et à amortir les forces qui déclenchent l’inflammation. Certains de ces dispositifs intègrent des plastiques conducteurs ou des nanomatériaux comme le graphène dans des supports flexibles, préservant des enregistrements électriques de haute qualité tout en réduisant fortement la rigidité. Plusieurs interfaces souples, y compris des implants cérébraux filiformes et des grilles en film mince reposant à la surface du cerveau, entrent déjà dans des essais cliniques, montrant que des mécanismes plus doux peuvent coexister avec une électronique avancée.
Des surfaces qui attirent les cellules au lieu de les repousser
Rendre les dispositifs plus souples n’est qu’une partie de la solution. Les cellules du cerveau réagissent aussi au « ressenti » chimique de la surface d’un implant. L’électronique bioactive exploite cela en recouvrant les électrodes d’ingrédients biologiques que le système nerveux connaît et accepte, tels que des protéines de l’ échafaudage naturel entourant les cellules ou de courtes molécules qui favorisent la croissance nerveuse. Ces revêtements peuvent encourager les neurones à se rapprocher des électrodes, atténuer l’activité des cellules immunitaires et amincir la cicatrice qui se forme habituellement. Certains revêtements sont conçus pour libérer lentement des médicaments — comme des anti‑inflammatoires ou des facteurs de croissance — exactement là où ils sont nécessaires, transformant un fil passif en une interface intelligente délivrant des médicaments. Le défi à venir est de maintenir ces couches délicates stables et efficaces pendant des années à l’intérieur du corps.
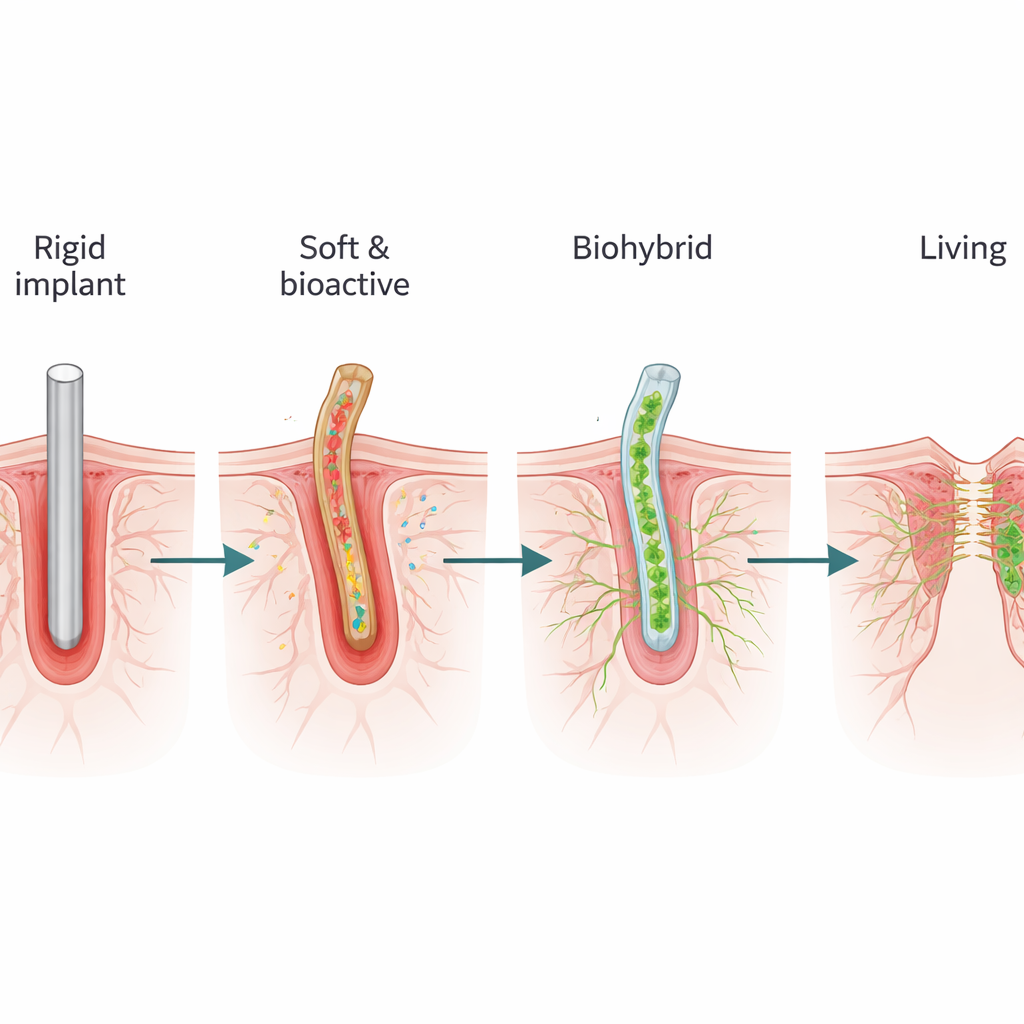
Mélanger des cellules vivantes avec des circuits
Plus loin sur le spectre, les dispositifs « biohybrides » incorporent de véritables cellules vivantes dans ou sur l’électronique. Dans une stratégie, des cellules sont cultivées sur des électrodes avant l’implantation, parfois au sein d’un hydrogel souple qui imite le tissu cérébral. Une fois dans le corps, cette couche vivante peut sécréter des molécules utiles, attirer des fibres nerveuses et former un pont biologique entre le matériel rigide et le tissu hôte. Les premières versions, telles que des électrodes en forme de cône qui attiraient les fibres nerveuses à l’intérieur, ont fourni des enregistrements stables pendant plus d’une décennie chez l’humain. Des approches plus récentes ensemencent les électrodes avec des cellules souches, des neurones ou des cellules musculaires, visant non seulement à lire ou stimuler l’activité mais aussi à régénérer des voies endommagées et restaurer des fonctions perdues, comme le mouvement après une lésion nerveuse. Ces systèmes doivent résoudre des problèmes difficiles de maintien en vie des cellules, d’orientation de leur croissance et d’empêcher qu’elles ne migrent ou forment des connexions indésirables.
« Fils » entièrement vivants pour le cerveau
À l’extrémité la plus ambitieuse se trouvent les « interfaces vivantes », construites entièrement à partir de matériaux biologiques et de cellules. Ici, de longs paquets de fibres nerveuses cultivées en laboratoire agissent comme des câbles vivants pouvant être implantés pour reconnecter des régions cérébrales ou franchir des lacunes dans des nerfs endommagés. Plutôt que de faire passer un courant à travers du métal, ces constructions utilisent des synapses naturelles — les points de contact entre neurones — pour transmettre des signaux. Dans le cerveau, de tels chemins vivants ont été conçus pour véhiculer des messages chimiques spécifiques, comme la dopamine, suscitant l’espoir de traiter des affections telles que la maladie de Parkinson en reconstruisant des circuits perdus plutôt qu’en masquant les symptômes par des impulsions électriques. Parce que ces dispositifs sont entièrement biologiques, ils s’intègrent bien au tissu hôte, mais ils exigent de nouvelles méthodes pour les surveiller et les contrôler, reposant souvent sur l’imagerie et la stimulation basées sur la lumière plutôt que sur des fils traditionnels.
Ce que cela signifie pour les soins futurs du cerveau et des nerfs
Ensemble, les interfaces souples, bioactives, biohybrides et entièrement vivantes dessinent une feuille de route vers des technologies neuronales qui coopèrent avec le corps plutôt que de lui être opposées. Une mécanique plus souple et des surfaces plus accueillantes peuvent réduire la formation de cicatrices et prolonger la durée de vie des dispositifs ; l’ajout de cellules vivantes et, finalement, de voies tissulaires entières pourrait permettre aux implants de réparer ou remplacer des circuits endommagés, au lieu de se contenter d’enregistrer leur activité. De nombreux obstacles scientifiques, de fabrication et réglementaires subsistent, en particulier pour les systèmes contenant des cellules et les systèmes entièrement vivants. Mais la direction est claire : les implants cérébraux et nerveux de demain ressembleront et se comporteront probablement moins comme des gadgets rigides et davantage comme des pièces de tissu vivant soigneusement conçues.
Citation: Boufidis, D., Garg, R., Angelopoulos, E. et al. Bio-inspired electronics: Soft, biohybrid, and “living” neural interfaces. Nat Commun 16, 1861 (2025). https://doi.org/10.1038/s41467-025-57016-0
Mots-clés: interfaces neuronales, électronique biohybride, implants souples, interface cerveau‑ordinateur, ingénierie tissulaire