Clear Sky Science · fr
Éclairer l’impact de l’acétylation N-terminale : de la protéine à la physiologie
Comment de minuscules étiquettes chimiques peuvent modifier le comportement des protéines
Chaque cellule de votre corps est remplie de protéines qui doivent se replier correctement, atteindre le bon endroit, s’assembler en machines moléculaires et être éliminées lorsqu’elles sont endommagées. Cet article de revue explore une modification chimique subtile mais extrêmement répandue à l’extrémité d’un grand nombre de protéines — appelée acétylation N‑terminale — et montre comment ce petit « chapeau » aide à contrôler tout, de la croissance cellulaire et des réponses au stress au développement cardiaque et aux fonctions cérébrales.
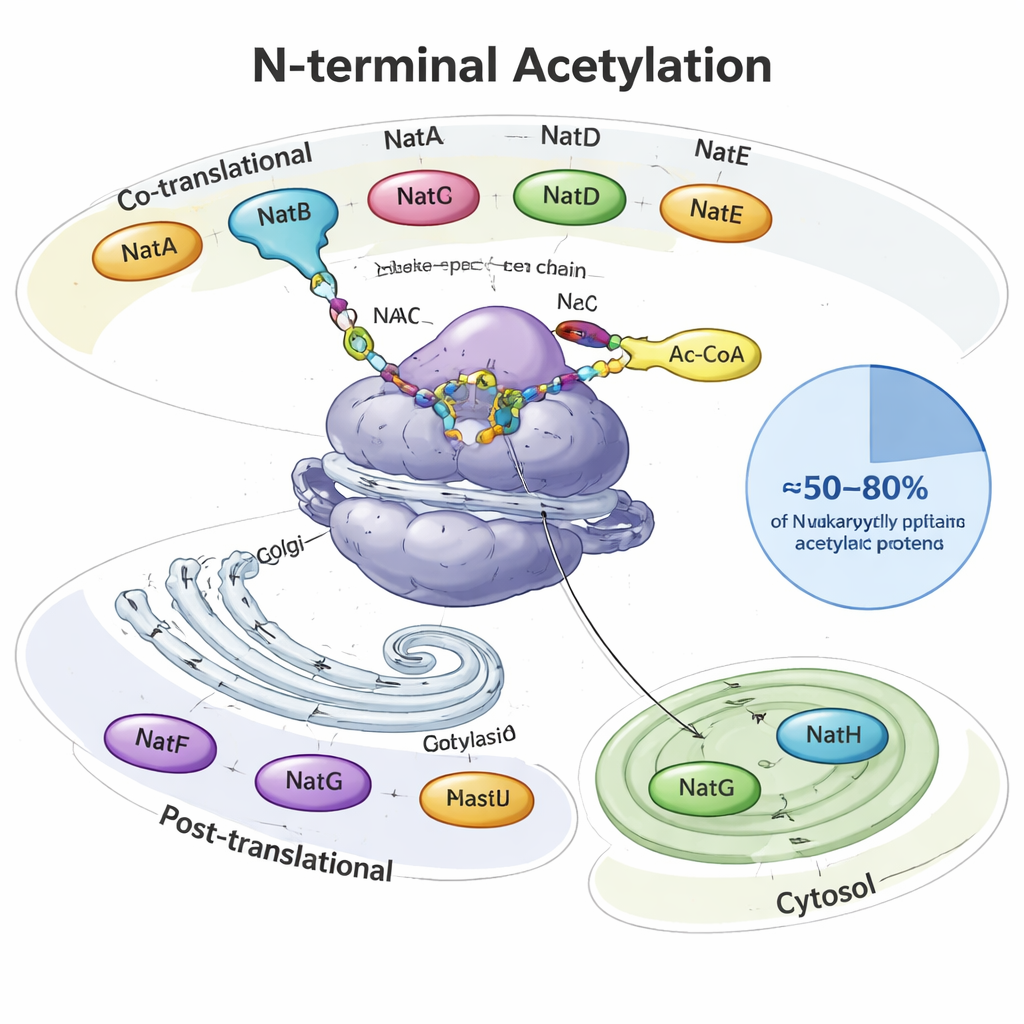
Le cap protéique que la plupart d’entre nous n’ont jamais entendu nommer
Quand une protéine est synthétisée, elle sort de l’usine cellulaire des protéines, le ribosome, comme un fil en croissance. À son tout début — le N‑terminus — de nombreuses protéines eucaryotes reçoivent un groupe acétyle, un petit cap à deux carbones. Des enzymes spécialisées appelées acétyltransférases N‑terminales (NATs) accomplissent ce travail, en utilisant une molécule métabolique commune (acétyl‑CoA) comme donneur. Chez les levures, les plantes et les animaux, huit types principaux de NAT (NatA–NatH) se partagent la tâche. Certaines agissent pendant que la protéine est encore en cours de synthèse, d’autres interviennent après et sont localisées à des sites spécifiques comme l’appareil de Golgi ou les plastides végétaux. Ensemble, elles modifient environ la moitié à quatre‑cinquièmes de toutes les protéines cellulaires, chaque NAT reconnaissant des séquences de départ préférentielles de deux à quatre acides aminés.
Beaucoup d’enzymes, chacune avec sa spécialité
NatA, NatB et NatC sont les principales actrices, agissant directement au ribosome et couvrant de larges portions de « l’acétylome N‑terminal ». NatA seule peut modifier environ 40 % des protéines humaines, en général celles dont la première méthionine a été retirée. NatB et NatC agissent sur des protéines qui conservent leur méthionine initiale, mais diffèrent par les acides aminés voisins qu’elles préfèrent. D’autres NAT sont plus sélectives : NatD cible seulement quelques histones qui emballent l’ADN, NatF vise les protéines transmembranaires au niveau du Golgi, NatG agit à l’intérieur des plastides des plantes, et NatH (NAA80) complète un processus de maturation en deux étapes sur l’actine, un composant majeur du squelette cellulaire. L’article rassemble des études structurales et biochimiques montrant comment des sous‑unités auxiliaires ancrent ces enzymes aux ribosomes ou aux membranes et affinent le choix des protéines ciblées.
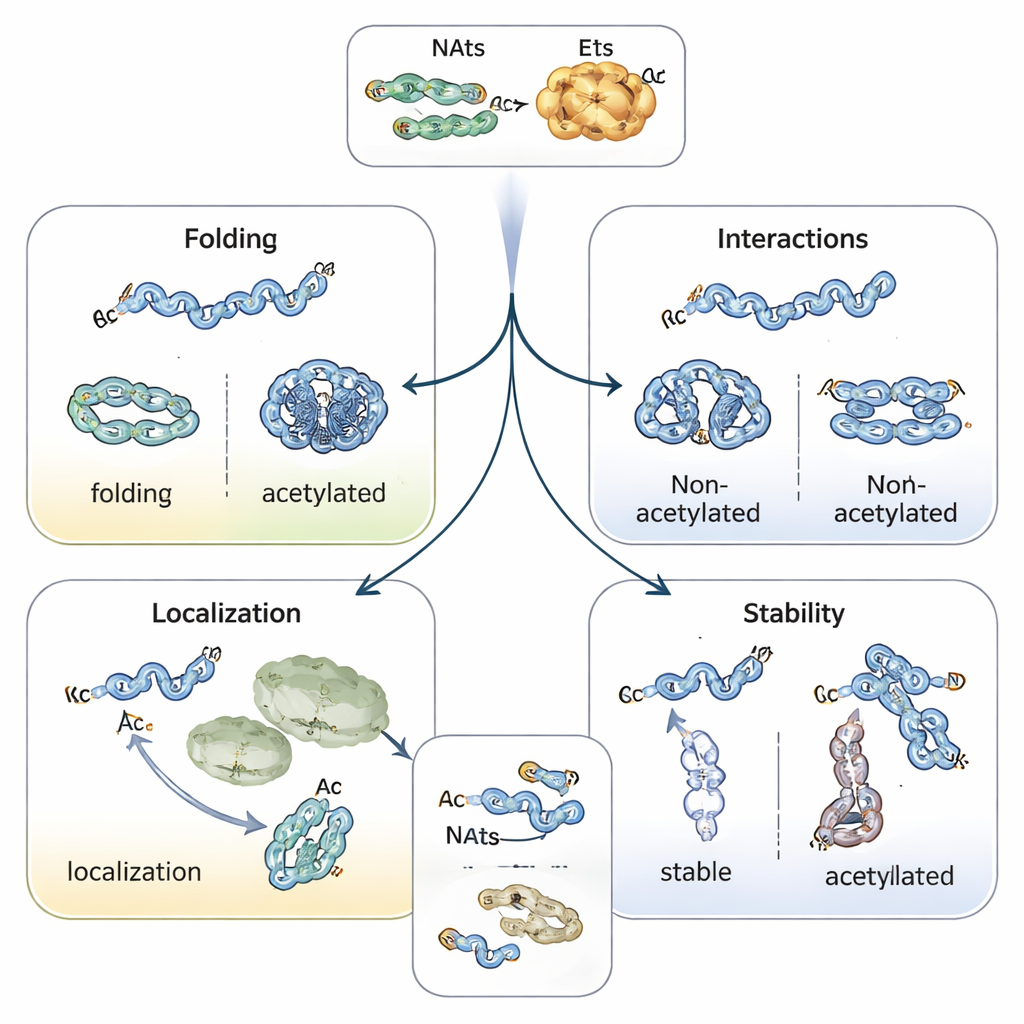
Orienter le repliement, la localisation et la durée de vie des protéines
L’ajout d’un cap acétyle modifie la nature chimique du début de la protéine, stabilisant souvent des structures hélicoïdales et influençant la façon dont les protéines se replient. Par exemple, la protéine liée à la maladie de Parkinson, l’alpha‑synucléine, a tendance à s’agréger moins et à adopter une conformation plus sûre lorsque son N‑terminus est acétylé. La tropomyosine, partenaire de l’actine, se lie et régule beaucoup mieux les filaments d’actine lorsqu’elle est correctement acétylée. Chez les plantes et les animaux, l’acétylation N‑terminale peut servir d’étiquette d’adresse, aidant les protéines à trouver les chloroplastes, les lysosomes ou le Golgi. Peut‑être le plus remarquable est son rôle dans la détermination de la durée de vie des protéines : un N‑terminus non protégé peut être lu comme un « signal de dégradation » par les enzymes d’ubiquitination, tandis que l’acétylation peut masquer ce signal et stabiliser la protéine — ou, dans certains cas, créer une étiquette conditionnelle qui n’est reconnue que lorsque la protéine est mal repliée ou n’est pas dans le bon complexe.
De la physiologie cellulaire au développement et à la maladie
Parce que l’acétylation N‑terminale touche tant de protéines, la perturbation des NAT a des conséquences étendues pour les organismes entiers. La suppression de NatA, NatB ou NatC chez des espèces modèles provoque souvent de graves défauts de développement, des réponses au stress altérées, voire la mort, tandis que des enzymes plus spécialisées comme NatF et NatH entraînent des problèmes plus ciblés tels que des calcifications cérébrales ou une perte auditive. Chez l’humain, des mutations héréditaires dans plusieurs gènes NAT sont à l’origine de syndromes neurodéveloppementaux rares comportant déficience intellectuelle, malformations cardiaques ou faiblesse musculaire. La même machinerie est fréquemment hyperactive dans les cancers, où des niveaux élevés de NAT sont corrélés à un mauvais pronostic et peuvent favoriser la croissance tumorale, les métastases et la résistance aux traitements. Les changements d’acétylation N‑terminale influencent aussi des protéines sujettes à l’agrégation telles que l’alpha‑synucléine et la huntingtine, reliant cette modification aux mécanismes des maladies neurodégénératives.
Perspectives et promesses médicales
Les auteurs concluent que, si nous connaissons aujourd’hui la plupart des enzymes centrales qui ajoutent ces caps N‑terminaux, nous ne comprenons encore qu’une fraction des cibles protéiques spécifiques et des règles de régulation. Un thème majeur est que l’acétylation du début de la protéine la protège souvent d’une destruction prématurée, tout en créant des signaux de contrôle qualité dépendants du contexte. Identifier quelles ligases à ubiquitine lisent quels motifs N‑terminaux, et découvrir si une enzyme peut retirer ces caps, sont des questions ouvertes clés. Parce que les NAT se trouvent au carrefour de la stabilité protéique, de la régulation génique et des réponses au stress cellulaire, des inhibiteurs sélectifs de NAT — et peut‑être à l’avenir des outils modulant l’acétylation N‑terminale de protéines spécifiques liées aux maladies — apparaissent comme des pistes prometteuses pour de nouvelles thérapies contre le cancer, les maladies cardiaques et la neurodégénérescence.
Citation: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Mots-clés: modification des protéines, acétylation N‑terminale, contrôle qualité des protéines, maladie neurodégénérative, biologie du cancer