Clear Sky Science · fr
La méthylation de l’ARN m6A module la réponse antivirale dans la maladie cœliaque
Quand un virus et le gluten font équipe
La maladie cœliaque est souvent perçue comme un problème alimentaire simple : manger du gluten et l’intestin est endommagé. Cette étude révèle une histoire plus profonde, où un type courant de virus intestinal et une petite marque chimique sur nos molécules d’ARN agissent de concert pour pousser le système immunitaire vers des lésions durables. Comprendre cette couche de contrôle cachée peut aider à expliquer pourquoi seules certaines personnes développent la maladie cœliaque et orienter vers de nouveaux traitements qui vont au‑delà du régime sans gluten. 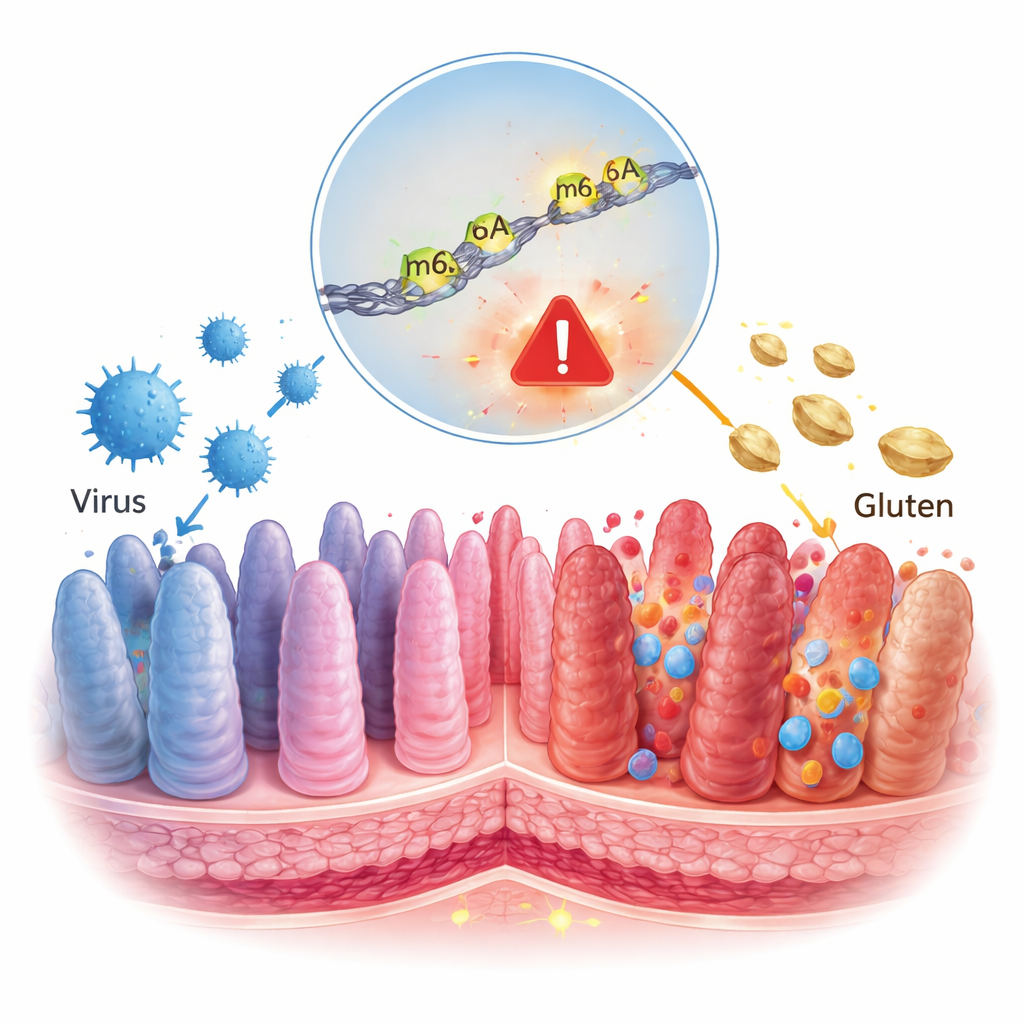
Une marque cachée sur nos messages génétiques
Nos cellules lisent sans cesse les gènes et les recopient en ARN, de courts « messages » qui indiquent à la cellule quelles protéines produire. Ces messages ne sont pas immuables ; ils peuvent être décorés de marques chimiques qui agissent comme des surligneurs, modulant l’intensité de la lecture d’un message. L’une des marques les plus courantes s’appelle m6A, un petit changement sur les lettres de l’ARN. On sait que les virus modifient ces marques d’ARN dans les cellules infectées, et des travaux antérieurs avaient déjà relié la m6A à la façon dont le gluten déclenche l’inflammation dans l’intestin cœliaque. Les auteurs ont cherché à savoir si une modification de la m6A induite par un virus pouvait aider à faire basculer le système immunitaire de la tolérance alimentaire vers l’attaque.
Preuves chez des patients atteints de maladie cœliaque
Les chercheurs ont d’abord examiné le sang et des biopsies intestinales de personnes atteintes de maladie cœliaque active et de témoins non cœliaques. Ils ont constaté que les patients cœliaques présentaient des taux plus élevés d’anticorps dirigés contre le réovirus, un virus à ARN double brin qui infecte l’intestin, suggérant des expositions plus fréquentes ou plus intenses. Dans les tissus intestinaux de ces patients, des gènes d’alerte antivirale clés, en particulier IRF7, étaient exprimés à des niveaux supérieurs, ainsi que des molécules inflammatoires comme STAT1 et le chimiokine attracteur de cellules immunitaires CXCL10. Parallèlement, la machinerie qui ajoute et lit les marques m6A était plus active, et le niveau total de m6A sur l’ARN était plus élevé. L’expression des gènes antiviraux augmentait et diminuait de concert avec les gènes liés à la m6A, laissant entendre que le même système de contrôle pouvait piloter à la fois la défense virale et les dommages auto‑immuns.
Comment le gluten amplifie l’alarme virale
Pour sonder la causalité, l’équipe a construit un modèle cœliaque dans des cellules intestinales cultivées en laboratoire. Ils ont simulé une infection virale en utilisant un ARN double brin synthétique, puis ajouté des fragments de gluten digérés similaires à ce qui apparaîtrait dans l’intestin après un repas. Le leurre viral seul stimulait à la fois IRF3 et IRF7, deux interrupteurs maîtres des réponses antivirales. Mais lorsque le gluten était ajouté, IRF7 montrait une forte poussée supplémentaire, alors qu’IRF3 ne variait pas. Les chercheurs ont découvert que, dans ces conditions, les marques m6A augmentaient sur une région spécifique de l’ARN d’IRF7, et que cet ARN interagissait physiquement avec une enzyme qui écrit la m6A (METTL3) et une enzyme qui l’efface (ALKBH5). Élever la m6A, soit en ajoutant plus de METTL3 soit en réduisant ALKBH5, augmentait encore les niveaux d’IRF7, liant ainsi directement la synergie virus‑plus‑gluten à cette modification d’ARN. 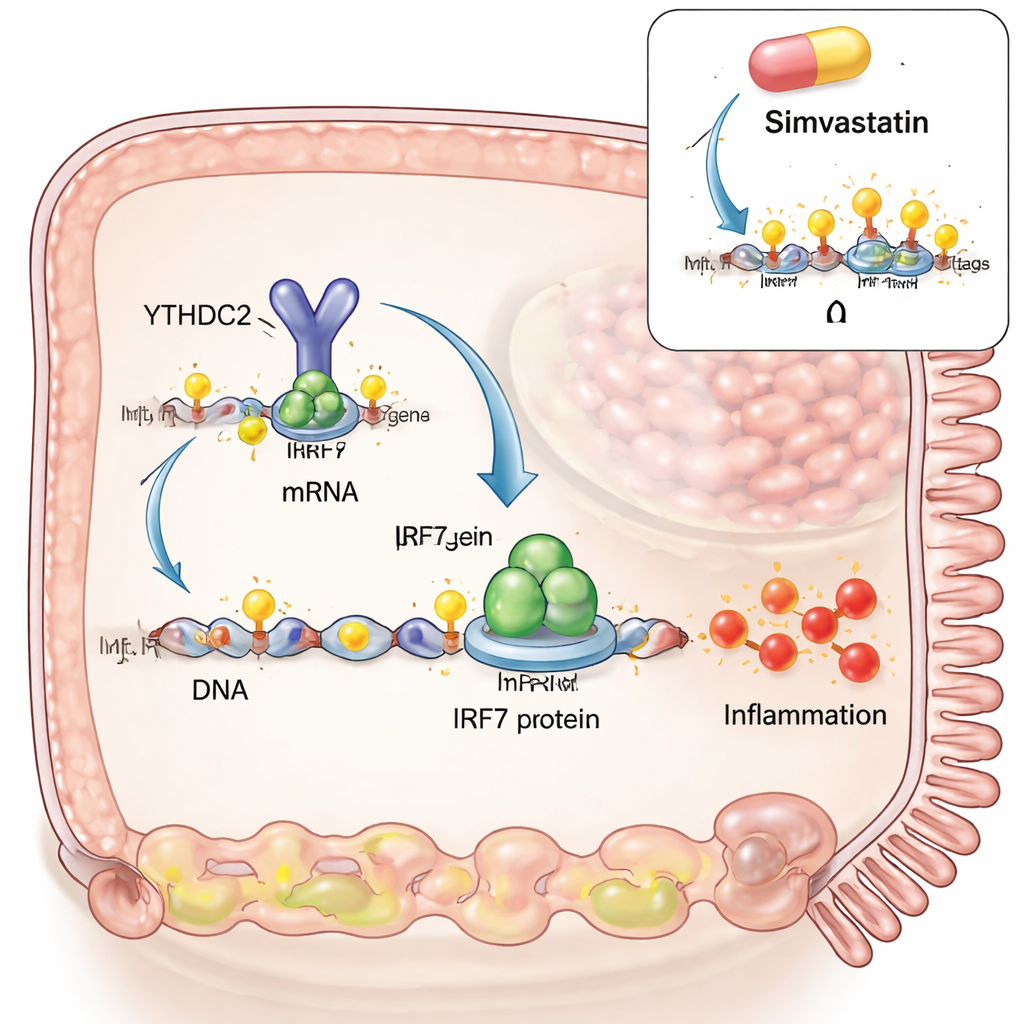
Le médiateur moléculaire et un médicament surprenant
Les auteurs ont ensuite cherché à comprendre comment les marques m6A sur l’ARN d’IRF7 modifient effectivement le comportement cellulaire. Ils ont conçu une version d’ARN d’IRF7 qui code pour la même protéine mais sans les sites m6A. Cet ARN produisait des quantités similaires de transcrit, mais beaucoup moins de protéine IRF7, et il ne parvenait pas à déclencher les gènes inflammatoires en aval comme STAT1 et CXCL10. Le maillon manquant était une protéine liseuse appelée YTHDC2, qui se lie normalement à la m6A dans la région codante et favorise une traduction efficace en protéine. Sans les sites m6A, YTHDC2 ne pouvait plus se fixer à l’ARN d’IRF7. Bloquer l’écrivain m6A METTL3 dans le modèle cellulaire réduisait la protéine IRF7 et CXCL10, diminuant la réponse inflammatoire. Un médicament hypocholestérolémiant, la simvastatine, qui a récemment été montré pour réduire la m6A dans d’autres tissus, a également diminué la m6A sur l’ARN d’IRF7, réduit la protéine IRF7 dans les cellules et atténué les gènes liés à IRF7 dans des biopsies intestinales de patients cœliaques cultivées ex vivo. Des comparaisons à grande échelle de l’expression génétique suggéraient que la simvastatine orientait le tissu cœliaque vers un profil plus proche de celui des patients sous régime sans gluten.
Ce que cela signifie pour les personnes atteintes de maladie cœliaque
Ce travail dresse le tableau d’un virus intestinal et du gluten agissant ensemble sur une couche finement réglée de contrôle de l’ARN. Chez les personnes susceptibles, l’infection virale semble augmenter le marquage m6A de l’ARN d’IRF7 dans les cellules intestinales. L’exposition au gluten amplifie ensuite ce signal marqué, entraînant davantage de protéine IRF7, des alarmes antivirales plus fortes et des niveaux plus élevés de messagers inflammatoires qui contribuent à l’attaque auto‑immune de la muqueuse intestinale. En réduisant les marques m6A — soit génétiquement, soit avec un médicament comme la simvastatine — la réaction en chaîne peut être atténuée, du moins dans des modèles in vitro et ex vivo. Pour le grand public, le message clé est que la maladie cœliaque ne dépend pas seulement de ce que l’on mange, mais aussi de la façon dont les infections et des marques chimiques subtiles sur l’ARN façonnent la décision du système immunitaire de tolérer ou d’attaquer. Cibler ces marques d’ARN pourrait un jour compléter le régime sans gluten et inspirer de nouveaux traitements pour une gamme plus large de maladies auto‑immunes.
Citation: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Mots-clés: maladie cœliaque, méthylation de l’ARN, immunité antivirale, IRF7, simvastatine