Clear Sky Science · fr
CRISPR-AuNP : optimisation physico-chimique d’une plate-forme à nanoparticules d’or pour une édition génique non virale, modulaire et économique dans les CPH
Rendre l’édition génique accessible à davantage de patients
Les outils d’édition génétique comme CRISPR ont déjà transformé la vie de personnes atteintes de maladies sanguines héréditaires, mais les traitements restent coûteux, techniquement exigeants et largement limités à quelques centres spécialisés. Cet article décrit une nouvelle façon d’introduire CRISPR dans les cellules souches hématopoïétiques en utilisant de minuscules particules à base d’or qui peuvent être préparées sur un plan de travail en quelques heures. L’objectif est de rendre ces approches puissantes d’édition génique plus simples, moins chères et plus faciles à déployer dans davantage d’endroits à travers le monde.
Pourquoi les cellules souches sanguines sont importantes
Les cellules souches et progénitrices hématopoïétiques résident dans la moelle osseuse et renouvellent en permanence tous les types de cellules sanguines. Si les médecins peuvent corriger en toute sécurité les mutations responsables de maladies dans ces cellules, un traitement unique pourrait fournir une cure à vie pour des affections telles que la drépanocytose et certaines déficiences immunitaires. Aujourd’hui, la méthode la plus courante pour introduire CRISPR dans ces cellules repose sur l’électroporation, un procédé qui utilise des impulsions électriques pour ouvrir des pores dans les membranes cellulaires. Bien que puissant, l’électroporation est agressive pour les cellules, nécessite des équipements coûteux et des réactifs spécialisés, et n’est pas facilement extensible ni exportable vers des contextes à ressources limitées. Les vecteurs viraux plus sûrs conviennent à de nombreuses thérapies géniques, mais ils sont moins adaptés à la livraison de CRISPR car ils continuent de produire les outils d’édition trop longtemps, augmentant le risque de modifications hors cible.
Construire un véhicule de livraison minuscule en or
Les chercheurs ont cherché à améliorer un système de nanoparticules d’or déjà décrit auparavant, qui portait les composants CRISPR à la surface. Dans les conceptions antérieures, l’ARN guide du système CRISPR était ancré directement sur le noyau d’or puis apparié avec la protéine Cas9. Cela fonctionnait raisonnablement bien pour un type d’enzyme CRISPR, mais donnait de mauvais résultats avec Cas9, au cœur de nombreuses stratégies thérapeutiques. En examinant de près le comportement de Cas9 et de son ARN guide dans les conditions acides utilisées lors de l’assemblage des particules, l’équipe a découvert que le duplex d’ARN guide devenait instable à la surface de l’or, entraînant peu ou pas de Cas9 actif attaché à la particule. La microscopie confocale a aussi suggéré que le revêtement polymère destiné à aider les particules à échapper aux compartiments cellulaires se détachait avant d’avoir pu remplir sa fonction.
Refonte progressive de la plate-forme
Pour surmonter ces problèmes, les scientifiques ont reconstruit le système depuis la base en trois étapes. D’abord, au lieu d’ancrer de l’ARN nu à l’or puis d’ajouter la protéine, ils ont formé des complexes ribonucléoprotéiques CRISPR complets (protéine plus ARN guide) avant de les mettre en contact avec la surface d’or. Ils ont identifié une condition légèrement acide permettant à ces complexes de se lier aux particules tout en maintenant l’activité de la protéine de coupure. Ensuite, ils ont enrobé les particules chargées avec des polymères spécialement conçus combinant des chaînes chargées positivement — nécessaires pour échapper aux compartiments cellulaires — et des segments flexibles et hydrophiles de polyéthylène glycol qui empêchent l’agrégation. En mesurant la taille, la charge de surface et la teneur en protéine, ils ont montré qu’ils pouvaient charger de manière reproductible des dizaines de complexes CRISPR par particule tout en conservant la stabilité en solution.
Percer les défenses cellulaires
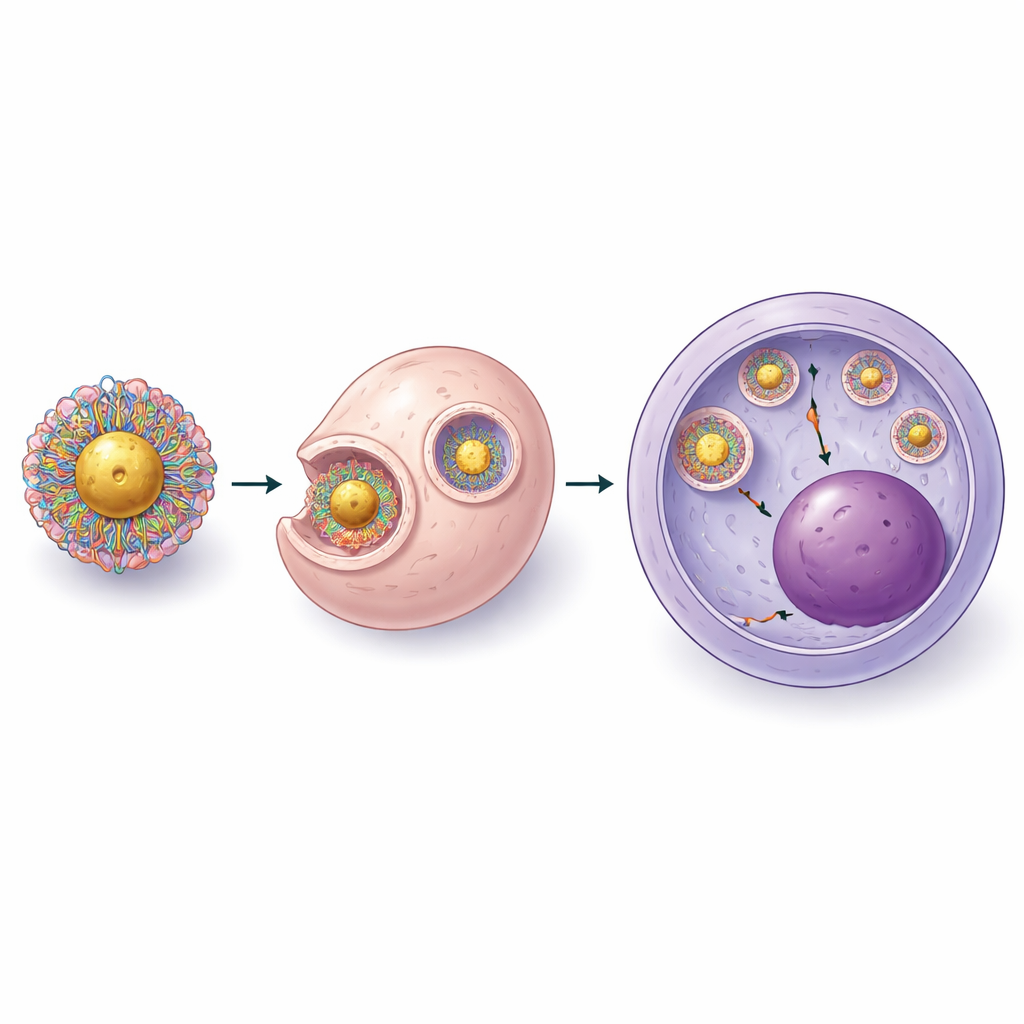
Même avec un meilleur chargement, les particules de deuxième génération restaient confrontées à un obstacle clé : faire sortir CRISPR des vésicules internes de la cellule vers le compartiment où se trouve l’ADN. L’équipe a donc ajusté systématiquement la chimie de la couche polymère et le rapport entre les groupes positifs du polymère et les groupes négatifs du complexe CRISPR. Ils ont découvert que l’ajout de plus courtes chaînes de polyéthylène glycol et d’un nombre maîtrisé d’ancrages contenant du soufre améliorait à la fois la stabilité des particules et la capacité à perturber les membranes endosomales sans nuire aux cellules. Dans la conception finale, de troisième génération, ils ont d’abord créé des complexes compacts de CRISPR et de polymère, puis les ont attachés à des noyaux d’or concentrés. La microscopie électronique a montré une fine coquille de CRISPR et de polymère autour de chaque sphère d’or, et l’imagerie dans des cellules souches vivantes a confirmé que la cargaison pouvait s’échapper vers l’intérieur de la cellule et atteindre le noyau.
Résultats d’édition avec plusieurs outils CRISPR
Pour tester l’efficacité des particules optimisées, les chercheurs ont ciblé un gène appelé bêta-2-microglobuline, qui produit une protéine présente à la surface de presque toutes les cellules sanguines et facilement mesurable par cytométrie en flux. En utilisant leur plate-forme or de troisième génération, ils ont obtenu plus de 10 % de perturbations précises de ce gène dans des cellules souches et progénitrices sanguines humaines primaires — des niveaux considérés comme significatifs pour de nombreuses applications thérapeutiques — tout en maintenant une forte survie cellulaire. Bien que cette efficacité soit inférieure à celle atteignable par électroporation, le système à base d’or ne nécessitait aucun équipement spécialisé et provoquait un stress minimal sur les cellules. Fait important, la même plate-forme pouvait être utilisée avec différentes protéines CRISPR, y compris Cas9, Cas12a et une enzyme plus récente appelée Cas12a-M29-1, avec des niveaux d’édition similaires et aucune toxicité détectable, soulignant le caractère modulaire de la conception.
Ce que cela pourrait signifier pour les thérapies futures
En termes simples, ce travail montre qu’il est possible de construire un transporteur minuscule et soigneusement conçu à base d’or capable d’introduire les outils CRISPR dans des cellules souches sanguines sensibles sans électricité ni virus, en utilisant des matériaux disponibles dans le commerce pour moins de soixante-dix dollars par million de cellules. Bien que des améliorations supplémentaires soient nécessaires pour égaler l’efficacité des meilleures méthodes cliniques actuelles, en particulier pour les maladies exigeant des niveaux très élevés de cellules corrigées, cette plate-forme assemblée au banc réduit les obstacles pratiques à la réalisation d’éditions géniques sophistiquées. Avec des raffinements et des tests de sécurité supplémentaires, de telles nanoparticules pourraient aider à étendre les bénéfices des thérapies basées sur CRISPR au-delà des centres spécialisés, rendant les traitements curatifs plus accessibles aux patients du monde entier.
Citation: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Mots-clés: édition génétique CRISPR, nanoparticules d’or, cellules souches hématopoïétiques, livraison non virale, nanomédecine