Clear Sky Science · fr
Repenser la génomique de la dystrophie musculaire facioscapulohumérale à l’ère du télomère-au-télomère : écueils dans le paysage caché des répétitions D4Z4
Pourquoi cette histoire de maladie musculaire compte
La dystrophie musculaire facioscapulohumérale (FSHD) est l’une des maladies héréditaires de perte musculaire les plus fréquentes, affaiblissant souvent les muscles du visage et des épaules chez des adultes jeunes par ailleurs en bonne santé. Pendant des années, les chercheurs ont ciblé un segment d’ADN unique proche de l’extrémité du chromosome 4 comme responsable. Cette nouvelle étude montre que la réalité est bien plus complexe : des répétitions d’ADN similaires sont disséminées dans tout le génome, et de nombreux tests de laboratoire standards ne peuvent pas les distinguer. Comprendre ce paysage caché est essentiel pour un diagnostic précis, une recherche de meilleure qualité et, à terme, des thérapies plus sûres.
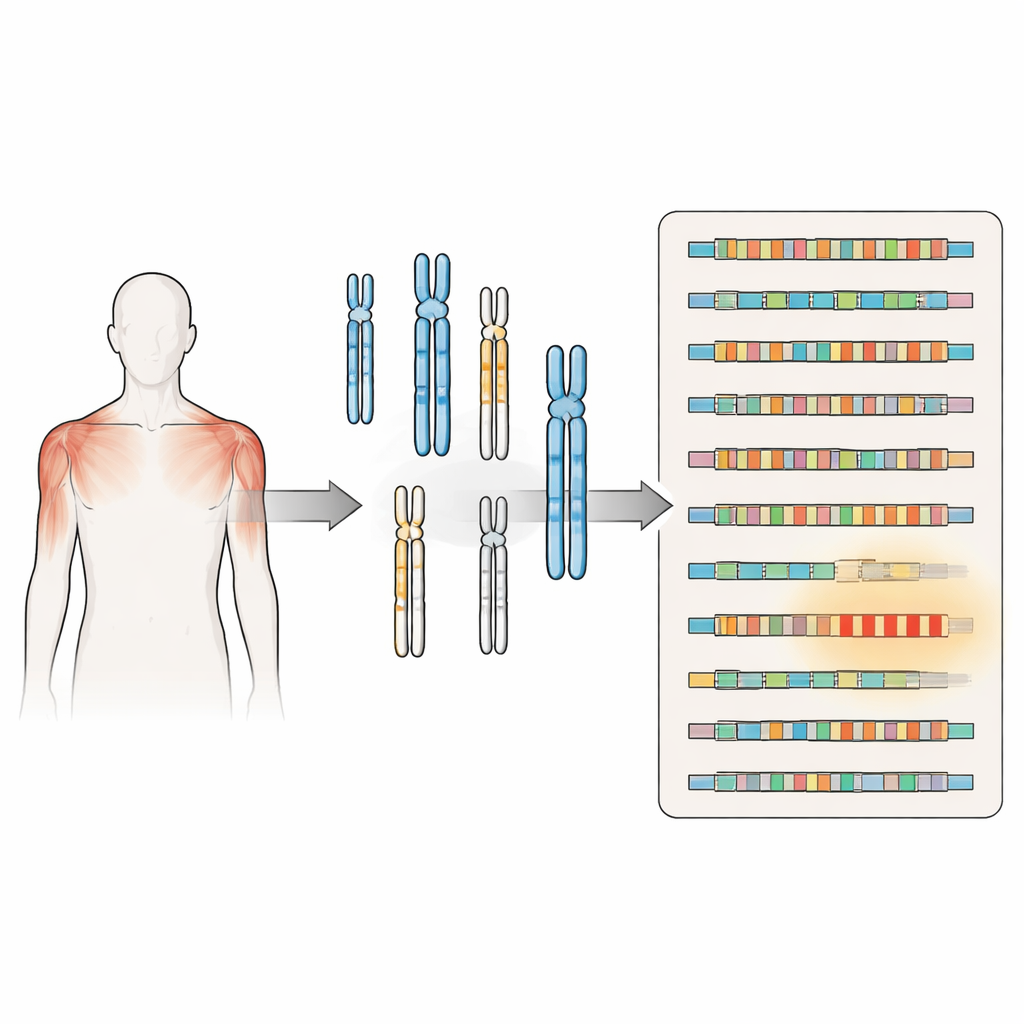
Un examen plus attentif d’un trouble musculaire énigmatique
La FSHD a longtemps été associée au raccourcissement d’une séquence répétée d’ADN appelée D4Z4 près de l’extrémité du chromosome 4. Lorsque cette région de répétitions se réduit au‑dessous d’une certaine taille et se trouve sur un contexte génétique particulier, elle permet la production d’une protéine nommée DUX4, capable d’endommager les cellules musculaires. Une seconde forme de la maladie survient lorsque des gènes qui maintiennent normalement cette région fortement compactée et silencieuse sont mutés, ce qui autorise là encore l’apparition de DUX4. Ces deux mécanismes convergent vers le même problème : un gène qui devrait être essentiellement inactif dans le muscle adulte devient sporadiquement actif, contribuant à la faiblesse et à l’atrophie musculaires.
Répétitions cachées dans tout le génome
Les premières cartes du génome humain étaient incomplètes, en particulier dans les régions riches en séquences répétitives aux extrémités chromosomiques et près des centromères. En utilisant la nouvelle assemblée du génome humain télomère‑au‑télomère, qui comble ces lacunes, les auteurs ont rescanné l’ensemble du génome en prenant la séquence D4Z4 du chromosome 4 comme modèle de recherche. Ils ont découvert des grappes et des copies isolées de répétitions de type D4Z4 sur au moins dix chromosomes supplémentaires. Certaines de ces répétitions sont structurellement complètes et se situent à proximité de signaux susceptibles de stabiliser des ARN de type DUX4, laissant penser qu’elles pourraient produire des protéines ou des molécules d’ARN apparentées dans des conditions appropriées.
Quand les tests de laboratoire voient plusieurs lieux à la fois
La recherche et le diagnostic de la FSHD reposent souvent sur des tests qui amplifient des fragments d’ADN ou d’ARN spécifiques à l’aide de courtes amorces, une stratégie connue sous le nom de PCR. Ces amorces ont été initialement conçues sous l’hypothèse que les répétitions D4Z4 n’existaient que sur les chromosomes 4 et 10. En combinant prédictions informatiques et expériences sur des cellules portant des chromosomes humains isolés, les auteurs montrent que de nombreux jeux d’amorces largement utilisés se lient non seulement à la région liée à la maladie sur le chromosome 4, mais aussi à des répétitions analogues disséminées dans le génome. Les amorces ciblant l’exon principal de DUX4 ou des ARN non codants voisins amplifient fréquemment des produits provenant de plusieurs chromosomes à la fois, rendant impossible de savoir où un signal donné a réellement pour origine.
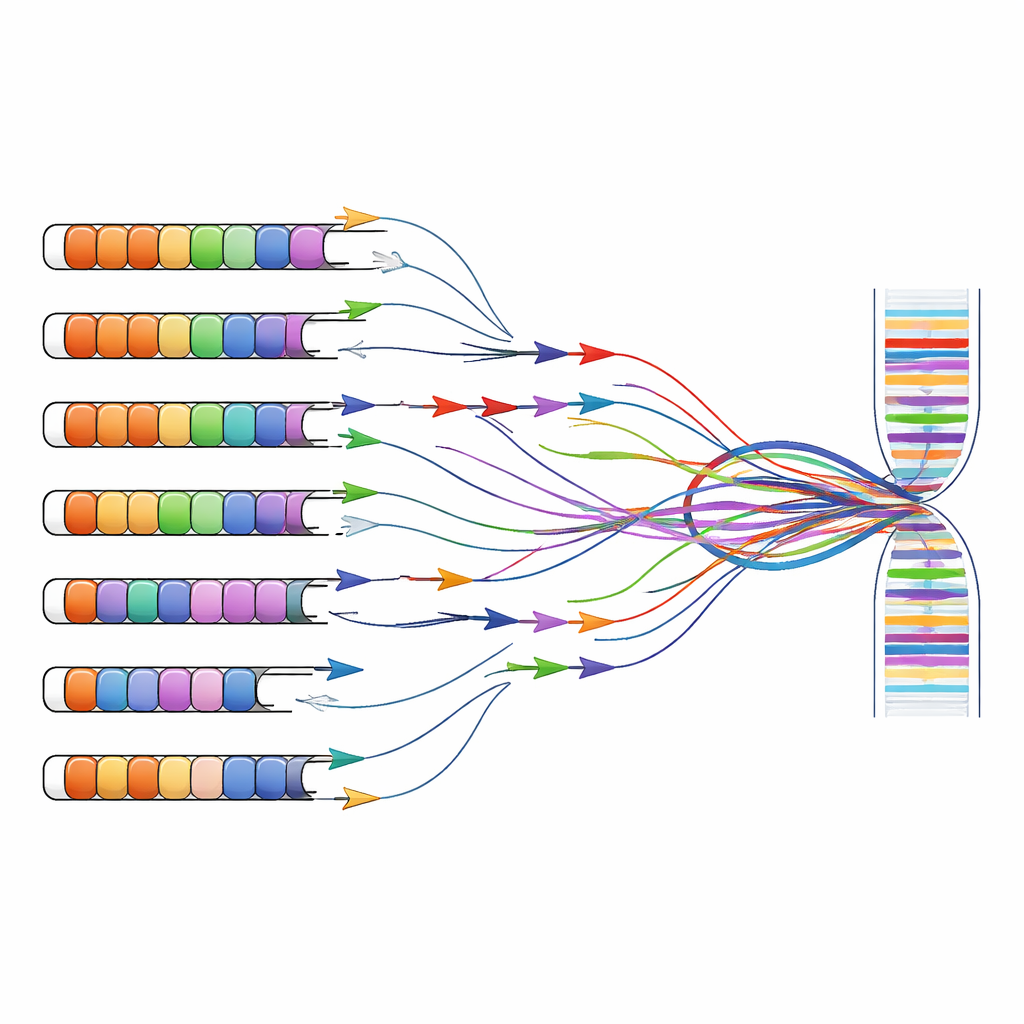
Repenser les outils diagnostiques et de recherche
Ce problème de multi‑localisation dépasse la recherche fondamentale et touche la clinique. Les tests plus récents qui mesurent la méthylation de l’ADN (une marque chimique associée au silence génique) ou qui utilisent le séquençage à lectures courtes agrègent souvent les signaux de nombreuses répétitions presque identiques. En conséquence, les mesures de la « méthylation D4Z4 » ou des « transcrits DUX4 » dans les ensembles de données publics peuvent en réalité refléter un mélange de contributions du chromosome 4, du chromosome 10 et d’autres sites. Les auteurs soutiennent que, pour relier correctement les altérations génétiques aux symptômes, les chercheurs doivent désormais adopter des méthodes conscientes des répétitions qui distinguent les loci individuels — par exemple le séquençage long‑read capable de couvrir des blocs de répétitions entiers et de capturer leurs profils de méthylation et leurs produits ARN dans leur intégralité.
Ce que cela signifie pour les patients et les thérapies futures
L’étude ne remet pas en cause le rôle central de la région D4Z4 raccourcie sur le chromosome 4 dans la FSHD, mais elle montre que cette région vit dans un voisinage encombré de séquences similaires. Des signaux autrefois supposés prouver l’activité au locus de la maladie peuvent en fait provenir en partie de ses cousins génomiques. Pour les patients, cela signifie que les outils diagnostiques les plus fiables seront ceux qui résolvent physiquement le chromosome exact et le bloc de répétitions impliqué, plutôt que de s’appuyer uniquement sur des mesures indirectes. Pour les chercheurs et les développeurs de médicaments, cela souligne la nécessité de conceptions hautement spécifiques qui évitent de cibler par erreur des répétitions inoffensives ailleurs dans le génome. À l’ère du télomère‑au‑télomère, comprendre et traiter la FSHD dépendra de la visualisation complète du paysage des répétitions, et non d’un seul repère.
Citation: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Mots-clés: dystrophie musculaire facioscapulohumérale, répétitions D4Z4, DUX4, génome télomère-au-télomère, diagnostic génétique