Clear Sky Science · fr
Chaperons artificiels : des conceptions conventionnelles aux systèmes intelligents
Aider les molécules à se replier correctement
À l’intérieur de chaque cellule vivante, de longues chaînes de protéines et de matériel génétique doivent se plier et se tordre en formes précisément adaptées pour fonctionner. Lorsqu’elles se replient mal, elles peuvent s’agglomérer, perdre leur fonction et même déclencher des maladies, comme des pathologies neurodégénératives. La nature s’appuie sur des molécules « chaperonnes » pour maintenir cet ordre microscopique, mais ces aides naturelles sont coûteuses, fragiles et difficiles à utiliser en dehors des cellules. Cet article explore la manière dont les scientifiques conçoivent aujourd’hui des chaperons artificiels — des assistants conçus pouvant ramener des molécules égarées à leur forme et même être activés ou désactivés comme des outils intelligents.
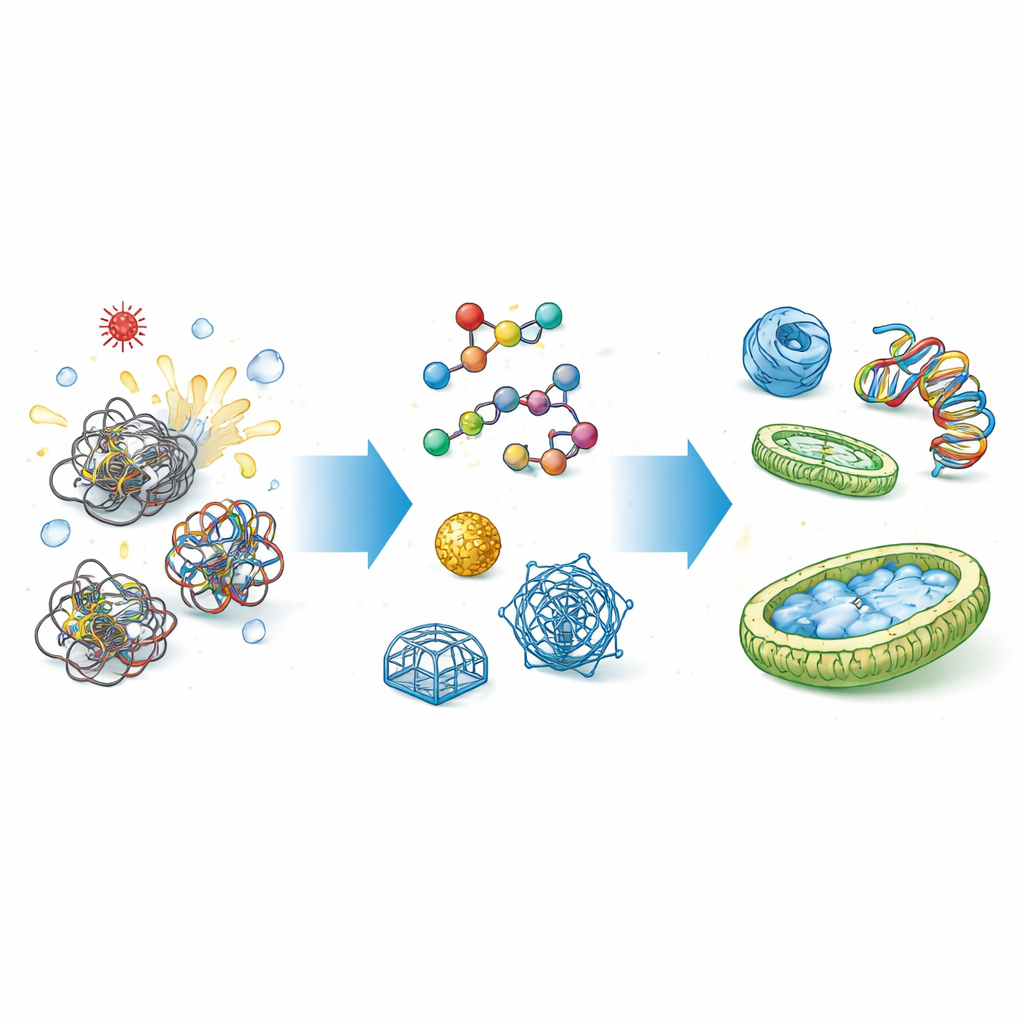
Pourquoi les cellules ont besoin d’aides au repliement
Les protéines et les acides nucléiques (comme l’ADN et l’ARN) ne naissent pas prêts à l’emploi ; ils doivent se replier en structures tridimensionnelles complexes. Le chemin vers ces formes est semé d’embûches, où les chaînes peuvent se coincer ou se coller entre elles. Les chaperons naturels, tels que les protéines de choc thermique, saisissent ces chaînes molles, protègent leurs zones adhésives et leur offrent un espace abrité pour se replier correctement. Des rôles de guidage similaires existent pour les acides nucléiques, où des chaperons aident à défaire les nœuds et à réarranger les appariements de bases. Quand ce contrôle fait défaut, le résultat peut être une perte de fonction, des agrégats toxiques, des maladies et des échecs coûteux dans la production industrielle de protéines.
Des produits chimiques simples aux polymères sur mesure
Les premiers chaperons artificiels étaient des produits chimiques relativement simples modifiant l’environnement perçu par les molécules. Certains solvants et détergents peuvent masquer des régions adhésives des protéines, prévenir les agrégations et leur donner une seconde chance de se replier correctement. Quelques petits acides gras, par exemple, aident le collagène muté à adopter une conformation plus correcte et soulagent le stress à l’intérieur de cellules atteintes de maladies héréditaires. Mais ces aides chimiques doivent généralement être ajoutées à fortes doses, sont difficiles à ajuster pour des cibles spécifiques et peuvent perturber d’autres composants dans des mélanges complexes. Pour gagner en contrôle, les chercheurs se sont tournés vers des polymères plus volumineux et sur mesure — des chaînes flexibles pouvant être décorées de branches chargées ou hydrophiles pour envelopper l’ADN, l’ARN et les protéines de façon plus sélective.
Boîte à outils : polymères et nanogels
Les polymères conçus peuvent se lier aux squelettes chargés de l’ADN ou aux zones exposées des protéines, aplanissant le paysage énergétique pour que ces molécules trouvent leurs formes préférées plus rapidement et de manière plus fiable. Pour les acides nucléiques, des polymères cationiques (chargés positivement) peuvent neutraliser la répulsion entre brins, accélérant l’appariement des bases, l’échange de brins et la formation de structures exotiques utilisées en calcul ADN et en biocapteurs. Pour les protéines, des polymères tels que des boucles de polyéthylène glycol spécialement façonnées ou des polyanions synthétiques peuvent surpasser certains chaperons naturels pour prévenir l’agrégation induite par la chaleur. D’autres systèmes associent des polymères chaperons flexibles à de courts peptides pour remodeler des membranes de type cellulaire en feuillets nanométriques plats ou en vésicules, créant des plateformes bidimensionnelles réversibles pour le transport de charges et l’ingénierie tissulaire.

Concevoir des chaperons intelligents et commutables
Au‑delà du simple maintien et relâchement de leurs clients, les chaperons artificiels modernes peuvent désormais répondre à leur environnement. Des nanogels, nanoparticules et réseaux polymériques ont été développés dont l’emprise sur les protéines se resserre ou se relâche en fonction de l’acidité, de la température, de la lumière ou de produits chimiques spécifiques comme le glucose. Par exemple, certaines micelles deviennent plus hydrophobes à un pH légèrement acide, imitant les chaperons naturels en capturant des protéines menacées puis en les relâchant quand le pH redevient favorable. Des polymères thermoréactifs se contractent ou se dilatent lorsqu’ils franchissent un seuil, leur permettant de séquestrer des protéines endommagées à une température et de libérer celles qui se sont refoldées à une autre. Des groupes photosensibles peuvent servir d’interrupteurs moléculaires, activant ou désactivant des voies d’assemblage d’ADN par une impulsion lumineuse, tandis que des particules sensibles au sucre peuvent protéger une hormone thérapeutique puis la libérer préférentiellement lorsque la glycémie est élevée.
Ce que cela implique pour la médecine et la technologie
L’article conclut que les chaperons artificiels évoluent de simples stabilisants chimiques vers des « outils moléculaires » hautement programmables capables de reconnaître, protéger et remodeler divers types de structures biologiques à la demande. En équilibrant soigneusement forces attractives et répulsives, et en intégrant une sensibilité à des signaux tels que le pH, la chaleur, la lumière ou le stress mécanique, ces systèmes peuvent plier les molécules cibles au bon endroit et au bon moment. À long terme, ces aides intelligentes pourraient rendre la production industrielle de protéines plus efficace, affiner les biocapteurs, alimenter des ordinateurs moléculaires et offrir de nouvelles approches pour traiter des maladies liées aux protéines mal repliées — potentiellement y compris des affections comme la maladie d’Alzheimer — tout en imitant de près le contrôle subtil que les cellules vivantes exercent déjà.
Citation: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Mots-clés: chaperons artificiels, repliement des protéines, polymères intelligents, nanomédecine, matériaux sensibles aux stimuli