Clear Sky Science · fr
Le virus oncolytique M1 réveille l’immunité des cellules T CD8+ contre le glioblastome via la présentation croisée d’antigènes dépendante des cellules B dans la rate
Rallumer le système immunitaire
Le glioblastome est l’un des cancers cérébraux les plus mortels, en partie parce qu’il est remarquablement efficace pour désactiver les défenses de l’organisme. Cette étude explore une nouvelle manière de réactiver ces défenses à l’aide d’un virus spécialement conçu, administré par voie intraveineuse, qui attaque à la fois les cellules tumorales et mobilise les cellules immunitaires contre le cancer. Le travail révèle un intervenant inattendu dans cette réponse : des cellules immunitaires de la rate qui contribuent à réveiller les cellules T tueuses du tumor.
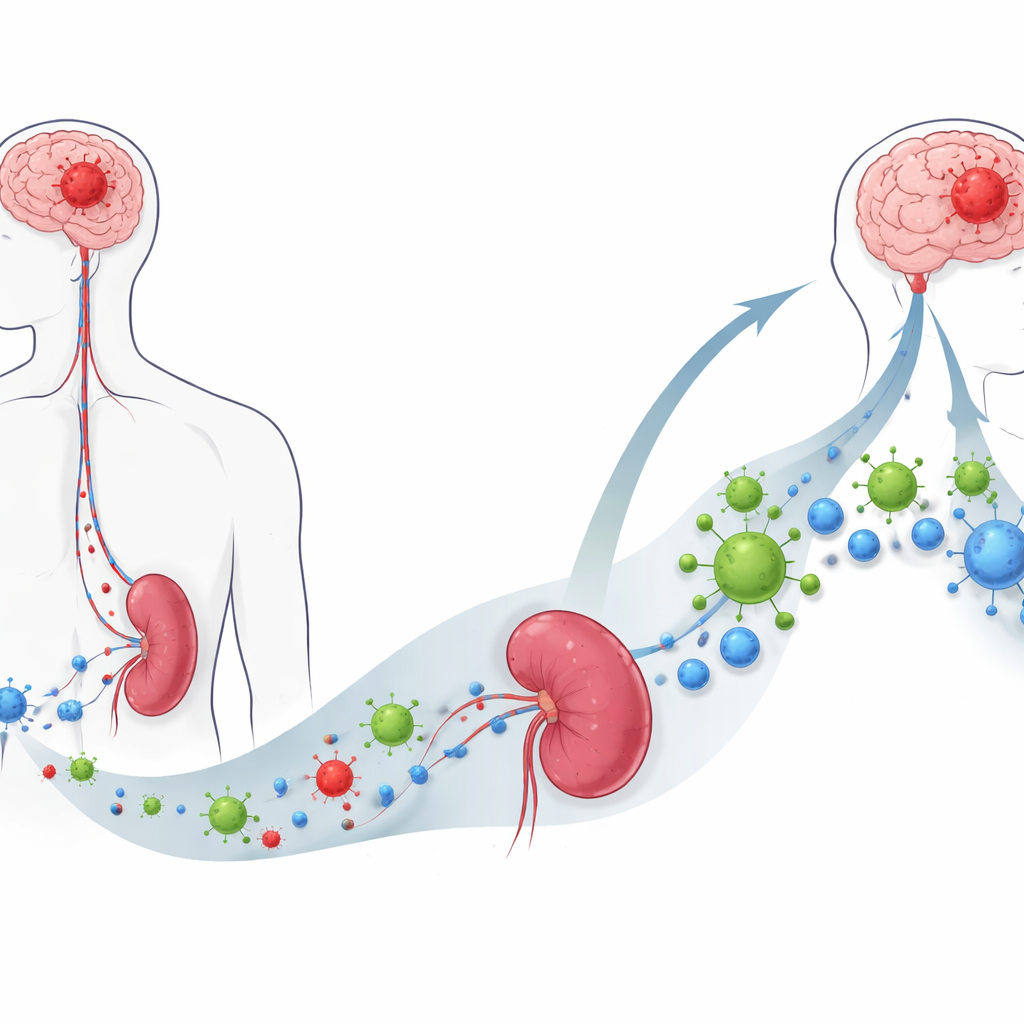
Un virus qui préfère les cellules cancéreuses
Les chercheurs ont étudié une thérapie expérimentale appelée virus oncolytique M1, ou OVM, un alphavirus modifié qui préfère infecter et tuer les cellules cancéreuses tout en épargnant les tissus normaux. En cultures cellulaires, l’OVM a efficacement envahi diverses lignées de glioblastome de souris et d’humain et les a poussées vers une forme de mort cellulaire qui laisse des « signaux de danger » moléculaires. Testé sur des fragments tumoraux humains fraîchement prélevés, l’OVM s’est répliqué fortement dans le tissu de glioblastome mais pas dans les échantillons cérébraux non cancéreux voisins, ce qui suggère qu’il peut mieux distinguer cellules malignes et saines que la chimiothérapie standard, qui endommageait les deux.
Renverser l’effondrement immunitaire systémique
Au-delà du cerveau, le glioblastome provoque un effondrement immunitaire généralisé : les patients et les modèles murins présentent des rates atrophiées et une forte perte de cellules T circulantes. Après un traitement intraveineux par OVM chez des souris porteuses de tumeurs, ce tableau a changé radicalement. Les rates ont repris du volume, les taux sanguins de cellules T CD4 et CD8 ont rebondi et des molécules immunosuppressives telles que l’IL-10 et le TGF-bêta ont diminué. Au site tumoral, davantage de cellules T — en particulier les cellules T CD8 « tueuses » reconnaissant un antigène tumoral modèle — ont infiltré le cerveau, transformant un microenvironnement tumoral auparavant « froid » en un lieu rempli de combattants immunitaires.
Pourquoi la rate est importante
De manière surprenante, la rate s’est avérée essentielle au succès de l’OVM. Lorsque la rate a été retirée chirurgicalement, le virus n’a plus ralenti la croissance tumorale ni prolongé la survie, et la poussée de cellules T dans le sang et le cerveau a en grande partie disparu. Le séquençage unicellulaire de l’ARN des cellules immunitaires spléniques a montré qu’après traitement par OVM, les cellules B de la rate formaient des réseaux de communication particulièrement intenses avec les cellules T. En culture, les cellules B issues de souris traitées par OVM faisaient proliférer et activer les cellules T CD8 beaucoup plus efficacement que les cellules B d’animaux non traités, tandis que les cellules dendritiques ne présentaient pas cet effet, ce qui désigne les cellules B comme des intermédiaires clés.
Des cellules B particulières qui amorcent les tueuses tumorales
En approfondissant, l’équipe a découvert un sous-groupe distinct de cellules B marqué par une molécule de surface nommée Bst2, qui s’est développé dans la rate après traitement par OVM. Ces cellules B Bst2-positives étaient enrichies en gènes impliqués dans la capture de matériel tumoral, son traitement intracellulaire et la présentation de fragments à la surface d’une manière que les cellules T CD8 peuvent « voir ». Les expériences ont montré que ces cellules capturaient les antigènes tumoraux plus efficacement, formaient des zones de contact étroites avec les cellules T CD8 et nécessitaient un contact cellulaire direct ainsi qu’une voie spécifique de traitement des protéines pour activer les T. Lorsque des cellules B Bst2-positives purifiées ont été transférées dans des souris déficientes en cellules B porteuses de tumeurs cérébrales, elles ont significativement prolongé la survie, alors que d’autres types de cellules B ne l’ont pas fait.
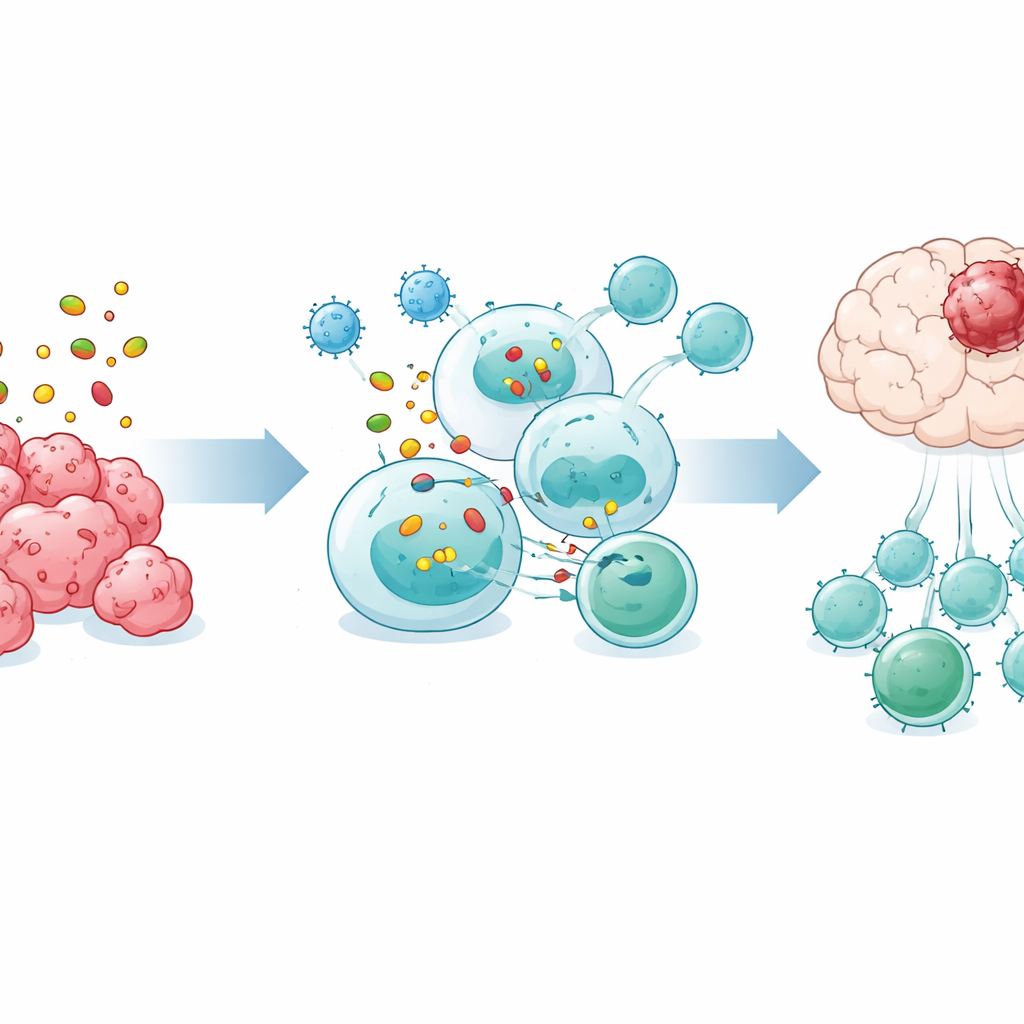
Renforcer l’efficacité de la thérapie par inhibition des points de contrôle
Les immunothérapies actuelles les plus prometteuses — les inhibiteurs de points de contrôle bloquant PD-1 ou PD-L1 — ont donné des résultats décevants dans le glioblastome. Dans les modèles murins utilisés ici, les anticorps anti–PD-1 ou anti–PD-L1 seuls ont eu peu d’effet. Cependant, la combinaison de l’OVM avec un anticorps bloquant PD-1 a considérablement augmenté le nombre de cellules T CD8 dans les tumeurs cérébrales, a fait passer les cellules T circulantes d’un état naïf à un état activé, a restauré la taille de la rate et a prolongé la survie. Le traitement par OVM a aussi augmenté l’expression de PD-1 sur les cellules T CD8 infiltrant la tumeur, les rendant plus susceptibles d’être restaurées par le blocage de PD-1.
Ce que cela pourrait signifier pour les patients
Pris ensemble, ces résultats suggèrent qu’un virus oncolytique administré par voie intraveineuse peut faire plus que simplement infecter et lyser les cellules de glioblastome. En recrutant un groupe spécialisé de cellules B dans la rate pour traiter le matériel tumoral et le présenter aux cellules T CD8, l’OVM reconstruit l’immunité systémique et ramène des cellules T tueuses dans le cerveau pour attaquer la tumeur. Dans des modèles précliniques, cette stratégie non seulement supprime la croissance tumorale seule, mais rend aussi les tumeurs cérébrales résistantes réceptives à la thérapie anti–PD-1. Si ces observations se confirment chez l’humain, l’OVM et les cellules B Bst2-positives pourraient constituer l’épine dorsale de nouvelles associations thérapeutiques — voire de vaccins personnalisés — qui donneraient enfin au système immunitaire une réelle chance contre le glioblastome.
Citation: Han, Y., Guo, C., Chen, C. et al. Oncolytic virus M1 reinvigorates CD8+ T-cell immunity against glioblastoma through B-cell-dependent antigen cross-presentation in the spleen. Cell Mol Immunol 23, 349–366 (2026). https://doi.org/10.1038/s41423-026-01396-w
Mots-clés: glioblastome, virus oncolytique, immunologie tumorale, cellules B, thérapie par inhibition des points de contrôle immunitaire