Clear Sky Science · fr
Aborder la cuproptose : du réarrangement métabolique à l’exploitation thérapeutique en cancérologie
Quand un métal utile se retourne contre le cancer
Le cuivre est surtout connu comme composant des fils électriques et de la plomberie, mais il circule aussi discrètement dans nos cellules, aidant les enzymes à produire de l’énergie et à nous protéger des dommages. Cet article de synthèse explore une tournure surprenante : dans certaines conditions, un excès de cuivre peut pousser les cellules cancéreuses vers une forme particulière de mort. Comprendre ce processus — appelé « cuproptose » — pourrait ouvrir de nouvelles voies pour traiter des tumeurs ayant échappé aux thérapies standard.
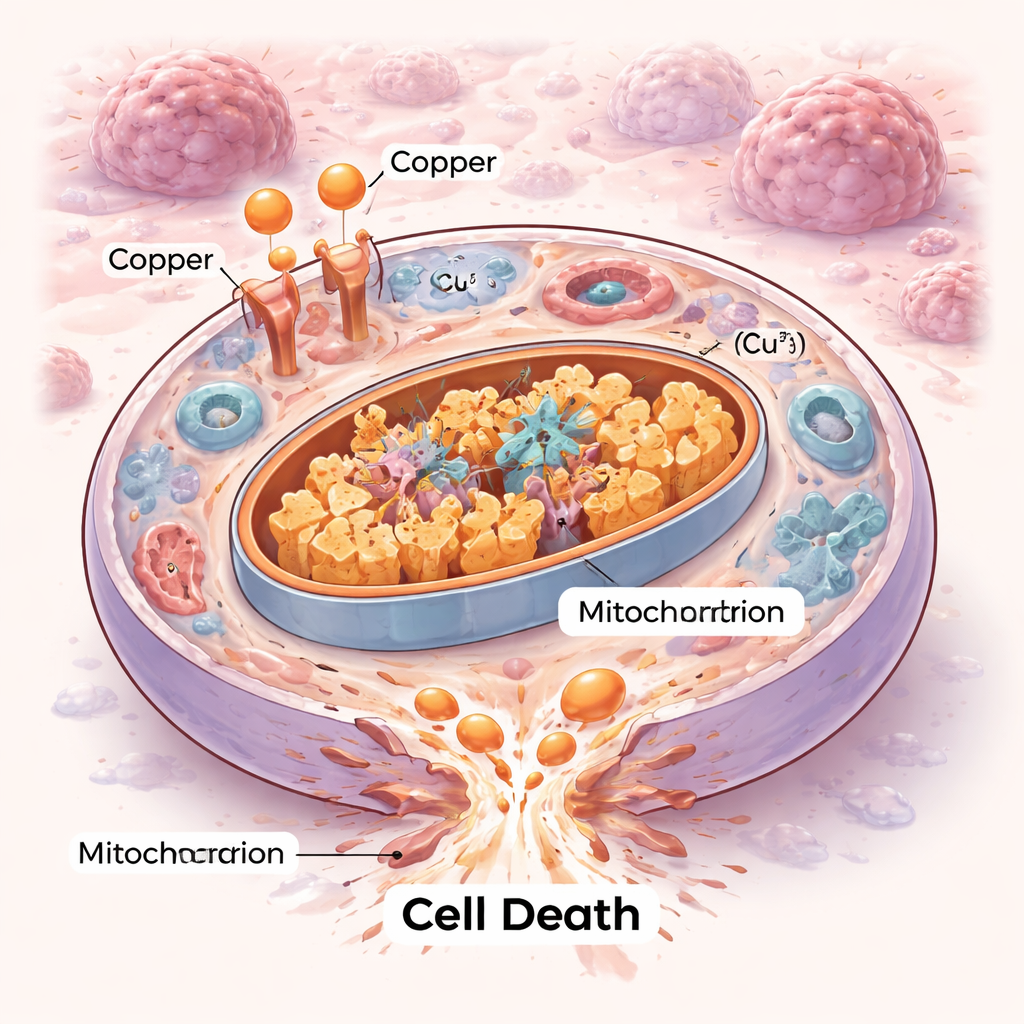
Une nouvelle façon dont les cellules peuvent mourir
Les cellules ne meurent pas toutes de la même manière. Pendant des décennies, les chercheurs ont cartographié des programmes d’autodestruction ordonnés comme l’apoptose, puis des formes plus récentes comme la ferroptose. La cuproptose apporte un nouveau chapitre. Ici, un excès de cuivre inonde les centrales énergétiques de la cellule — les mitochondries — et se lie à des enzymes métaboliques spécifiques qui participent normalement à la combustion du carburant. Cette liaison provoque l’agrégation de ces enzymes et déstabilise de petits composants fer‑soufre dont les mitochondries ont besoin pour fonctionner. Le résultat est une sorte d’embouteillage interne et de panne mécanique que la cellule ne peut pas réparer, aboutissant à une mort par stress protéotoxique plutôt que par les voies suicidaires classiques.
Comment les cellules cancéreuses contrôlent le cuivre et l’énergie
Parce que le cuivre est à la fois essentiel et dangereux, les cellules entretiennent un réseau logistique élaboré pour le déplacer en sécurité. Des transporteurs dédiés font entrer le cuivre dans la cellule, des protéines chaperonnes l’escortent vers les mitochondries et d’autres destinations, et des molécules de stockage comme les métallothionéines et le glutathion neutralisent tout excès. Les tumeurs réorganisent souvent ce système. Certaines augmentent les importateurs ou les chaperonnes pour alimenter leurs forts besoins énergétiques ; d’autres rehaussent les exportateurs ou les protéines de stockage pour éviter une surcharge en cuivre. Parallèlement, de nombreux cancers modifient leur métabolisme — basculant entre la glycolyse en surface et une respiration mitochondriale plus profonde. La revue explique que la cuproptose frappe surtout les cellules qui dépendent encore fortement des mitochondries, rendant les tumeurs présentant ce profil métabolique particulièrement vulnérables.
Commutateurs maîtres qui règlent la sensibilité au cuivre
De grands « décideurs » cellulaires influencent la survenue de la cuproptose. Le suppresseur de tumeur p53, par exemple, tend à éloigner les cellules d’une fermentation rapide du glucose vers un usage mitochondrial du carburant plus ordonné. Ce faisant, et en modifiant la gestion des enzymes liant le cuivre, p53 peut rendre les cancers plus sensibles à la mort induite par le cuivre — tandis que les formes mutantes de p53 font souvent l’inverse. En revanche, le facteur d’hypoxie HIF‑1α, activé au cœur des tumeurs faiblement oxygénées, aide les cellules à échapper à la cuproptose en abaissant l’expression de certaines enzymes mitochondriales et en renforçant des boucliers liant le cuivre. D’autres voies, comme Wnt/β‑caténine et AKT, favorisent la résistance en stimulant l’export du cuivre ou en modifiant chimiquement des protéines cruciales pour qu’elles ne répondent plus à une surcharge cuivrique. Ensemble, ces réseaux agissent comme des thermostats, augmentant ou diminuant la sensibilité d’une tumeur aux traitements à base de cuivre.
Le cuivre, le système immunitaire et une administration de médicaments plus intelligente
Le rôle du cuivre ne se limite pas à tuer directement les cellules cancéreuses ; il façonne aussi le paysage immunitaire qui entoure les tumeurs. Un stress cuivrique contrôlé peut rendre les cellules cancéreuses mourantes plus « visibles », libérant des signaux de danger qui recrutent et activent les lymphocytes T, les cellules dendritiques et les macrophages. Le cuivre peut également influencer les niveaux de points de contrôle immunitaire comme le PD‑L1, que les tumeurs utilisent pour désactiver les lymphocytes T anticancéreux, offrant ainsi des opportunités de combiner des médicaments ciblant le cuivre avec des immunothérapies modernes. Parce que le cuivre libre peut nuire aux tissus sains, les chercheurs développent des outils de précision : des ionophores de petite taille qui chaperonnent le cuivre sélectivement dans les cellules cancéreuses, et des plates‑formes de nanomédecine qui encapsulent du cuivre ou des médicaments activés par le cuivre dans des particules ciblées ou des hydrogels. Ces technologies visent à élever le cuivre à des niveaux létaux à l’intérieur des tumeurs tout en maintenant le reste de l’organisme dans une zone sûre.
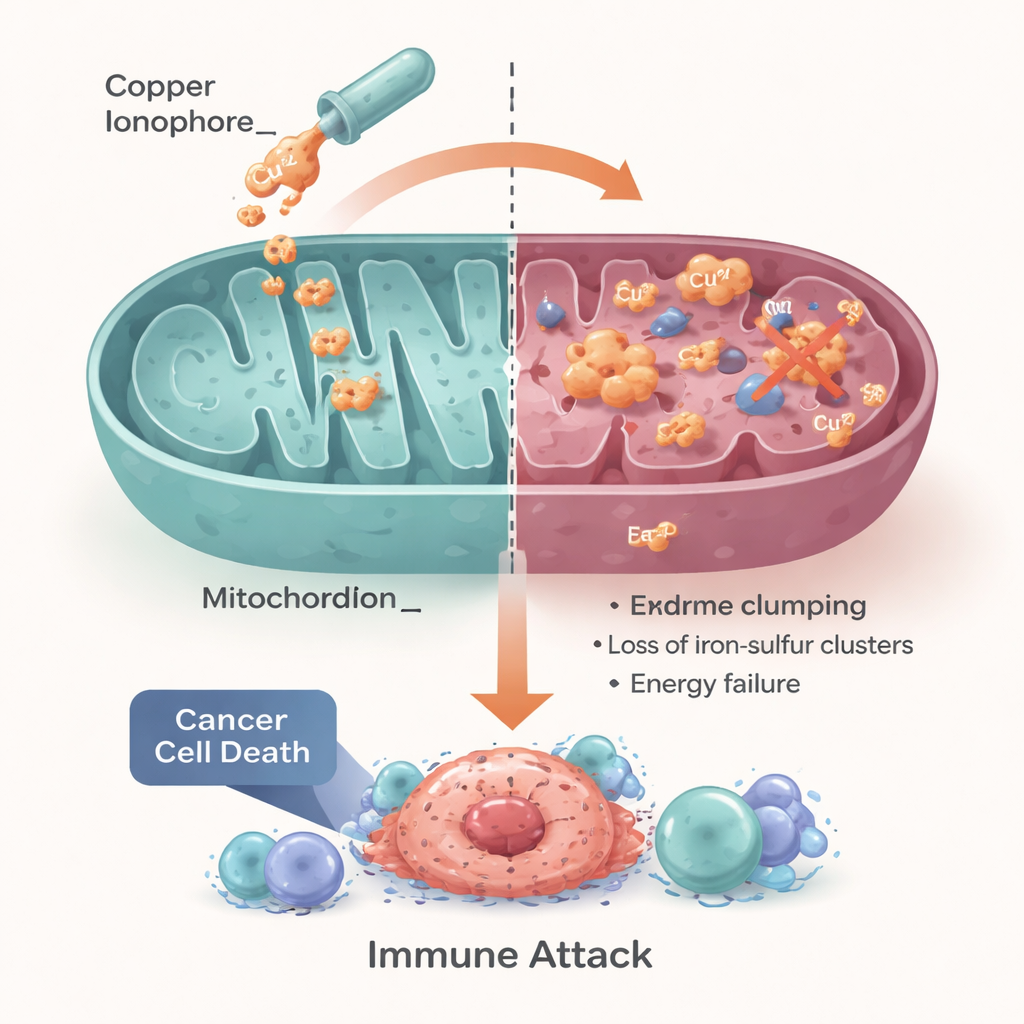
Tirer parti d’une faiblesse cellulaire pour un traitement
Les auteurs concluent que la cuproptose transforme un besoin cellulaire fondamental — une gestion fine du cuivre et de l’énergie — en un talon d’Achille potentiel pour le cancer. Les cancers présentant des anomalies dans la gestion du cuivre ou une dépendance excessive au métabolisme mitochondrial peuvent être particulièrement sensibles aux stratégies basées sur le cuivre, y compris des médicaments repositionnés comme le disulfirame et l’elesclomol, ainsi que des nanoparticules de prochaine génération. Cependant, ils soulignent que le succès dépendra d’un appareillage précis des bons patients avec la bonne approche, en utilisant des biomarqueurs renseignant sur les transporteurs du cuivre, l’activité mitochondriale et le statut immunitaire et en oxygène de la tumeur. Si ces obstacles peuvent être levés, exploiter la cuproptose pourrait offrir aux oncologues un nouveau levier alimenté par un métal pour traiter des tumeurs qui disposent aujourd’hui de peu d’options efficaces.
Citation: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Mots-clés: cuproptose, métabolisme du cuivre, thérapie contre le cancer, métabolisme tumoral, immunothérapie anticancéreuse