Clear Sky Science · fr
Force magnéto-mécanique dynamique dans les lysosomes induit une repolarisation durable des macrophages pour l’immunité antitumorale
Utiliser des forces douces pour réveiller le système immunitaire
Le cancer survit souvent en plongeant les défenses de l’organisme dans un état d’inertie. Cette étude explore une manière inattendue de les réveiller : en tirant physiquement sur de minuscules compartiments à l’intérieur des cellules immunitaires à l’aide de nanoparticules actionnées magnétiquement. Plutôt que de se fier uniquement aux médicaments, les chercheurs utilisent des forces mécaniques finement réglées à l’intérieur des cellules pour reprogrammer les macrophages en combattants tumoraux durables.
Pourquoi les tumeurs solides sont difficiles à traiter
Les immunothérapies modernes du cancer, comme les anticorps anti‑points de contrôle et les cellules immunitaires modifiées, ont transformé le traitement de certains cancers sanguins. Pourtant, pour de nombreuses personnes atteintes de tumeurs solides, comme le cancer du poumon, ces approches ne bénéficient qu’à une minorité. Une raison majeure est le microenvironnement tumoral. Les tumeurs sont entourées d’une niche protectrice remplie de cellules et de signaux qui étouffent l’immunité. Les macrophages, qui peuvent soit attaquer les tumeurs (un état de type M1) soit les aider (un état de type M2), sont souvent poussés vers ce mode pro‑tumeur M2. Inverser cette programmation « nuisible » de façon durable a été difficile avec les seuls médicaments biochimiques conventionnels.
Transformer des nanoparticules en minuscules moteurs mécaniques
L’équipe a conçu des nanomoteurs magnétiques — des particules nanométriques d’oxyde de fer dopé au zinc, recouvertes d’un polymère chargé positivement — qui sont facilement ingérées par les macrophages et se retrouvent concentrées dans les lysosomes, centres de recyclage et de signalisation de la cellule. Une fois à l’intérieur, un champ magnétique rotatif externe fait s’aligner ces particules en chaînes en forme de tige qui tournent, brassant le fluide visqueux des lysosomes et créant de petits tourbillons. Des simulations informatiques et des expériences sur membranes modèles ont montré qu’en réglant soigneusement la fréquence de rotation, la contrainte de cisaillement sur la membrane lysosomale peut atteindre une zone optimale : suffisamment forte pour rendre la membrane momentanément perméable, mais pas au point de la détruire définitivement.
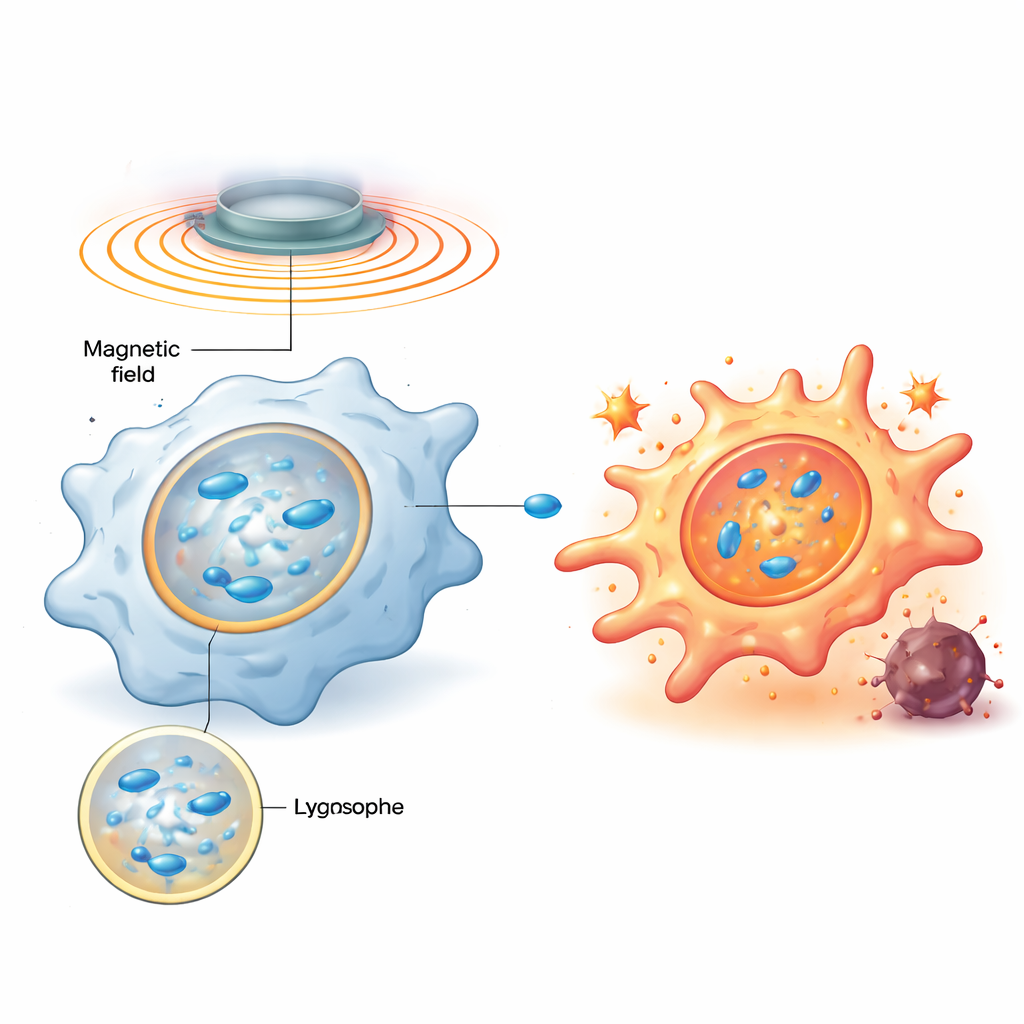
Une impulsion mécanique déclenche une alarme biochimique
Lorsque la membrane lysosomale est brièvement perturbée, une protéine lectine qui se lie aux sucres, appelée galectine‑9, converge vers les zones endommagées et agit comme capteur de ce stress mécanique. L’étude montre que cela active à son tour une enzyme clé de détection énergétique, AMPK, qui stimule ensuite la voie de signalisation NF‑κB — bien connue pour diriger les réponses inflammatoires et antimicrobiennes. Ensemble, ces signaux réorientent le métabolisme des macrophages, quittant un état calme et économe en carburant au profit d’une glycolyse rapide, un profil associé à un comportement agressif de type M1. Fait important, lorsque le champ magnétique est coupé, le lysosome se répare et la signalisation retombe ; lorsque le champ est réactivé plus tard, la même voie se réactive. Ce cycle programmable marche‑arrêt permet aux chercheurs de « tapoter » à plusieurs reprises le même interrupteur mécanique sans tuer les cellules.
Rééduquer les macrophages pour combattre les tumeurs
En culture cellulaire, cette perméabilisation lysosomale induite magnétiquement — nommée MagLMP — a converti des macrophages poussés vers un état pro‑tumeur de type M2 en un état pro‑inflammatoire de type M1. Ces cellules reprogrammées produisaient davantage de cytokines inflammatoires et conservaient leur profil de type M1 pendant plusieurs jours, même dans un milieu de culture dérivé de tumeur qui les pousse habituellement vers le M2. Dans des modèles tumoraux murins, l’incorporation de nanomoteurs magnétiques dans les tumeurs et l’application quotidienne de cycles du champ rotatif ont ralenti la croissance de plusieurs types de cancer. Lorsque les macrophages ont été expérimentalement épuisés, le bénéfice a en grande partie disparu, montrant que ces cellules sont au cœur de l’effet du traitement. Le séquençage ARN unicellulaire des tissus tumoraux a en outre révélé que MagLMP augmentait la proportion de macrophages de type M1, renforçait les neutrophiles antitumoraux et les cellules T CD8 effectrices, et surexprimait des gènes liés à NF‑κB et à la glycolyse au sein des macrophages.
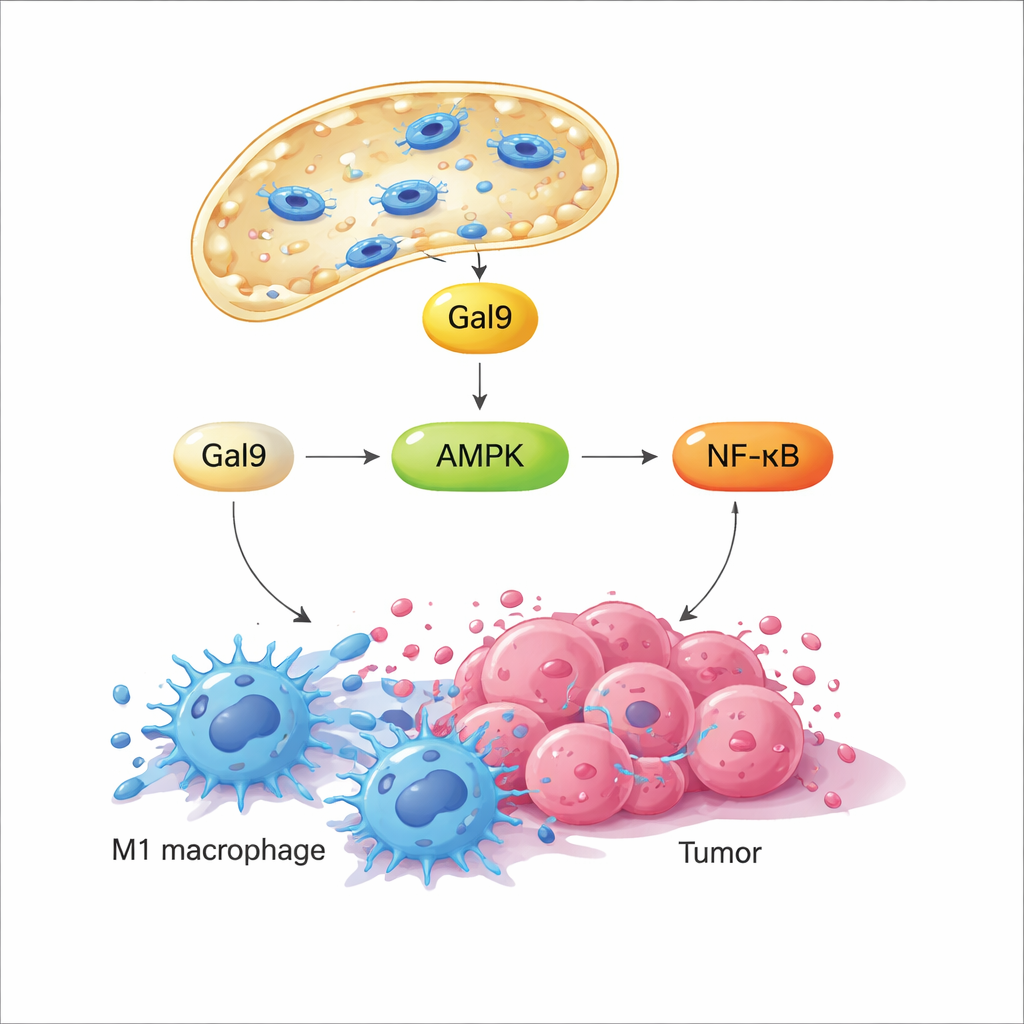
Du contrôle local à une thérapie systémique
Les chercheurs se sont ensuite demandé si cette approche pouvait fonctionner de façon plus proche d’un traitement réel, administrée par voie sanguine. Ils ont injecté les nanomoteurs par voie intraveineuse et utilisé un simple aimant externe pour les concentrer au sein des tumeurs, démontrant une captation efficace par les macrophages du lit tumoral. Le traitement MagLMP qui a suivi a à nouveau orienté les macrophages vers l’état de type M1 et freiné la croissance tumorale. Dans un modèle murin de cancer du poumon à un stade précoce, se développant directement dans le poumon, la combinaison de guidage magnétique et de cycles MagLMP a considérablement prolongé la survie : environ un tiers des souris traitées ont vécu plus de 300 jours, contre seulement quelques semaines chez les animaux témoins. L’association de MagLMP avec un inhibiteur de point de contrôle PD‑1 a encore amélioré le contrôle tumoral dans des modèles difficiles à traiter.
Une nouvelle façon de contrôler l’immunité de l’intérieur
Ce travail montre que de minuscules forces mécaniques bien contrôlées à l’intérieur d’un organite spécifique peuvent être exploitées pour orienter le comportement immunitaire chez des animaux vivants. En « piquant » les lysosomes de manière répétée et réversible, MagLMP active un axe galectine‑9–AMPK–NF‑κB qui reprogramme les macrophages en combattants tumoraux durables sans endommager massivement les cellules. Pour les non‑spécialistes, l’idée centrale est que des signaux physiques — délivrés par des nanomoteurs entraînés magnétiquement — peuvent agir comme un réglage du système immunitaire, offrant une nouvelle classe d’outils destinée à compléter les médicaments dans les immunothérapies anticancéreuses futures.
Citation: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Mots-clés: immunothérapie du cancer, reprogrammation des macrophages, nanoparticules magnétiques, mécanotransduction, signalisation lysosomale