Clear Sky Science · fr
Activation mécanique transitoire du canal Piezo1 facilite l'expansion ex vivo des cellules souches hématopoïétiques
Produire davantage de cellules souches sanguines salvatrices
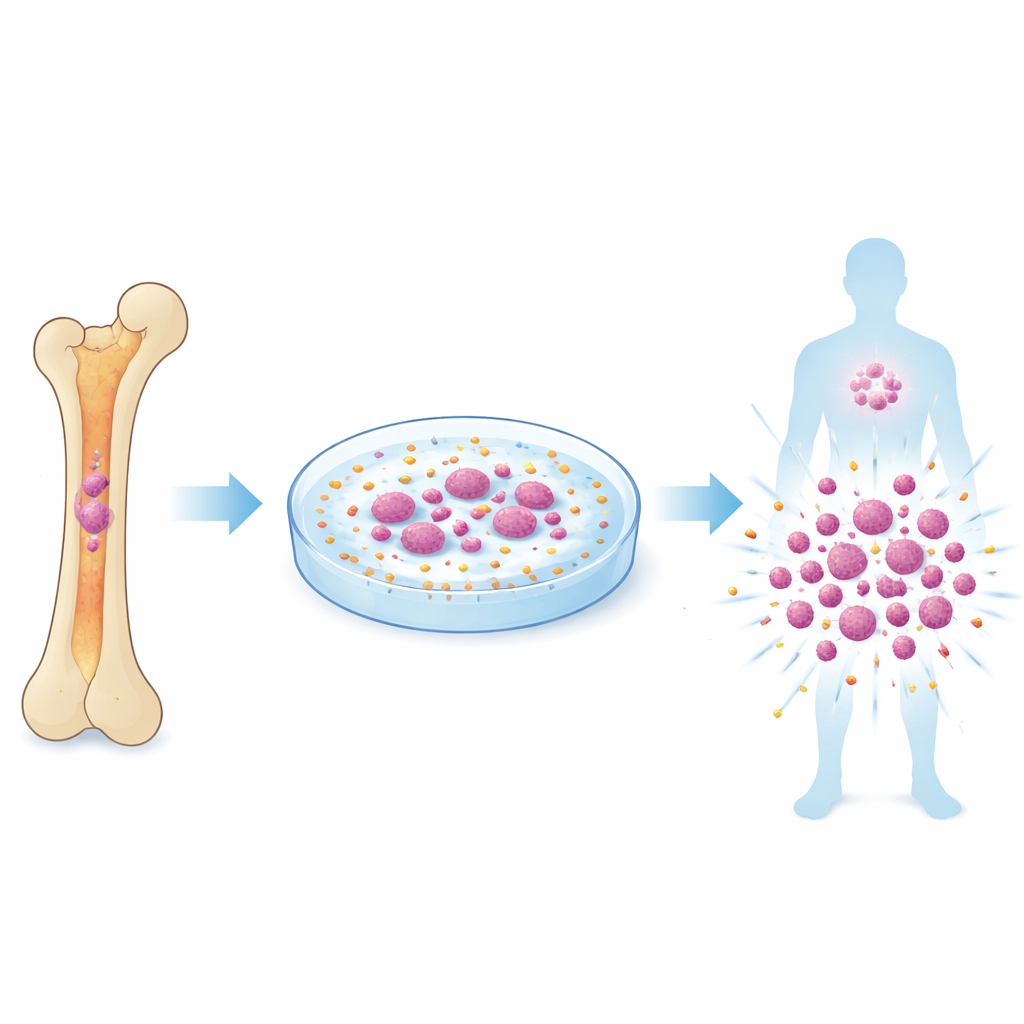
Les greffes de moelle osseuse peuvent guérir certains cancers du sang et des troubles héréditaires, mais les médecins sont souvent limités par le faible nombre de véritables cellules souches hématopoïétiques qu'ils peuvent obtenir d'un donneur. Cette étude révèle une manière surprenante de faire croître ces cellules rares hors du corps en les « touchant » doucement avec de minuscules billes en plastique qui stimulent un senseur mécanique à leur surface. Le travail suggère une nouvelle voie, potentiellement plus sûre, pour générer suffisamment de cellules souches afin que davantage de patients puissent bénéficier de la transplantation.
Pourquoi il est si difficile de faire croître des cellules souches sanguines
Les cellules souches sanguines se trouvent profondément dans nos os et fournissent discrètement, pendant toute la vie, l'ensemble de nos globules rouges, globules blancs et plaquettes. La transplantation de ces cellules peut réinitialiser un système sanguin endommagé, comme dans le traitement de la leucémie, mais seulement si suffisamment de cellules saines sont disponibles et qu'elles conservent leur fonctionnalité complète. Les tentatives d'expansion en culture ont souvent échoué : les cellules ont tendance soit à cesser de se renouveler, soit à perdre leur capacité à rétablir durablement le système sanguin. La plupart des méthodes actuelles reposent sur des cocktails de facteurs de croissance et des modifications génétiques, mais elles ne recréent pas entièrement l'environnement physique complexe de la moelle osseuse, où les cellules souches ressentent en permanence des poussées, des tractions et des pressions.
Un interrupteur mécanique caché sur les cellules souches
Les chercheurs se sont concentrés sur une protéine appelée Piezo1, un petit canal en forme de valve dans la membrane cellulaire qui s'ouvre lorsque la membrane est courbée ou étirée, laissant entrer des ions calcium et déclenchant des signaux intracellulaires. En examinant de nombreux types cellulaires sanguins, ils ont constaté que Piezo1 est particulièrement abondant dans les véritables cellules souches hématopoïétiques. Lorsqu'ils ont supprimé Piezo1 génétiquement, ou l'ont bloqué avec un médicament, les cellules souches cultivées en boîtes ne pouvaient plus s'étendre correctement ni reconstituer le sang des souris après transplantation. Fait intéressant, stimuler Piezo1 en continu avec des activateurs chimiques était également nocif : les cellules accumulaient un excès de calcium, produisaient des molécules réactives délétères et étaient moins capables de s'implanter. Ces résultats suggèrent que les cellules souches ont besoin d'une activation mécanique brève et bien synchronisée de Piezo1, et non d'une stimulation chimique constante.
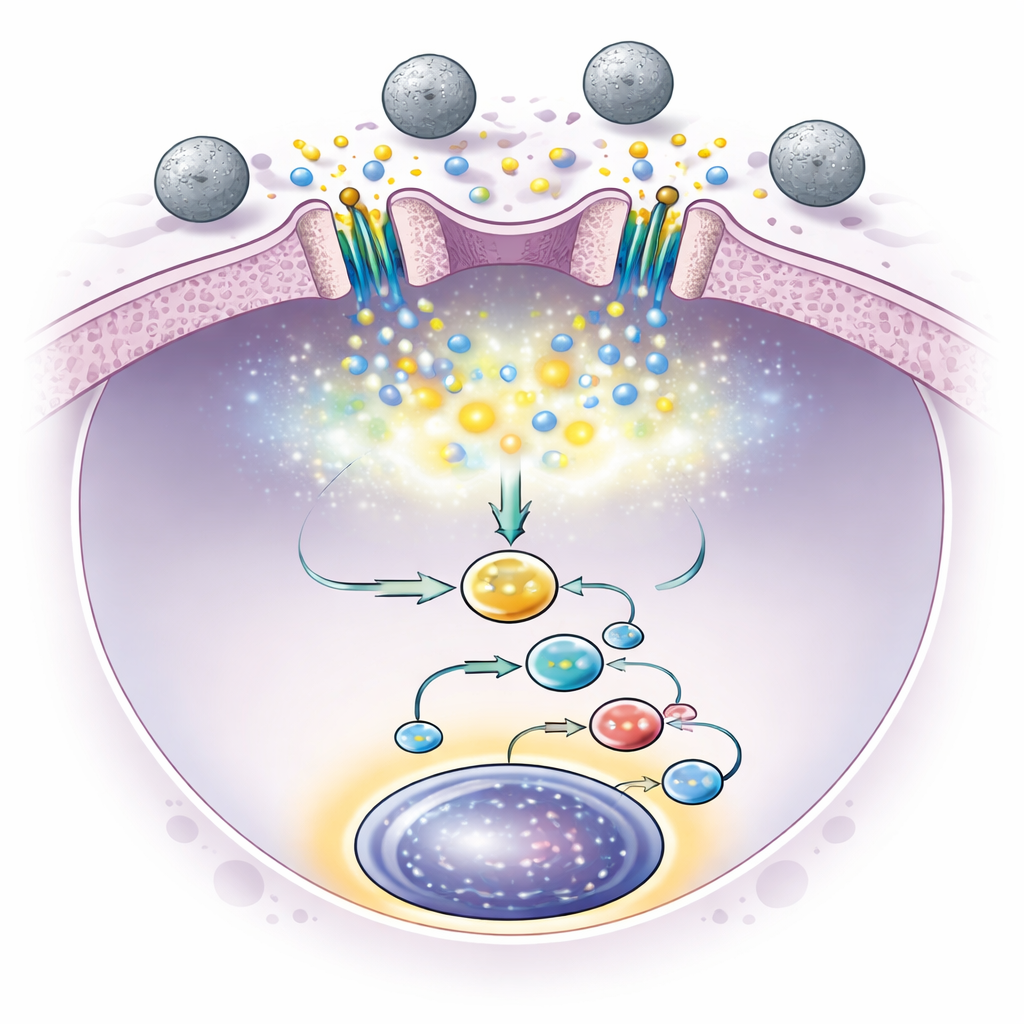
Exploiter de minuscules billes pour stimuler le senseur
Pour fournir juste la bonne impulsion mécanique, l'équipe a utilisé des sphères polymères microscopiques, essentiellement de petites billes en plastique lisses, qui peuvent heurter les cellules souches en culture. Ils ont testé des billes de tailles et de rigidités différentes et ont découvert que des sphères de polystyrène de 500 nanomètres — appelées PS500 — étaient remarquablement efficaces. Lorsque des cellules de moelle osseuse de souris étaient cultivées avec ces billes, le nombre de cellules souches augmentait de façon spectaculaire, et ces cellules conservaient une forte capacité de reconstitution à long terme lors de transplantations en série sur plusieurs générations de souris. Des images soignées et des mesures mécaniques ont montré que les billes indentent à plusieurs reprises la membrane des cellules souches avec de minuscules forces, suffisantes pour ouvrir les canaux Piezo1 en courtes rafales sans submerger les cellules.
Du contact mécanique aux signaux de croissance
L'ouverture brève des canaux Piezo1 provoquait de petites impulsions d'entrée de calcium dans les cellules souches. Cela activait à son tour des voies intracellulaires conduisant à la production de certaines protéines de signalisation, notamment le facteur de croissance interleukine-6. L'interleukine-6 agissait ensuite en rétroaction sur les cellules souches et activait une protéine appelée Stat3 dans leurs noyaux, reconnue pour soutenir la survie et l'auto-renouvellement des cellules souches. Lorsque les chercheurs ont bloqué cette voie Stat3, l'effet bénéfique des billes disparaissait, confirmant que cette chaîne d'événements — contact mécanique, impulsion calcique, libération d'interleukine-6 et activation de Stat3 — était cruciale pour l'expansion. De manière importante, après seulement une courte période d'exposition aux billes, la signalisation restait active et le nombre de cellules souches continuait d'augmenter, soulignant qu'une stimulation constante n'était pas nécessaire.
Promesses pour les transplantations humaines
L'équipe a ensuite appliqué la même approche à des cellules souches sanguines humaines collectées à partir de sang de cordon ombilical, une source courante mais souvent limitée pour la transplantation. Avec les billes PS500, ces cellules humaines se sont multipliées plusieurs fois plus que grâce aux meilleures méthodes basées uniquement sur de petites molécules, tout en conservant leur capacité à reconstituer de façon permanente le sang de souris immunodéficientes. Des études de sécurité chez la souris ont suggéré que les billes n'entrent pas dans les cellules souches, peuvent être efficacement éliminées par simple centrifugation ou filtration, et ne causent pas de lésions organiques évidentes ni d'anomalies sanguines aux doses testées. Cela positionne le système basé sur des billes comme une technologie pratique et potentiellement évolutive pour les banques de sang et les centres de transplantation.
Ce que cela pourrait signifier pour les patients
Essentiellement, l'étude montre qu'un signal mécanique doux — délivré par des billes nanoscopiques en mouvement — peut amener les cellules souches sanguines à se multiplier tout en préservant leur puissance, en activant brièvement un capteur de pression intégré plutôt qu'en le surchargeant. Si cette approche est transposable en clinique, elle pourrait faciliter la génération d'un nombre suffisant de cellules souches de haute qualité à partir d'une petite unité de sang de cordon ou d'un donneur partiel, élargissant l'accès à des greffes curatives pour beaucoup plus de personnes. Elle met également en évidence l'importance de prendre en compte non seulement le « bouillon » chimique entourant les cellules, mais aussi les sensations physiques qu'elles éprouvent, pour débloquer de nouvelles façons de contrôler le destin cellulaire.
Citation: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Mots-clés: cellules souches hématopoïétiques, canaux ioniques mécanosensibles, Piezo1, microsphères en polystyrène, transplantation de cellules souches