Clear Sky Science · fr
La bilirubine active directement RIPK3 pour induire une nécroptose non classique
Quand une molécule utile devient nocive
La bilirubine est surtout connue comme le pigment jaune responsable de la jaunisse néonatale et de la couleur familière des ecchymoses. À faibles concentrations, elle protège même nos cellules contre les dommages. Mais quand la bilirubine s’accumule dans l’organisme et pénètre dans le cerveau, elle peut provoquer des lésions durables, en particulier chez les nouveau-nés et les personnes atteintes d’une insuffisance hépatique sévère. Cette étude révèle une manière surprenante par laquelle un excès de bilirubine peut actionner directement un « interrupteur mortel » moléculaire à l’intérieur des cellules cérébrales, déclenchant une forme destructrice de mort cellulaire et offrant une nouvelle cible pour des thérapies futures.
Du pigment sanguin à la menace cérébrale
La bilirubine est produite lors du recyclage des globules rouges. Normalement, le foie la modifie et l’élimine, maintenant des taux bas et relativement sûrs. Dans certaines situations — comme la jaunisse néonatale, des infections sévères ou une insuffisance hépatique — la bilirubine non traitée peut s’accumuler. Parce qu’elle se dissout facilement dans les graisses, cette forme « libre » peut traverser la barrière hémato-encéphalique, surtout lorsque celle-ci est altérée par la maladie ou l’inflammation. Une fois dans le cerveau, la bilirubine est connue pour être toxique, mais les étapes exactes par lesquelles elle endommage les neurones restaient floues.
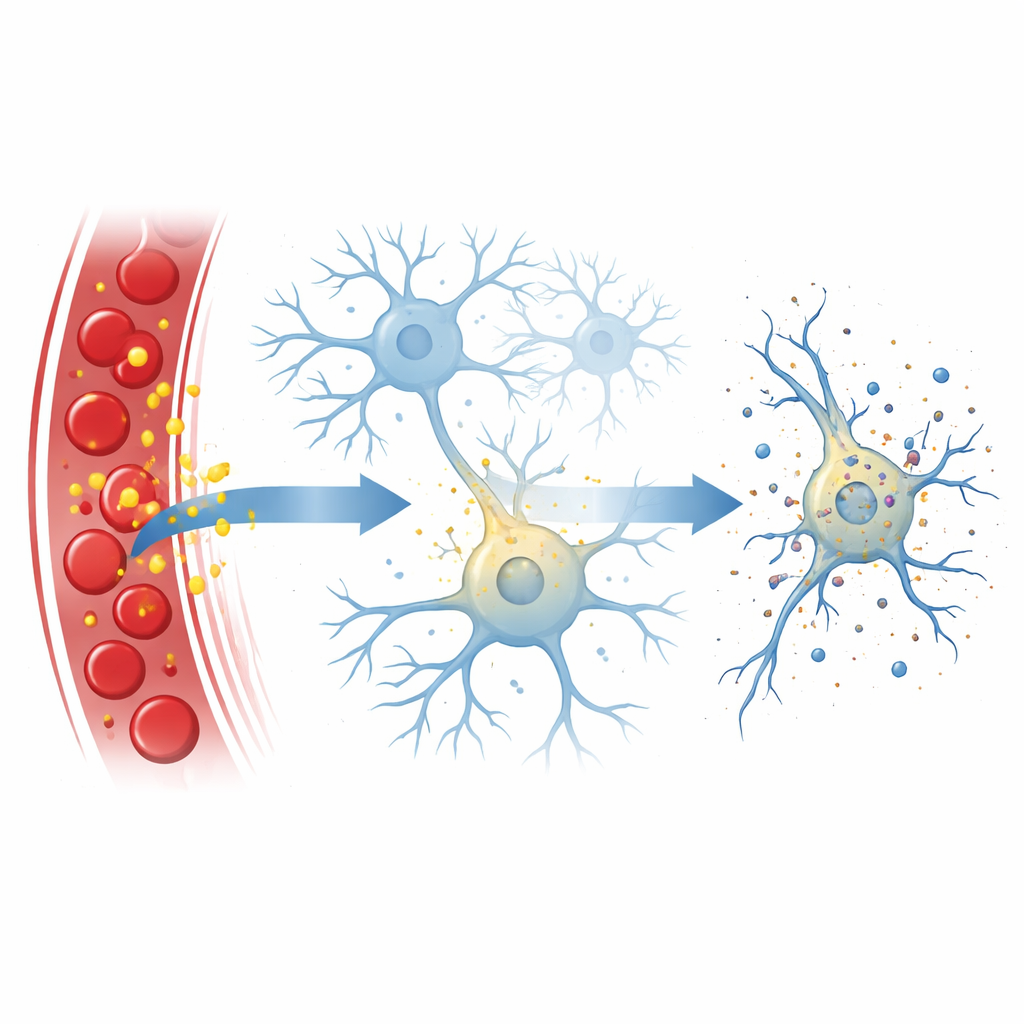
Une explosion cellulaire contrôlée
Les chercheurs se sont concentrés sur la nécroptose, une forme régulée de mort cellulaire qui ressemble à une petite explosion : la cellule gonfle, sa membrane externe se rompt et son contenu se répand, déclenchant souvent une inflammation. Ce processus est normalement conduit par une chaîne de protéines, avec une protéine appelée RIPK3 agissant comme un centre névralgique et une autre, MLKL, perforant la membrane cellulaire. Dans les voies décrites en manuel, RIPK3 est activé par des protéines partenaires qui reconnaissent des signaux de danger tels que des molécules inflammatoires ou du matériel génétique viral. Ici, l’équipe a découvert que la bilirubine peut contourner ces partenaires habituels et induire malgré tout la nécroptose dans les cellules nerveuses.
La bilirubine saisit l’interrupteur mortel de la cellule
En utilisant des neurones en culture, des coupes de cerveau et des modèles murins, les scientifiques ont montré que la bilirubine active sélectivement RIPK3 et son partenaire en aval MLKL dans les cellules nerveuses, tout en laissant les protéines en amont habituellement impliquées pour la plupart inchangées. Des expériences génétiques ont révélé que lorsque RIPK3 ou MLKL étaient supprimés, la bilirubine ne pouvait plus tuer efficacement les neurones. Des tests biochimiques sont allés plus loin : la bilirubine se liait physiquement à RIPK3 en deux sites spécifiques au sein de son noyau actif, favorisait l’agrégation des molécules de RIPK3 et augmentait leur activité kinase — la fonction chimique qui déclenche la voie de mort. Cette interaction directe avec RIPK3 ne dépendait pas de la surface d’interaction typique de la protéine (le domaine RHIM) ni d’autres protéines adaptatrices, délimitant ainsi une route non classique vers la nécroptose.
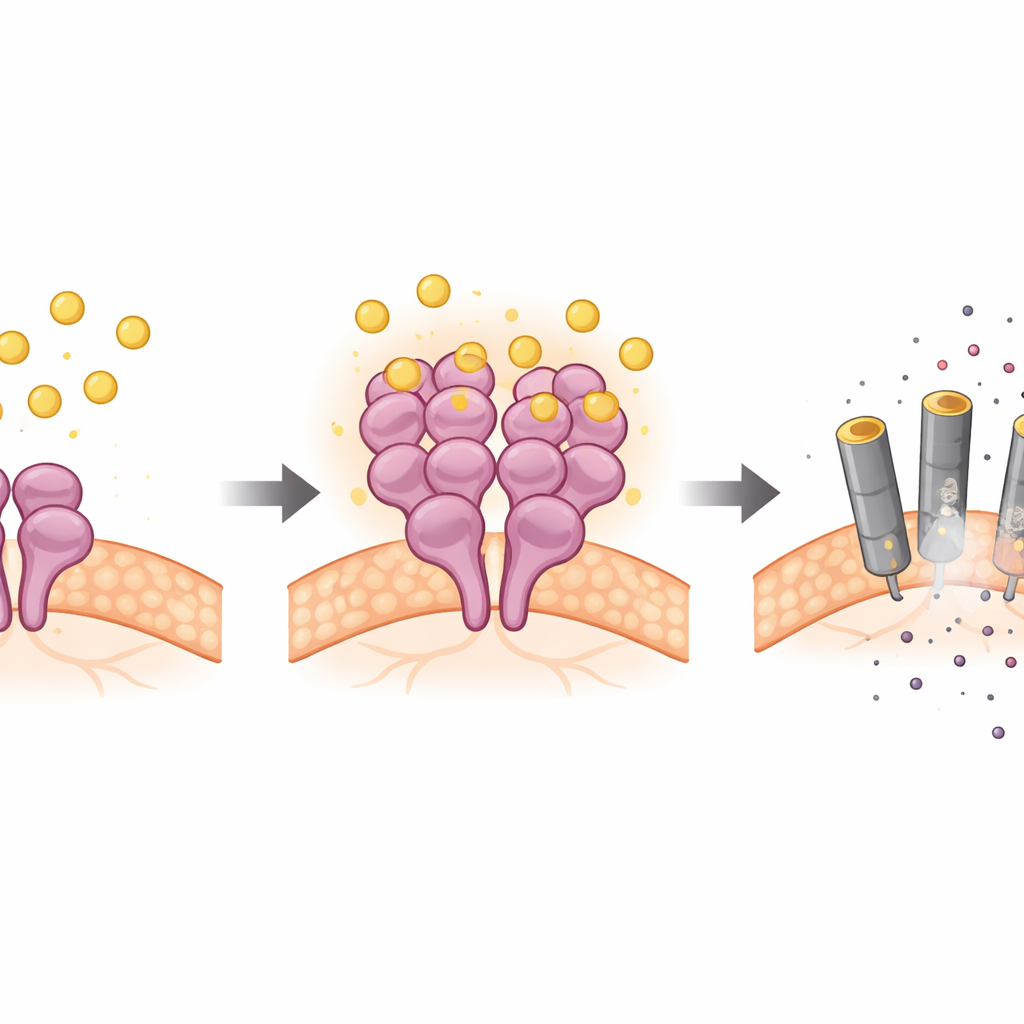
Preuves issues du cerveau vivant
Pour savoir si ce mécanisme a une importance chez l’animal entier, l’équipe a élevé les taux de bilirubine chez la souris soit en l’injectant dans le cerveau, soit en provoquant une atteinte hépatique et une inflammation de sorte que la bilirubine pénètre naturellement dans le cerveau. Chez des souris normales, cela entraînait une forte activation de RIPK3 et MLKL dans des régions cérébrales vulnérables, une augmentation des marqueurs de mort cellulaire et une perte visible de neurones sains. Les souris conçues pour être dépourvues de RIPK3 étaient protégées : leurs neurones montraient beaucoup moins de dégâts, moins de signaux de mort et des réponses inflammatoires réduites, bien que les taux de bilirubine aient été tout aussi élevés. Fait important, une forme traitée et hydrosoluble de la bilirubine, généralement considérée comme inoffensive, n’activait ni RIPK3 ni n’induisait de lésions cérébrales similaires, soulignant que la forme non modifiée et liposoluble est la véritable responsable.
Qu’est-ce que cela signifie pour les patients
Ce travail montre que l’excès de bilirubine non conjuguée peut activer directement RIPK3, déclenchant une rupture contrôlée mais destructrice des cellules cérébrales par nécroptose. Plutôt que d’agir seulement comme un poison général ou une source de stress oxydatif, la bilirubine se comporte comme un petit activateur moléculaire d’un programme de mort spécifique dans les neurones et les cellules immunitaires cérébrales. Pour les patients atteints d’une jaunisse sévère ou d’une insuffisance hépatique, cela suggère que bloquer RIPK3 ou MLKL — en particulier avec des médicaments capables de pénétrer dans le cerveau — pourrait un jour aider à limiter les dommages neurologiques. En termes simples, l’étude montre comment un pigment normalement utile peut devenir un assassin moléculaire précis, et elle indique de nouvelles façons de le neutraliser sans perturber ses rôles protecteurs quotidiens.
Citation: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Mots-clés: neurotoxicité de la bilirubine, nécroptose, RIPK3, insuffisance hépatique et lésion cérébrale, voies de mort cellulaire