Clear Sky Science · fr
Pipeline intégrée de profilage spatial pour déterminer les architectures du microenvironnement tumoral dans des spécimens cliniques archivés en utilisant la technologie superplex CmTSA
Pourquoi le paysage caché autour des tumeurs compte
Les cancers ne croissent pas isolément. Ils sont entourés d’un voisinage animé composé de cellules immunitaires, de cellules de soutien, de vaisseaux sanguins et de tissu cicatriciel qui forment ensemble le « microenvironnement » de la tumeur. Cet article présente une méthode pratique pour cartographier en détail ce paysage caché en utilisant des échantillons tissulaires courants d’hôpital. En révélant quels types de cellules se côtoient et comment elles s’organisent en quartiers bénéfiques ou nuisibles, la méthode pourrait aider les médecins à mieux prédire le comportement d’un cancer et à choisir les traitements les plus susceptibles d’être efficaces.
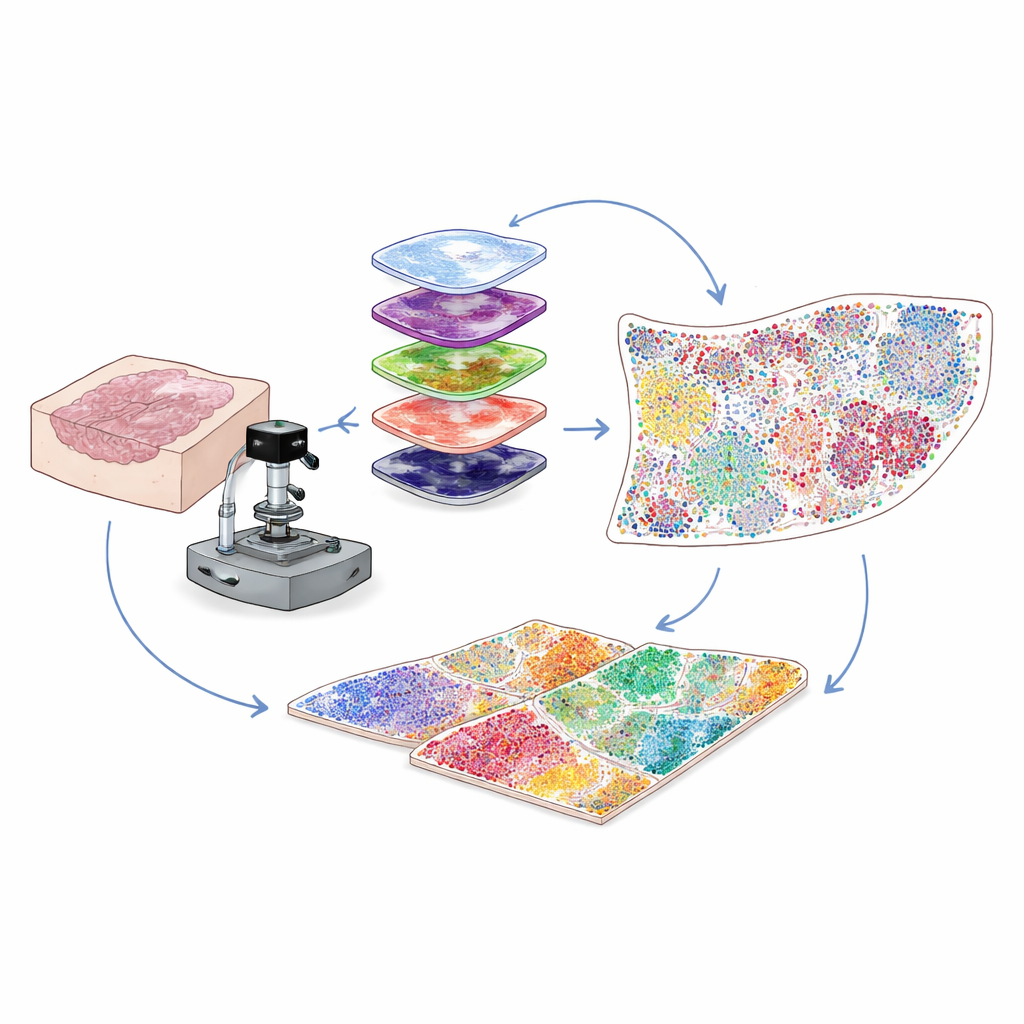
Voir davantage dans des échantillons hospitaliers quotidiens
La plupart des échantillons cliniques de cancer sont conservés sous forme de fines coupes de tissu incluses dans de la paraffine, appelées blocs FFPE, qui peuvent être stockées pendant des années. Ce sont une mine d’or pour la recherche, mais un problème technique a freiné les scientifiques : ces échantillons présentent une fluorescence de fond naturelle qui masque les signaux faibles de nombreuses protéines importantes. Les auteurs ont résolu ce problème en combinant une lumière intense, finement calibrée, avec un traitement chimique doux pour effacer sélectivement cette fluorescence de fond sans abîmer le tissu ni les cibles protéiques. Cette étape hybride optique et chimique de « blanchiment » améliore nettement la clarté des images, permettant de détecter des signaux protéiques faibles qui autrement seraient perdus.
Peindre des dizaines d’étiquettes protéiques sur la même coupe
Pour savoir quelles cellules sont présentes et ce qu’elles font, les chercheurs colorent les tissus avec des anticorps qui se fixent sur des protéines spécifiques. Les méthodes multiplex traditionnelles peinent soit avec une faible intensité pour les protéines rares, soit à suivre simultanément un nombre limité de marqueurs. Ici, l’équipe utilise une approche appelée amplification du signal par tyramide cyclique. À chaque cycle, un petit ensemble de marqueurs est coloré puis « développé » enzymatiquement en taches fluorescentes brillantes et permanentes. Les anticorps sont ensuite délicatement retirés tandis que le signal reste, le fond est à nouveau blanchi, et le groupe de marqueurs suivant est ajouté. En répétant ce cycle de nombreuses fois et en alignant les images à l’aide du signal constant des noyaux cellulaires, ils peuvent visualiser de manière fiable 30 à 60 protéines différentes sur une seule coupe, sur l’ensemble d’une lame, à la résolution de la cellule unique.
Transformer des images colorées en atlas cellule par cellule
Les images à haut multiplex contiennent des millions de pixels, bien plus que ce qu’un humain pourrait analyser à l’oeil nu. Les auteurs construisent donc une chaîne de traitement par vision par ordinateur qui identifie et délimite d’abord chaque noyau cellulaire à l’aide d’outils d’apprentissage profond initialement développés pour la segmentation cellulaire générale. Ensuite, en fonction de l’endroit où apparaît la fluorescence de chaque protéine—à la membrane, dans le cytoplasme ou dans le noyau—et sur la base d’ensembles de règles logiques, chaque cellule se voit attribuer un type ou un sous-type, par exemple cellule tumorale, cellule T auxiliaire, cellule T cytotoxique, cellule B, fibroblaste ou autre. Le résultat est un tableau numérique listant, pour chaque cellule sur la lame, son identité et ses coordonnées exactes. Cela transforme une image complexe en une carte quantitative de qui se trouve où dans le microenvironnement tumoral.
Révéler les voisinages cellulaires qui influencent le pronostic
Les cellules agissent rarement seules ; ce qui compte, ce sont leurs voisins. Pour capturer cela, les chercheurs testent différentes façons de définir des voisinages locaux autour de chaque cellule et retiennent une approche réseau basée sur un rayon. Imaginez tracer un petit cercle—environ l’épaisseur d’un cheveu humain—autour de chaque cellule et lister qui se trouve à l’intérieur. En regroupant les cellules dont les cercles environnants présentent des mélanges de voisins similaires, la méthode identifie des « niches fonctionnelles » récurrentes, comme des zones riches en cellules immunitaires, des barrières denses en fibroblastes, ou des régions dominées par la tumeur. L’application de cette stratégie aux tissus colorectaux montre que les voisinages basés sur un rayon correspondent mieux aux structures anatomiques connues que d’autres méthodes. Dans des échantillons de cancer du col de l’utérus provenant de patients avec des issues favorables versus défavorables, l’équipe observe que des niches riches en cellules immunitaires se regroupent près du bord tumoral chez les patients qui vont bien, tandis que les patients avec un mauvais pronostic présentent des zones épaisses riches en fibroblastes qui entourent les cellules tumorales et semblent isoler les cellules immunitaires attaquantes.
Des cartes spatiales à des traitements sur mesure
En combinant une coloration de haute qualité et abordable pour de nombreuses protéines avec une analyse d’image robuste, ce travail fournit une pipeline complète applicable à un grand nombre d’échantillons hospitaliers standards. La méthode transforme le tissu préservé en cartes détaillées montrant comment les cellules tumorales, immunitaires et stromales s’organisent et interagissent. Pour le lecteur non spécialiste, la conclusion est que non seulement les types cellulaires, mais leurs schémas de voisinage précis, influencent le comportement d’un cancer. Cette plateforme peut aider les chercheurs à localiser des hotspots immunitaires protecteurs, à identifier des barrières cellulaires suppressives et, en fin de compte, à soutenir des pronostics plus précis et des stratégies d’immunothérapie mieux ajustées.
Citation: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Mots-clés: microenvironnement tumoral, protéomique spatiale, imagerie multiplex, immunologie du cancer, analyse monocellulaire