Clear Sky Science · fr
L’acide palmitique active c-Myc via des voies dépendantes de la palmitoylation double pour favoriser le cancer du côlon
Pourquoi la graisse dans notre alimentation compte pour la santé du côlon
Le cancer du côlon est l’un des cancers les plus fréquents dans le monde, et de nombreuses études associent les régimes riches en graisses à un risque accru de développer la maladie. Pourtant, la manière dont certaines graisses alimentaires influencent les gènes oncogéniques dans les cellules du côlon restait peu claire. Cet article révèle une connexion directe entre l’acide palmitique — une graisse majeure présente dans la viande, les produits laitiers et de nombreux aliments transformés — et un puissant gène promoteur de cancer, c-Myc. Les travaux montrent comment cette graisse courante peut alimenter l’inflammation, reprogrammer le métabolisme cellulaire et enfermer les tumeurs du côlon dans une dépendance néfaste à l’acide palmitique.
De la graisse quotidienne à l’inflammation chronique de l’intestin
L’acide palmitique est un acide gras saturé abondant dans les régimes riches en graisses. Les chercheurs ont nourri des souris avec différents régimes : alimentation standard, régimes enrichis en acide palmitique ou régime classique riche en graisses, puis ont déclenché une colite, un type d’inflammation du côlon. Les souris nourries avec des régimes riches en acide palmitique ou en graisses ont développé une inflammation intestinale plus sévère que celles sous régime normal. Leurs côlons étaient plus courts, davantage endommagés à l’examen microscopique et remplis de cellules immunitaires, signes d’une lésion inflammatoire agressive. Les profils d’expression génique dans ces tissus enflammés ressemblaient à ceux observés dans un modèle bien connu de cancer du côlon induit par l’inflammation, suggérant que l’acide palmitique pousse l’environnement intestinal vers un état favorable au cancer.
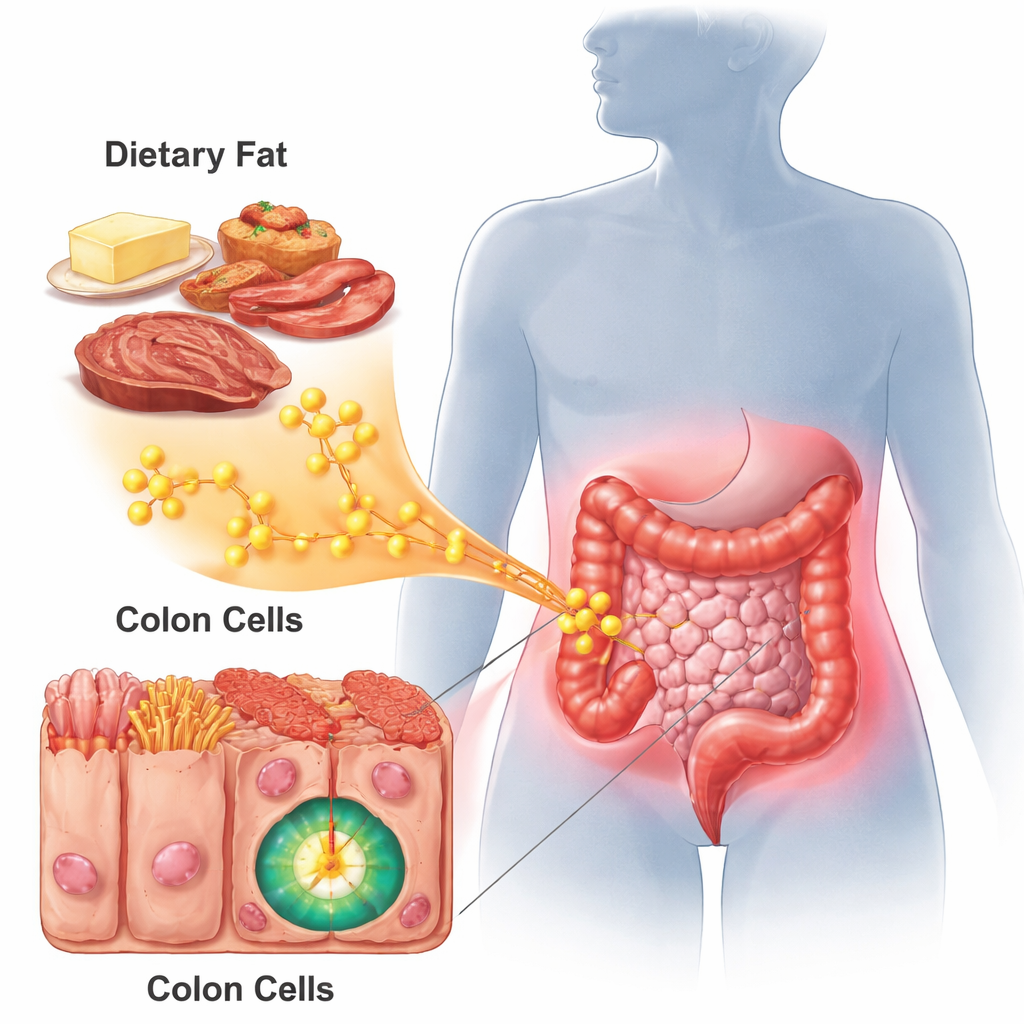
Un interrupteur détectant les graisses qui suralimente un gène cancéreux
L’équipe s’est focalisée sur c-Myc, un gène maître qui stimule la croissance cellulaire, la survie et des comportements de type souche dans de nombreux cancers. Tant dans les tissus de souris que dans des échantillons humains de cancer du côlon, l’activité de c-Myc — et non sa quantité — était anormalement élevée. En comparant les profils géniques des souris alimentées en acide palmitique, des tumeurs coliques précoces et des cancers avancés, les scientifiques ont identifié une protéine auxiliaire critique : ZDHHC9. Cette enzyme attache des chaînes d’acides gras à d’autres protéines dans un processus appelé palmitoylation. Ils ont découvert qu’une molécule inflammatoire, l’IL-1β, augmente lors de la colite et stimule les niveaux de ZDHHC9, qui modifie ensuite directement c-Myc en un site spécifique. Cette « étiquette » grasse renforce le partenariat de c-Myc avec son partenaire de liaison MAX, rendant le complexe c-Myc plus actif pour activer les gènes de croissance et de pluripotence, même sans augmentation de l’expression du gène c-Myc lui-même.
Comment les cellules cancéreuses deviennent dépendantes de l’acide palmitique
À mesure que les tumeurs progressent, la relation entre c-Myc et l’acide palmitique bascule d’une poussée unidirectionnelle à une boucle autorenforçante. L’étude montre que c-Myc active directement FATP2, un transporteur qui importe des acides gras à longue chaîne comme l’acide palmitique dans les cellules cancéreuses du côlon. Les tumeurs présentant une activité accrue de c-Myc présentaient davantage de FATP2 et des signatures métaboliques d’acides gras plus prononcées. En culture cellulaire et dans des greffes tumorales chez la souris, un apport supplémentaire d’acide palmitique a accéléré la croissance des cellules cancéreuses et augmenté la palmitoylation de c-Myc, amplifiant encore son activité. Cela crée un cercle vicieux : l’inflammation et le régime augmentent l’acide palmitique, qui active c-Myc ; c-Myc augmente alors FATP2, faisant entrer encore plus d’acide palmitique et maintenant le « moteur de croissance » en marche.
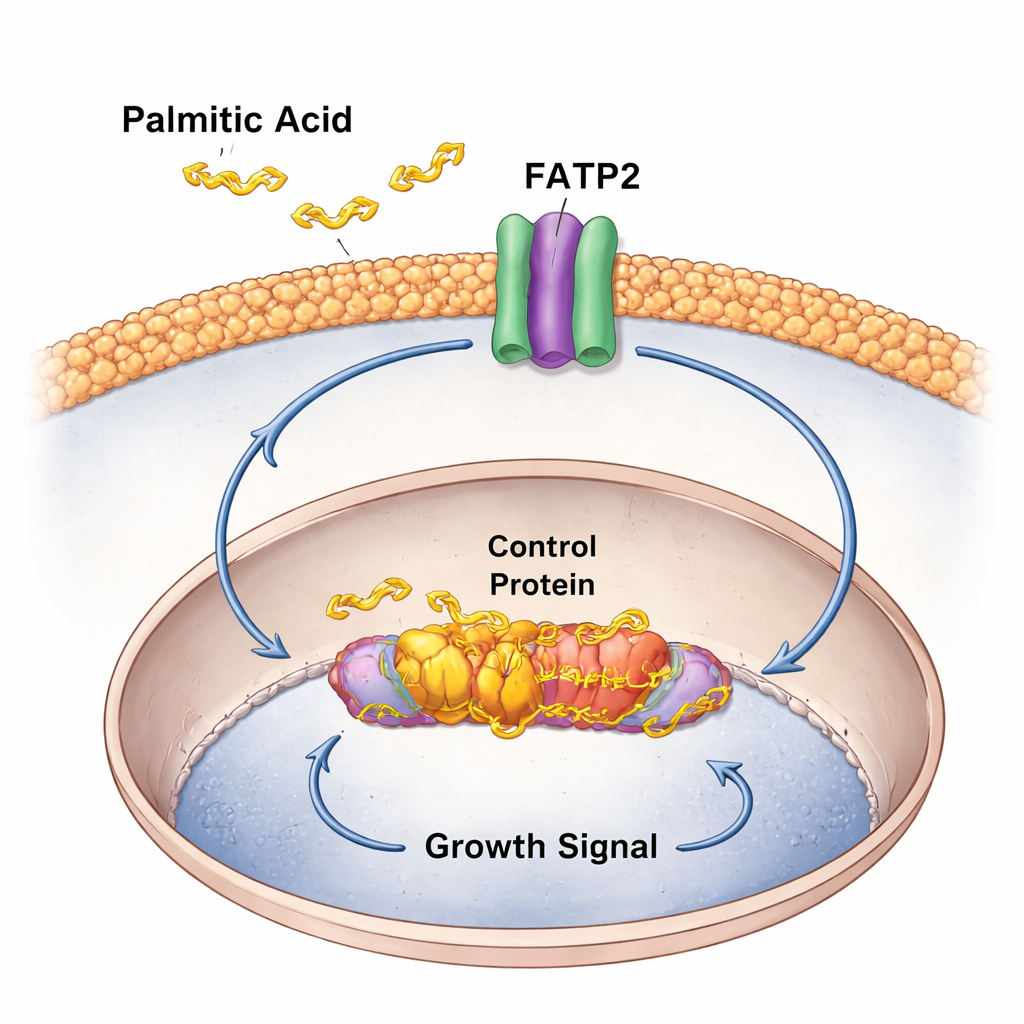
Transformer une faiblesse métabolique en opportunité thérapeutique
Parce que les tumeurs du côlon dans ce modèle deviennent dépendantes de l’acide palmitique et de l’axe ZDHHC9–FATP2–c-Myc, les auteurs ont testé si rompre ce circuit pouvait ralentir le cancer. L’utilisation d’outils génétiques pour désactiver ZDHHC9 ou FATP2 dans les cellules tumorales a considérablement réduit la croissance tumorale chez des souris alimentées avec des régimes riches en acide palmitique. La combinaison des deux réductions d’expression était encore plus efficace. Ils ont ensuite utilisé des inhibiteurs de type médicament : le 2BP, qui bloque de façon large les enzymes de palmitoylation, et la Lipofermata, qui inhibe FATP2. Chaque traitement a réduit la taille des tumeurs et l’activité des gènes cibles de c-Myc, et ensemble ils ont réduit les tumeurs de plus de 80 %, sans toxicité évidente chez les souris. Cela suggère que cibler la façon dont les cellules cancéreuses traitent l’acide palmitique pourrait indirectement maîtriser un gène autrement « difficile à cibler » comme c-Myc.
Ce que cela signifie pour l’alimentation et les thérapies futures
Concrètement, cette étude révèle qu’une graisse alimentaire courante peut agir comme un signal qui passe c-Myc à la vitesse supérieure, d’abord en aggravant l’inflammation intestinale, puis en câblant les tumeurs matures pour qu’elles désirent davantage d’acide palmitique. Plutôt que de n’être qu’un carburant, l’acide palmitique devient une partie d’un réseau de communication entre l’alimentation, le système immunitaire et les gènes oncogéniques. Le travail suggère deux conclusions principales : limiter les aliments riches en acide palmitique pourrait contribuer à réduire le risque de cancer du côlon, en particulier chez les personnes souffrant d’inflammation intestinale chronique, et de nouvelles thérapies ciblant ZDHHC9 ou FATP2 pourraient exploiter la dépendance tumorale à cette graisse pour ralentir ou arrêter la maladie.
Citation: Du, W., Zhang, J., Wang, Y. et al. Palmitic acid activates c-Myc via dual palmitoylation-dependent pathways to promote colon cancer. Cell Discov 12, 12 (2026). https://doi.org/10.1038/s41421-026-00869-6
Mots-clés: cancer du côlon, régime riche en graisses, acide palmitique, c-Myc, dépendance métabolique