Clear Sky Science · fr
Chronobiologie des virus neurotropes : entrée virale rythmique et horloges hôtes arrhythmiques
Pourquoi le moment compte pour les infections cérébrales
De nombreux virus dangereux, notamment la rage et les herpès, ont la capacité d’envahir le cerveau et les nerfs. Cette étude pose une question étonnamment simple aux implications majeures : l’heure de la journée modifie‑t‑elle la facilité avec laquelle ces virus « neurotropes » peuvent pénétrer notre système nerveux, et les virus peuvent‑ils à leur tour perturber nos horloges internes ? Comprendre ce dialogue bidirectionnel entre horloges biologiques et virus pourrait ouvrir de nouvelles façons d’optimiser la vaccination, les antiviraux et même l’organisation du travail posté pour réduire le risque.
Horloges quotidiennes et portes d’entrée virales
Presque chaque cellule du corps porte un système de timing intégré sur 24 heures, souvent appelé horloge circadienne. Il est gouverné par un ensemble de protéines clés de l’horloge, dont BMAL1 et REV‑ERBα, qui activent et inhibent des milliers de gènes en ondes rythmiques. Les auteurs se sont concentrés sur les « poignées de porte » que les virus utilisent pour entrer dans les cellules — les protéines réceptrices à la surface cellulaire — pour des dizaines de virus ciblant ou envahissant le cerveau. En examinant des organoïdes cérébraux dérivés de cellules souches, des lignées cellulaires d’origine nerveuse et des tissus de souris, ils ont constaté que la plupart de ces récepteurs viraux montent et descendent au cours de la journée. Ces rythmes suivaient de près l’activité des composants de l’horloge, suggérant que notre système de timing quotidien contrôle discrètement combien de points d’entrée viraux sont disponibles à chaque heure.
Un facteur du cycle cellulaire devient un messager de l’horloge
En creusant plus loin, les chercheurs ont demandé comment une protéine habituellement connue pour contrôler la division cellulaire, appelée E2F8, s’intègre à ce réseau temporel. Ils ont découvert qu’E2F8 est lui‑même sous contrôle circadien et se comporte comme un relais entre l’horloge et au moins un récepteur clé de la rage, p75NTR. Lorsque la protéine d’horloge REV‑ERBα est active, elle réprime E2F8. À son tour, un faible niveau d’E2F8 libère la gêne sur le gène p75NTR, permettant la production de davantage de ce récepteur et rendant les cellules plus accueillantes pour le virus de la rage. Fait marquant, E2F8 exerce aussi un retour sur l’horloge : il peut se lier directement aux régions de contrôle des gènes centraux de l’horloge tels que REV‑ERBα et PER2 et en atténuer l’activité. Cela crée une boucle de rétroaction dans laquelle un régulateur du cycle cellulaire contribue à façonner les rythmes quotidiens et, à travers eux, la vulnérabilité des cellules nerveuses à l’infection.
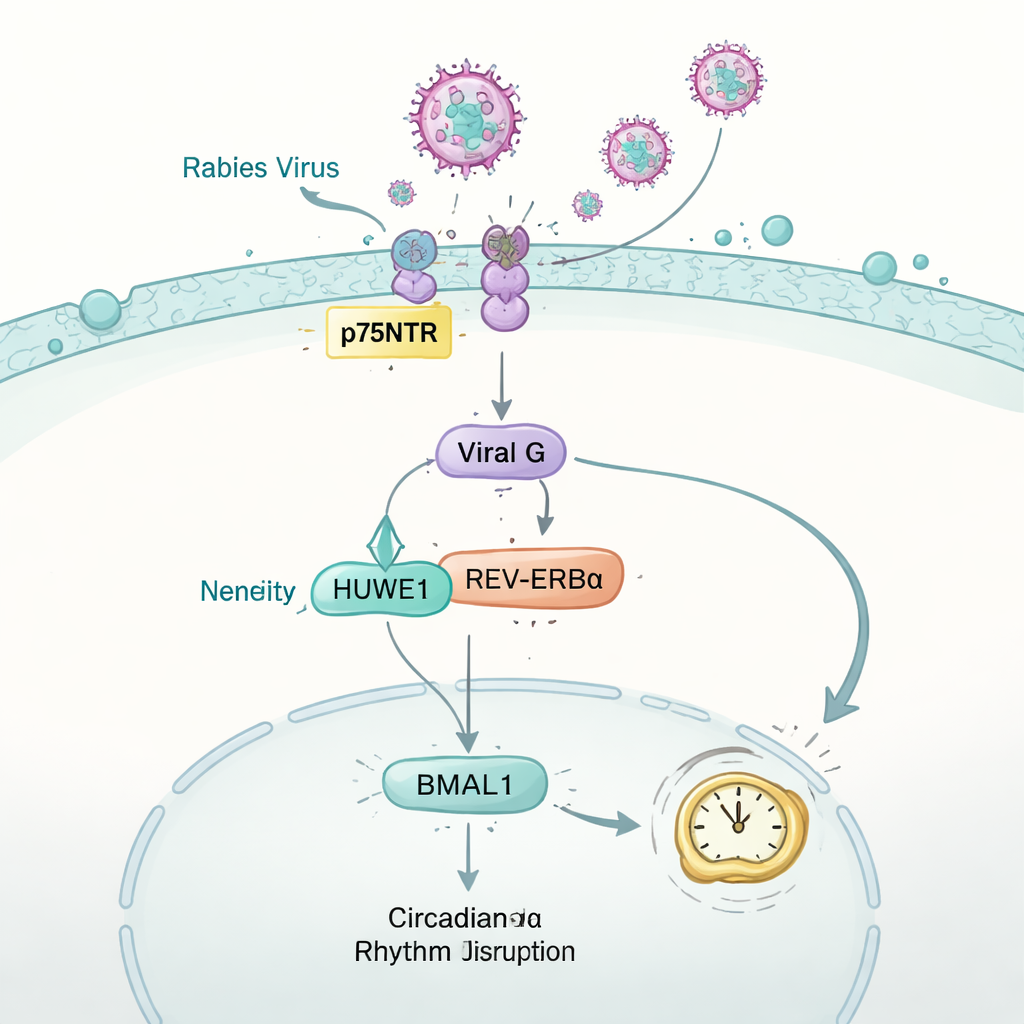
Comment le virus de la rage dérégle l’horloge
L’étude a ensuite inversé la question : un virus peut‑il riposter contre l’horloge ? En utilisant des souris infectées par le virus de la rage, l’équipe a surveillé l’activité de nage, le métabolisme et la chimie respiratoire. Malgré un apport alimentaire normal en début d’infection, les animaux ont progressivement perdu les rythmes jour‑nuit réguliers observés chez les souris saines. Dans le cerveau et plusieurs autres organes, les niveaux de la protéine d’horloge cruciale BMAL1 ont chuté brutalement. Dans des cellules de type nerveux, cet effet a pu être attribué à la glycoprotéine « G » du virus de la rage, une protéine de surface qui aide normalement le virus à fusionner avec les cellules. G a détourné une enzyme hôte nommée HUWE1, qui sert habituellement à marquer une autre protéine d’horloge, REV‑ERBα, pour son élimination. En entrant en compétition pour HUWE1, la protéine virale G a stabilisé REV‑ERBα, entraînant une suppression accrue de BMAL1 et, finalement, une perturbation de l’horloge qui maintient la physiologie sur un rythme de 24 heures.
Timing, décalage horaire et gravité de l’infection
Pour tester si ces changements moléculaires ont des conséquences pour l’organisme entier, l’équipe a infecté des souris par la rage à différents moments de la journée, sous cycles lumière‑obscurité réguliers, sous conditions chroniques de « décalage horaire », et chez des animaux génétiquement dépourvus de REV‑ERBα. Les souris infectées au début de leur phase active (nuit), lorsque le récepteur de la rage p75NTR atteint son pic, ont perdu du poids plus rapidement, présenté des charges virales plus élevées dans plusieurs régions cérébrales, davantage d’inflammation cérébrale et sont mortes plus tôt que les souris infectées au début de leur phase de repos. Les souris exposées à des décalages de phase répétés mimant le travail posté rotatif ont perdu les rythmes normaux de l’horloge dans le cerveau, ont montré des niveaux persistants de p75NTR plus élevés, disposaient de signaux antiviraux de base plus faibles et ont développé une maladie plus sévère. En revanche, les souris sans REV‑ERBα exprimaient moins de p75NTR, portaient des charges virales plus faibles et survivaient plus longtemps après l’infection, indiquant que ce composant de l’horloge est un gardien critique de la gravité de la rage.
Qu’est‑ce que cela implique pour les humains
En termes simples, l’étude montre que nos horloges internes ne définissent pas seulement les heures de sommeil ; elles ouvrent et ferment aussi des portes moléculaires utilisées par les virus envahissant le cerveau, et ces mêmes virus peuvent riposter en brouillant l’horloge. Un facteur unique, REV‑ERBα, occupe une jonction clé : avec E2F8, il modifie à la fois les niveaux de récepteurs et le timing quotidien, tandis que le virus de la rage le manipule à son avantage. Ces connaissances suggèrent des pistes pratiques. Les vaccins ou antiviraux pourraient être plus efficaces à certains moments de la journée, quand les récepteurs sont bas ou que les réponses immunitaires sont fortes. Les personnes dont les rythmes sont chroniquement perturbés — comme les travailleurs postés ou les voyageurs fréquents — pourraient courir des risques accrus face à certaines infections neurotropes. Cibler REV‑ERBα ou des voies associées pourrait aider à renverser la balance en faveur de l’hôte, réduire la sévérité des infections et améliorer les résultats.
Citation: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Mots-clés: horloge circadienne, virus neurotropes, rage, récepteurs viraux, chronothérapie