Clear Sky Science · fr
ATP6V1B2 atténue la stéatose hépatique en favorisant l’acidification lysosomale dans les hépatocytes
Pourquoi une graisse hépatique compte
Beaucoup de personnes accumulent de la graisse dans le foie sans s’en rendre compte. Cette affection, désormais appelée maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD), touche environ un quart de la population mondiale et peut évoluer silencieusement vers une fibrose, une insuffisance hépatique et d’autres maladies graves. Pourtant, les médecins disposent encore de peu d’outils fiables pour prédire qui va s’aggraver, et peu de traitements ciblent directement les problèmes cellulaires sous-jacents. Cette étude révèle comment une « pompe acide » cellulaire peu connue aide les cellules hépatiques à éliminer l’excès de graisse et propose une nouvelle orientation pour le diagnostic et la thérapie.
Un assistant caché à l’intérieur des cellules hépatiques
À l’intérieur de chaque cellule hépatique se trouvent de petits centres de recyclage appelés lysosomes. Ils dépendent d’un bain acide interne pour dégrader les éléments usés et les lipides excédentaires. L’acidité est maintenue par une pompe moléculaire connue sous le nom de V-ATPase, composée de plusieurs sous-unités protéiques. Les auteurs se sont intéressés à une pièce cruciale, ATP6V1B2, particulièrement importante pour préserver l’acidité lysosomale. Ils ont cherché à savoir si des altérations de cette protéine pouvaient aider à expliquer l’accumulation de graisse dans la MASLD et si ses niveaux sanguins pourraient signaler la maladie.
Indices tirés des patients et des modèles animaux
En examinant des bases de données génétiques publiques et des échantillons sanguins de patients, les chercheurs ont constaté que les niveaux d’ATP6V1B2 étaient systématiquement plus faibles chez les personnes atteintes de MASLD, et encore plus bas chez celles atteintes de cirrhose, une forme sévère de lésion hépatique. Des niveaux réduits d’ATP6V1B2 dans le foie étaient associés à plus d’inflammation, à une fibrose plus marquée et à des marqueurs sanguins d’atteinte hépatique plus élevés. Dans des modèles murins nourris avec des régimes riches en lipides ou déficients en nutriments — des méthodes standard pour reproduire la MASLD — l’apport hépatique en ATP6V1B2 a également diminué. Ces éléments suggèrent que la perte de cette protéine n’est pas qu’un effet secondaire, mais pourrait être étroitement liée à la progression de la maladie.
Ce qui se dérègle dans les cellules hépatiques stressées
Pour savoir ce qui se passe lorsque l’ATP6V1B2 est perturbée, l’équipe a utilisé des cellules hépatiques en culture surchargées d’acides gras, reproduisant un environnement « lipotoxique ». Lorsqu’ils ont réduit artificiellement l’ATP6V1B2, les gouttelettes lipidiques ont grossi, les sous-produits oxydants dangereux ont augmenté et les centrales énergétiques de la cellule (mitochondries) ont commencé à faillir. Les signaux de stress intracellulaires ont grimpé, et une enzyme clé de synthèse lipidique, la synthase des acides gras (FASN), a fortement augmenté. En revanche, lorsque l’ATP6V1B2 était surexpressée, les cellules supportaient mieux la charge lipidique : les gouttelettes lipidiques diminuaient, le stress oxydatif s’atténuait et les mitochondries se rétablissaient. Ces expériences montrent que l’ATP6V1B2 agit comme un frein protecteur contre l’accumulation de lipides et les dommages cellulaires.
Comment un recyclage défaillant favorise l’accumulation de graisse
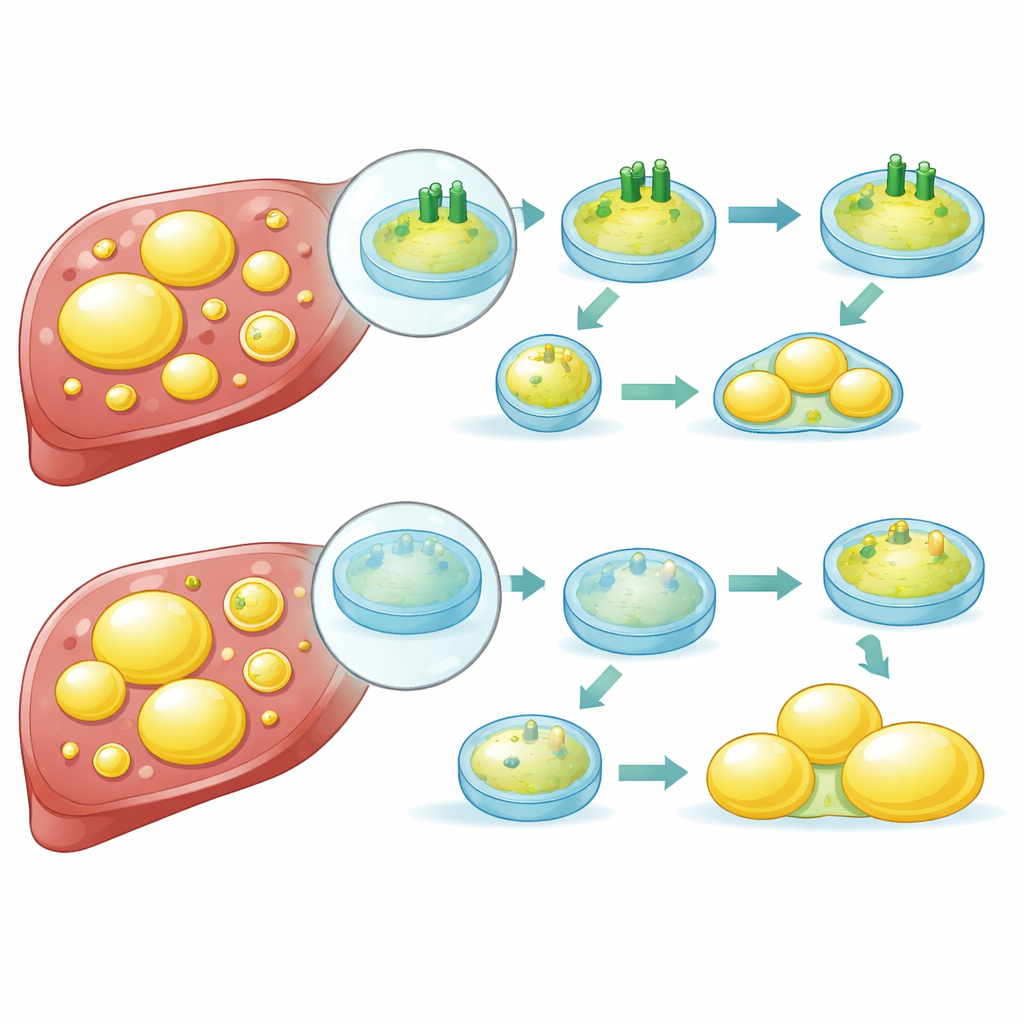
En approfondissant, les chercheurs ont découvert que l’ATP6V1B2 contrôle le degré d’acidité et l’activité des lysosomes. Lorsque la protéine était réduite, les lysosomes perdaient leur acidité, leur capacité à dégrader le contenu diminuait et le flux de matériel dans le système de recyclage cellulaire (autophagie) se trouvait bloqué. En conditions normales, la FASN peut être dirigée vers les lysosomes pour y être détruite. Avec un ATP6V1B2 fonctionnel, cette voie opère efficacement, maintenant les niveaux de FASN sous contrôle et limitant la synthèse lipidique. Mais quand l’ATP6V1B2 vient à manquer, les lysosomes ne peuvent plus dégrader correctement la FASN. L’enzyme s’accumule, la cellule augmente la production de lipides, et les gouttelettes de graisse continuent de croître. L’étude suggère également que les voies de stress intracellulaire augmentent encore la production de FASN lorsque l’ATP6V1B2 est bas, créant un cercle vicieux.
Ce que cela signifie pour les soins futurs
Pour le grand public, le message est simple : une seule protéine qui aide les lysosomes à rester acides peut fortement influencer si les cellules hépatiques stockent ou éliminent les lipides. Des niveaux réduits d’ATP6V1B2, observés chez les patients et dans les modèles de MASLD, affaiblissent le système de recyclage interne du foie, permettant à la graisse et aux lésions de s’accumuler. Mesurer cette protéine dans le sang pourrait aider les médecins à évaluer la gravité de la maladie, et des stratégies qui restaurent l’acidité lysosomale ou renforcent l’activité d’ATP6V1B2 pourraient constituer la base de nouveaux traitements. En mettant en lumière cette « pompe acide » et son contrôle des enzymes de gestion des lipides, l’étude ouvre la voie à des thérapies ciblant les lysosomes pour arrêter ou inverser la maladie du foie gras.
Citation: Xu, R., Yang, F., Zhang, Z. et al. ATP6V1B2 alleviates hepatic steatosis by promoting lysosomal acidification in hepatocytes. Cell Death Discov. 12, 170 (2026). https://doi.org/10.1038/s41420-026-03052-8
Mots-clés: stéatose hépatique, lysosomes, autophagie, métabolisme des lipides, inflammation hépatique