Clear Sky Science · fr
Le contexte épigénétique définit l’activité transcriptionnelle des voies NF-κB canonique et non canonique dans le cancer du pancréas
Pourquoi cette étude importe pour les patient·e·s
Le cancer du pancréas est l’un des cancers les plus mortels, en partie parce que ses cellules sont particulièrement habiles à détecter et à répondre aux signaux de danger dans leur environnement. Cette étude examine deux de ces signaux, appelés TNFα et TWEAK, et montre comment ils activent différents « modes de lecture » dans l’ADN des cellules cancéreuses. Comprendre ces modes pourrait ouvrir de nouvelles voies pour ralentir la croissance tumorale, limiter la dissémination et améliorer l’efficacité des traitements.
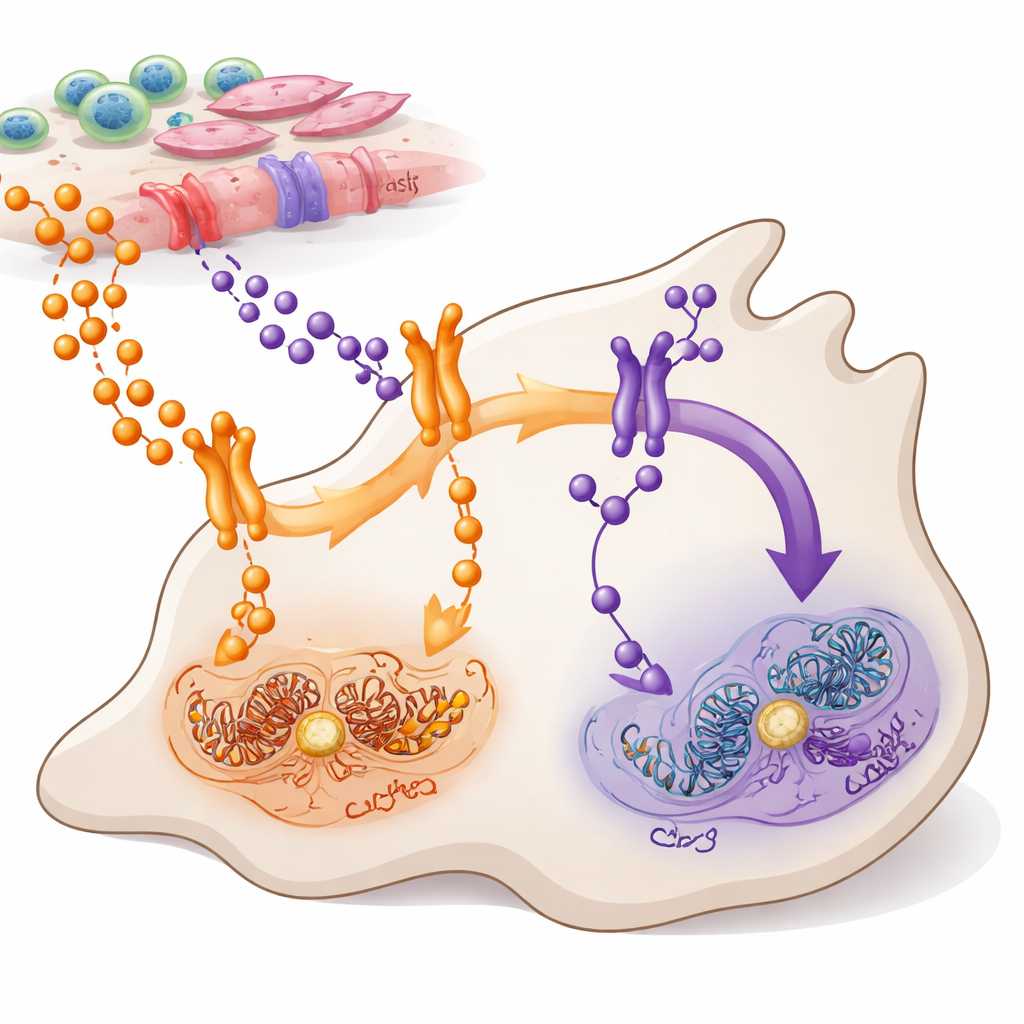
Deux itinéraires de messages vers les cellules cancéreuses
TNFα et TWEAK sont de petits messagers protéiques libérés par les cellules à l’intérieur et autour d’une tumeur. Les deux s’adressent à un système de contrôle majeur à l’intérieur des cellules connu sous le nom de NF-κB, qui contribue à décider si les cellules prolifèrent, se déplacent ou meurent. Les auteurs se sont concentrés sur l’adénocarcinome canalaire pancréatique, la forme la plus courante et la plus agressive du cancer du pancréas, où NF-κB est anormalement actif dans la plupart des tumeurs. Ils ont cartographié quelles cellules produisent TNFα et TWEAK, quelles cellules portent leurs récepteurs, et comment ces signaux circulent à travers deux branches apparentées de NF-κB — souvent appelées voies canonique (via RELA) et non canonique (via RELB).
Qui envoie les signaux dans le voisinage tumoral
En combinant le séquençage d’ARN unicellulaire de milliers de cellules issues de tumeurs de patient·e·s avec de la microscopie avancée, l’équipe a montré que TNFα provient principalement de cellules immunitaires, en particulier des macrophages et de certains lymphocytes T et B. TWEAK, en revanche, est produit par un ensemble plus large : macrophages, fibroblastes, cellules endothéliales et cellules stellaires. Leurs récepteurs diffèrent aussi. Les cellules tumorales et les fibroblastes proches expriment fortement le récepteur principal de TNFα et le récepteur clé de TWEAK. L’analyse des réseaux suggère que la signalisation via TWEAK forme un réseau de communication plus large et plus complexe entre cellules tumorales et cellules de soutien, tandis que la signalisation TNFα est plus concentrée dans les zones riches en cellules immunitaires.
Différents degrés de réponse à l’intérieur des cellules tumorales
Dans des lignées cellulaires de cancer du pancréas, les chercheur·se·s ont traité les cellules par TNFα ou TWEAK et ont mesuré les gènes qui s’activent au fil du temps. TNFα a déclenché une vague rapide et étendue d’activité génique liée à l’inflammation, à la migration cellulaire, au remodelage tissulaire et à la survie. TWEAK a induit un ensemble de changements plus restreint et plus lent qui recouvrait en grande partie les cibles de TNFα plutôt que de lancer un programme unique. Les deux signaux pouvaient favoriser la migration cellulaire et, dans certaines conditions, la mort cellulaire, mais TNFα avait l’effet le plus marqué sur la mobilité. En examinant les données de tumeurs de patient·e·s issues du Cancer Genome Atlas, l’équipe a observé que les tumeurs avec des niveaux élevés de TNFα ou de TWEAK partageaient de nombreux gènes activés, confirmant ces schémas dans des cancers humains réels.
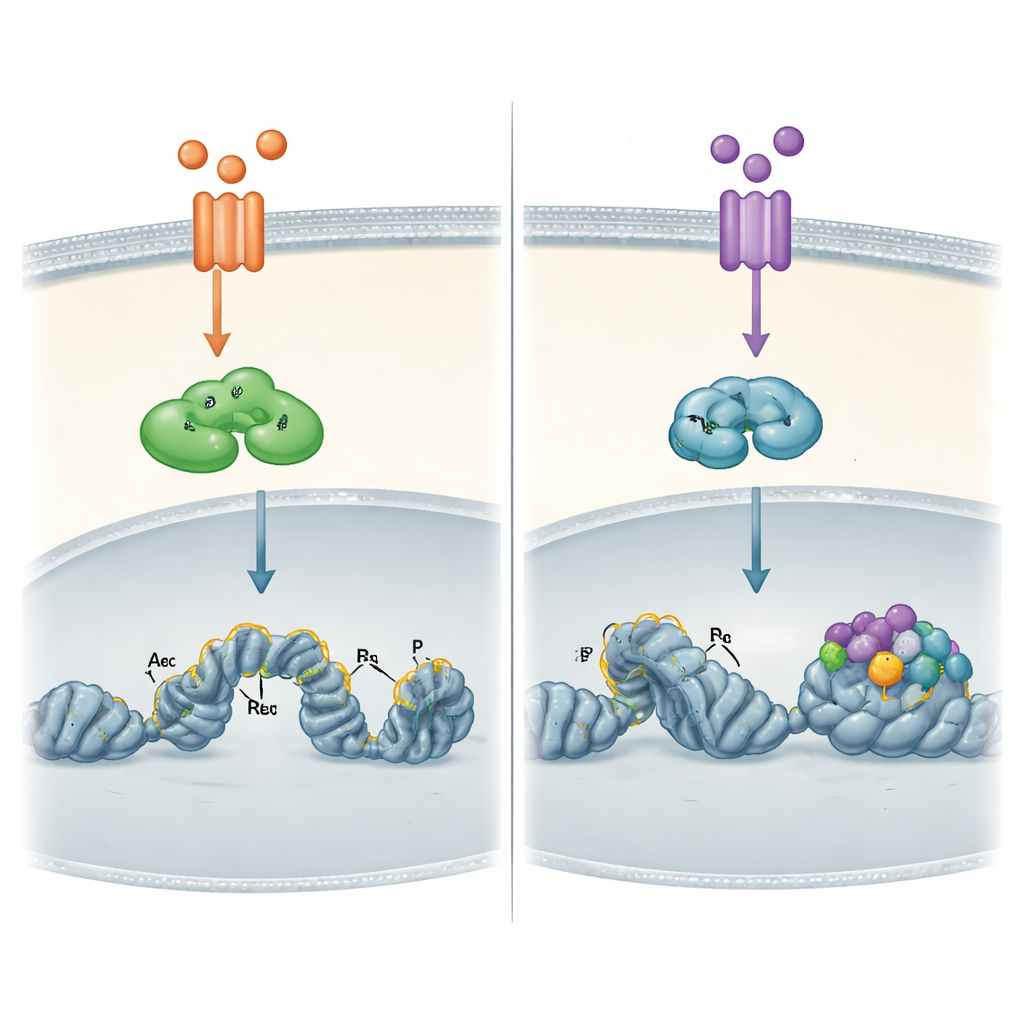
Comment le paysage de l’ADN façonne chaque voie
Les différences les plus marquantes sont apparues lorsque les auteurs ont examiné directement la chromatine des cellules cancéreuses — la forme compacte de l’ADN et de ses protéines associées. À partir de cartes d’occupations à l’échelle du génome, ils ont montré que RELA activé par TNFα peut se lier non seulement à des régions d’ADN déjà ouvertes, mais aussi à des régions plus condensées qu’il aide ensuite à « ouvrir » en ajoutant des marques chimiques associées aux interrupteurs actifs. RELB, activé plus tard par TWEAK, se liait presque exclusivement à des sites déjà accessibles et marqués comme actifs. Ces sites liés par RELB étaient particulièrement riches en motifs d’amarrage pour une autre famille de facteurs, AP-1, ce qui suggère que RELB dépend d’autres protéines pour préparer le terrain avant de pouvoir agir.
Ce que cela implique pour les traitements futurs
Pour un public non spécialiste, l’idée principale est que TNFα et TWEAK utilisent le même ensemble NF-κB de façons très différentes. TNFα, via RELA, agit comme un interrupteur maître capable d’écarter des sections fermées de l’ADN des cellules cancéreuses et d’activer un large éventail de gènes impliqués dans la croissance, la survie et la dissémination. TWEAK, via RELB, ressemble davantage à un spécialiste qui ne peut intervenir que là où l’ADN est déjà ouvert et où des cofacteurs tels qu’AP-1 sont présents. Cette division du travail suggère que des médicaments ciblant le remodelage de la chromatine, AP-1 ou des branches spécifiques de NF-κB pourraient atténuer sélectivement des programmes géniques nuisibles dans le cancer du pancréas tout en préservant d’autres fonctions.
Citation: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Mots-clés: cancer du pancréas, signalisation NF-kappaB, microenvironnement tumoral, régulation épigénétique, TNF et TWEAK