Clear Sky Science · fr
La glutamate décarboxylase 1 (GAD1) freine la progression du glioblastome via la voie GSK3β/β-caténine
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’une des formes de cancer du cerveau les plus mortelles : la plupart des patients survivent à peine un peu plus d’un an après le diagnostic. Les traitements actuels — chirurgie, radiothérapie et chimiothérapie — empêchent rarement la récidive de la maladie. Cette étude explore un allié surprenant déjà présent dans les cellules cérébrales, une enzyme appelée GAD1, et suggère qu’augmenter son activité pourrait ralentir la croissance et la dissémination tumorales.
Un défenseur discret au sein des cellules cérébrales
GAD1 est surtout connu pour son rôle dans les neurones sains, où il contribue à produire le neurotransmetteur apaisant GABA. Les chercheurs se sont demandé si cette enzyme pouvait aussi influencer les tumeurs cérébrales. En comparant des cellules de glioblastome et des cellules gliales normales, ils ont constaté que les niveaux de GAD1 étaient systématiquement plus faibles dans les cellules cancéreuses. De larges bases de données de patients ont confirmé que les tumeurs présentant peu de GAD1 étaient associées à des survies plus courtes, ce qui suggère que GAD1 agit davantage comme un frein que comme un accélérateur dans cette maladie.
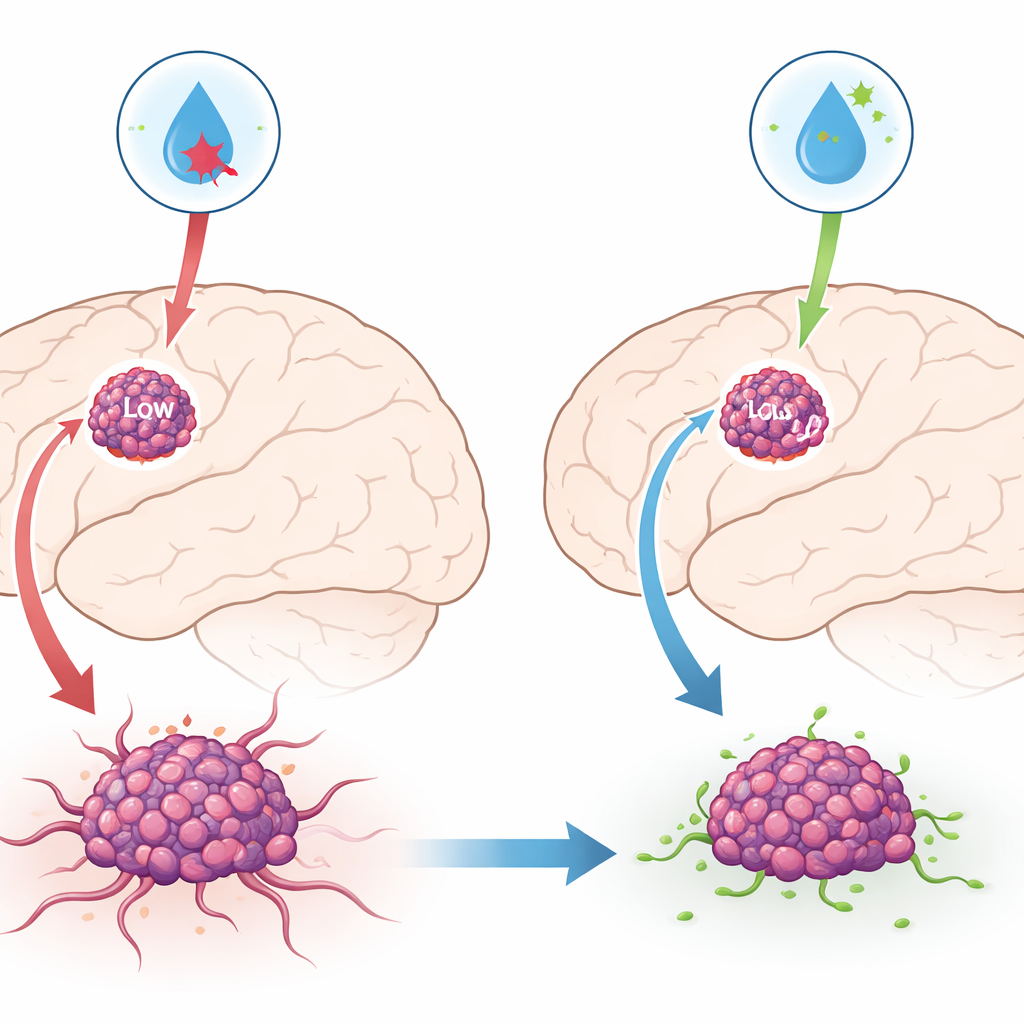
Augmenter ou réduire le frein
Pour tester cette idée, l’équipe a artificiellement augmenté ou diminué les niveaux de GAD1 dans plusieurs lignées cellulaires humaines de glioblastome cultivées en laboratoire. Lorsqu’ils ont sursystématisé GAD1, les cellules tumorales se divisaient plus lentement, formaient moins de colonies, se déplaçaient moins pour combler une entaille dans la culture et avaient des difficultés à envahir un gel mimant le tissu environnant. En réduisant GAD1, l’effet inverse est apparu : les cellules progressaient plus rapidement dans le cycle cellulaire, se propageaient davantage et envahissaient plus profondément. Ces expériences montrent que GAD1 influence fortement l’agressivité des cellules de glioblastome.
Un circuit de contrôle caché au sein de la tumeur
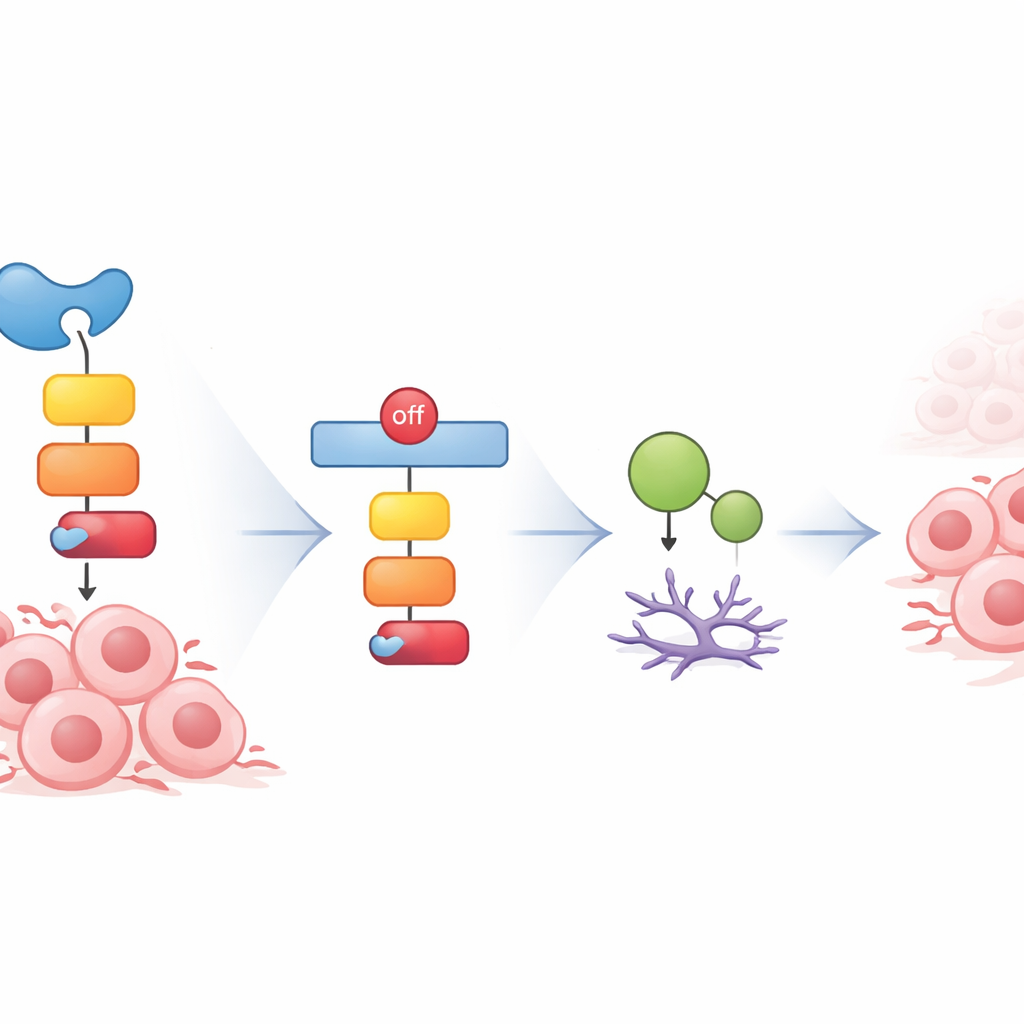
Les scientifiques se sont ensuite demandé comment GAD1 exerce ce contrôle. Ils ont ciblé une voie de signalisation interne centrée sur la protéine GSK3β et un régulateur de croissance bien connu, la β-caténine. Dans de nombreux cancers, lorsque cette voie est fortement active, les cellules se multiplient et envahissent plus facilement. Les chercheurs ont observé que des niveaux plus élevés de GAD1 atténuaient des étapes clés de cette voie et, par conséquent, réduisaient les quantités de deux protéines importantes qui pilotent la progression du cycle cellulaire et l’invasion tissulaire. La diminution de GAD1 activait cette voie, restaurant ces signaux de croissance et d’invasion. Fait intéressant, l’ajout simple de GABA, le produit habituel de GAD1, n’a pas annulé les effets de la perte de GAD1, ce qui implique que l’enzyme influence le comportement tumoral via des rôles supplémentaires, non classiques.
Essais médicamenteux et petits poissons révèlent l’impact in vivo
Parce que les effets de GAD1 transitaient par GSK3β, l’équipe a utilisé une petite molécule inhibitrice de cette kinase pour vérifier si elle pouvait neutraliser l’impact de la perte de GAD1. Dans des cellules de glioblastome à GAD1 réduit, l’inhibiteur a diminué la prolifération, ralenti la progression du cycle cellulaire et réduit l’invasion, tout en abaissant les mêmes protéines en aval liées à la croissance et à la dissémination. Pour aller au‑delà des cultures, les chercheurs ont implanté des cellules tumorales humaines marquées par fluorescence dans des larves de poisson-zèbre transparentes, créant un modèle vivant où la croissance tumorale peut être observée en temps réel. Les tumeurs génétiquement modifiées pour surproduire GAD1 restaient plus petites et les poissons survivaient plus longtemps, tandis que les tumeurs dépourvues de GAD1 croissaient davantage et réduisaient la survie.
Ce que cela peut signifier pour les traitements futurs
Dans l’ensemble, ces résultats présentent GAD1 comme un garde‑fou intégré qui limite le glioblastome en diminuant l’activité d’un circuit puissant de croissance et d’invasion à l’intérieur des cellules tumorales. Lorsque GAD1 est bas, ce circuit fonctionne sans contrôle, contribuant à expliquer pourquoi les patients porteurs de telles tumeurs ont un pronostic plus défavorable. De nombreuses questions demeurent — notamment comment GAD1 se raccorde exactement à l’interrupteur GSK3β — mais ce travail met en lumière GAD1 et sa voie en aval comme des pistes prometteuses pour de nouvelles thérapies. À long terme, des médicaments qui augmentent l’activité de GAD1 ou imitent son influence modulatrice sur ce réseau de signalisation pourraient offrir une nouvelle approche pour ralentir l’un des cancers cérébraux les plus agressifs.
Citation: Zheng, Y., Zhong, Z., Zhang, C. et al. Glutamate decarboxylase 1 (GAD1) suppresses the progression of glioblastoma through GSK3β/β-catenin pathway. Cell Death Discov. 12, 132 (2026). https://doi.org/10.1038/s41420-026-02997-0
Mots-clés: glioblastome, cancer du cerveau, GAD1, signalisation tumorale, modèle de poisson-zèbre