Clear Sky Science · fr
Exploiter la pyroptose dans la thérapie du cancer du sein : mécanismes immunologiques et stratégies émergentes en biomatériaux
Transformer la mort cellulaire en nouvelle arme contre le cancer du sein
Le cancer du sein reste l’un des cancers les plus fréquents et les plus tenaces dans le monde. De nombreuses tumeurs finissent par échapper à la chirurgie, à la chimiothérapie et même aux immunothérapies modernes. Cette revue explore une idée émergente : déclencher délibérément une forme « enflammée » de mort cellulaire, la pyroptose, au sein des tumeurs mammaires. En faisant éclater les cellules cancéreuses de façon contrôlée et inflammatoire, les chercheurs espèrent à la fois tuer directement la tumeur et susciter une réponse immunitaire qui se joindra à l’attaque.
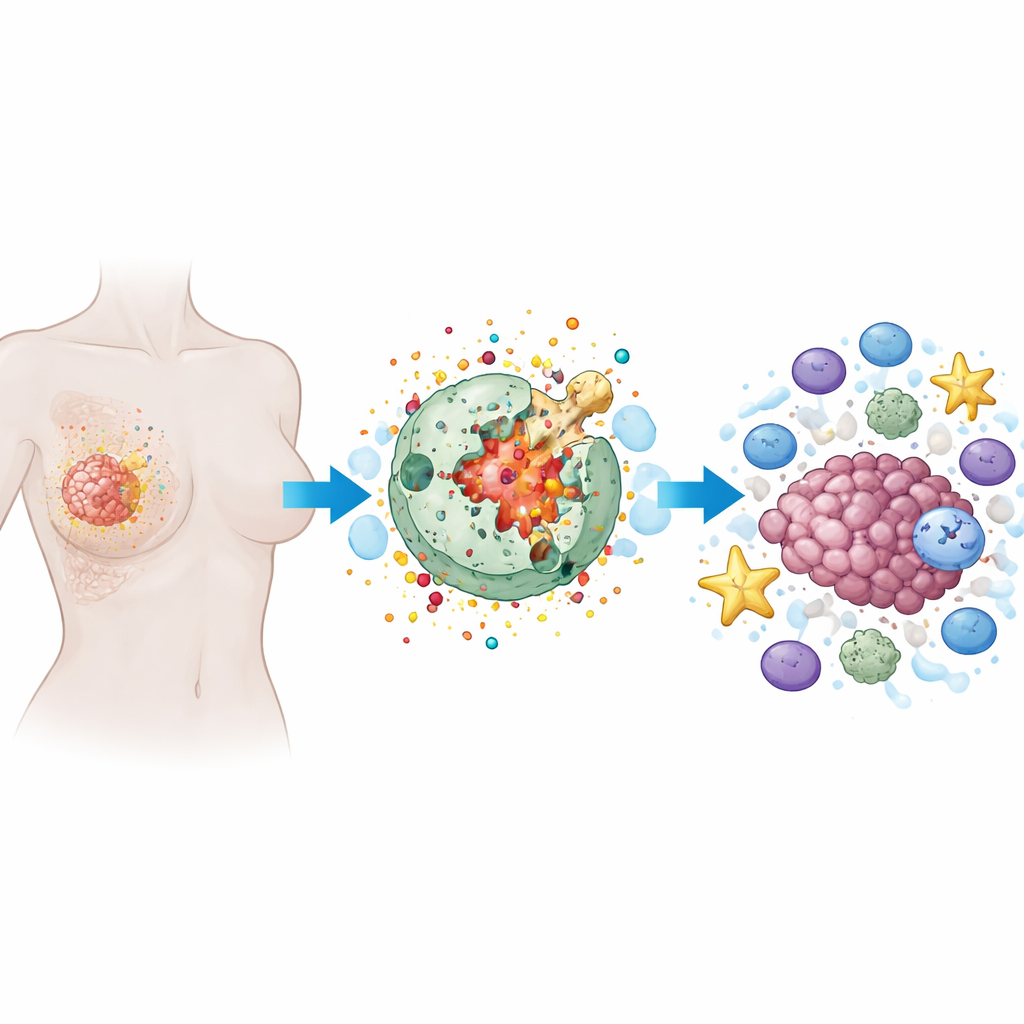
Comment fonctionne cette forme « enflammée » de mort cellulaire
La pyroptose est une forme programmée de mort cellulaire où la cellule gonfle, sa membrane externe se perce de pores, puis se rompt en déversant son contenu. Contrairement à la mort cellulaire calme et ordonnée observée dans de nombreuses thérapies, la pyroptose est bruyante et inflammatoire. Des protéines spécialisées, en particulier une famille appelée gasdermines, agissent comme de petites charges de démolition. Une fois clivées par des enzymes intracellulaires, les gasdermines percent la membrane cellulaire. Cela détruit non seulement la cellule cancéreuse, mais libère aussi des signaux d’alarme et des molécules pro‑inflammatoires capables d’attirer et d’activer les cellules immunitaires.
Pourquoi les tumeurs mammaires posent un défi particulier
Le cancer du sein n’est pas une maladie unique mais un ensemble de sous‑types au comportement différencié. Certains, comme les cancers du sein triple‑négatifs, sont dépourvus de cibles médicamenteuses courantes et résistent souvent aux traitements. Beaucoup de tumeurs mammaires sont dites « immunologiquement froides », c’est‑à‑dire qu’elles contiennent peu de cellules immunitaires actives. La revue explique comment les caractéristiques du microenvironnement tumoral — notamment les cellules stromales, les cellules immunosuppressives et les pénuries locales en oxygène — peuvent à la fois favoriser la pyroptose et, si elle est mal contrôlée, transformer son inflammation en combustible pour la croissance et la dissémination tumorales. Cette double nature en fait un objectif où la précision est essentielle.
Les interrupteurs gasdermine à l’intérieur des cellules tumorales
Un thème central de l’article est la façon dont différentes gasdermines fonctionnent comme des commutateurs moléculaires à l’intérieur des cellules cancéreuses du sein. Des isoformes telles que GSDMD et GSDME peuvent convertir des signaux issus de la chimiothérapie, de la radiothérapie ou d’attaques par des cellules immunitaires en une pyroptose complète. D’autres, comme GSDMC et certaines formes de GSDMB, sont souvent surexprimées dans les tumeurs agressives et peuvent soit promouvoir, soit freiner la maladie selon leur mode d’activation. De nombreux cancers du sein répriment chimiquement GSDME, atténuant ainsi la pyroptose et l’activation immunitaire. Restaurer ou activer sélectivement les gasdermines appropriées pourrait déterminer si une thérapie se contente de tuer quelques cellules ou transforme la tumeur entière en un vaccin in situ qui alerte le système immunitaire.
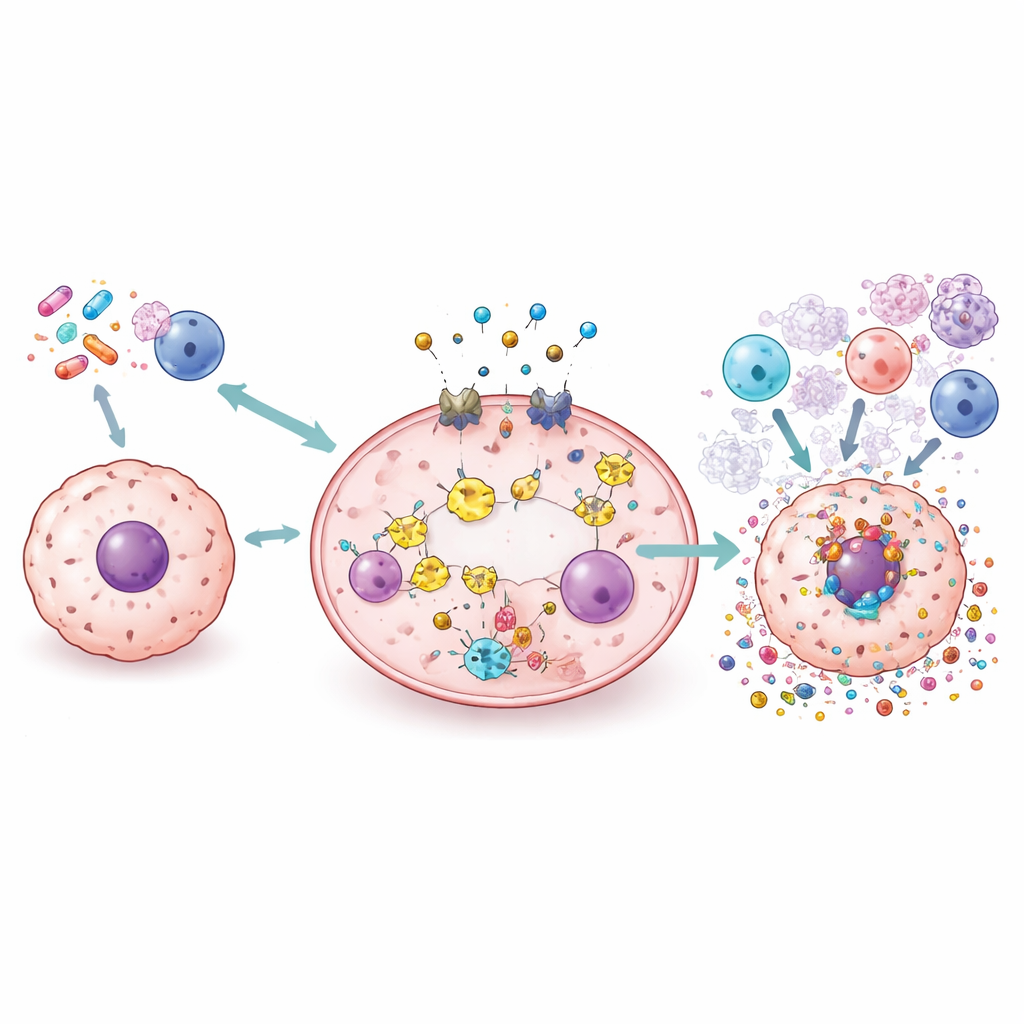
Nouveaux outils : médicaments, nanoparticules, virus et radiations
La revue passe en revue un large éventail de stratégies à l’étude pour exploiter la pyroptose en toute sécurité. Des médicaments classiques comme le cisplatine et la doxorubicine peuvent être réorientés ou reformulés pour pousser les cellules cancéreuses vers un éclatement piloté par les gasdermines plutôt qu’une mort silencieuse. De petites molécules peuvent amplifier ou bloquer des éléments de la voie afin d’ajuster finement l’inflammation. Des nanoparticules et des vecteurs biomimétiques sont conçus pour délivrer la chimiothérapie, des ions cuivre ou des molécules activées par la lumière directement dans les tumeurs, où elles déclenchent la pyroptose tout en épargnant les tissus sains. Des virus oncolytiques et la radiothérapie peuvent également être ingénierés ou combinés à d’autres agents pour provoquer la pyroptose et remodeler le paysage immunitaire tumoral, rendant potentiellement les inhibiteurs de points de contrôle immunitaire plus efficaces.
Concilier bénéfice puissant et risques réels
Parce que la pyroptose est très inflammatoire, les mêmes réactions qui aident le système immunitaire à combattre le cancer peuvent aussi endommager les tissus normaux ou même favoriser la croissance tumorale si elles deviennent chroniques. Les auteurs mettent en avant des biomarqueurs précoces — tels que des signatures géniques, des schémas de méthylation, des fragments de protéines gasdermine dans le sang et des profils de cytokines — qui pourraient aider à identifier les patients susceptibles de bénéficier et ceux exposés à un risque élevé de « tempêtes de cytokines » dangereuses. Des conceptions avancées en nanomédecine, des combinaisons médicamenteuses soigneusement choisies et une surveillance en temps réel des marqueurs inflammatoires sont explorées pour garder la réponse efficace mais contrôlée.
Ce que cela pourrait signifier pour les patients à venir
En termes simples, cette revue soutient que faire « mourir bruyamment » les cellules cancéreuses pourrait transformer la prise en charge du cancer du sein. En déclenchant la pyroptose dans un sous‑ensemble précis de cellules tumorales, les cliniciens pourraient à la fois réduire la tumeur et réveiller une réponse immunitaire puissante et durable, transformant des tumeurs froides en tumeurs chaudes plus réceptives aux immunothérapies modernes. Pourtant, la pyroptose est une alliée volatile : si elle est libérée trop largement ou trop longtemps, elle peut aggraver l’inflammation ou favoriser l’émergence de cellules résistantes. Les recherches futures se concentreront sur l’identification des patients bénéficiaires, la perfection des systèmes de délivrance ciblés et la conduite d’essais cliniques associant des approches inductrices de pyroptose à des médicaments immunitaires. Si ces défis sont relevés, exploiter la pyroptose pourrait ajouter une dimension puissante et nouvelle au traitement du cancer du sein.
Citation: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Mots-clés: pyroptose, cancer du sein, gasdermine, microenvironnement tumoral, nanomédecine