Clear Sky Science · fr
Dynamique absolue et statique relative : la relation entre la glycolyse et l’OXPHOS dans le développement du cancer
Pourquoi les choix énergétiques du cancer comptent
Les cellules cancéreuses ressemblent à des athlètes d’endurance extrêmes : elles doivent constamment s’alimenter pour croître, se propager et échapper aux traitements. Cette revue explique comment les cellules tumorales exploitent deux systèmes énergétiques principaux — l’un rapide et l’autre efficace — et, surtout, comment elles les mélangent et les intervertissent. Comprendre ces stratégies énergétiques changeantes offre une nouvelle perspective pour diagnostiquer et traiter le cancer sur l’ensemble du cours de la maladie.
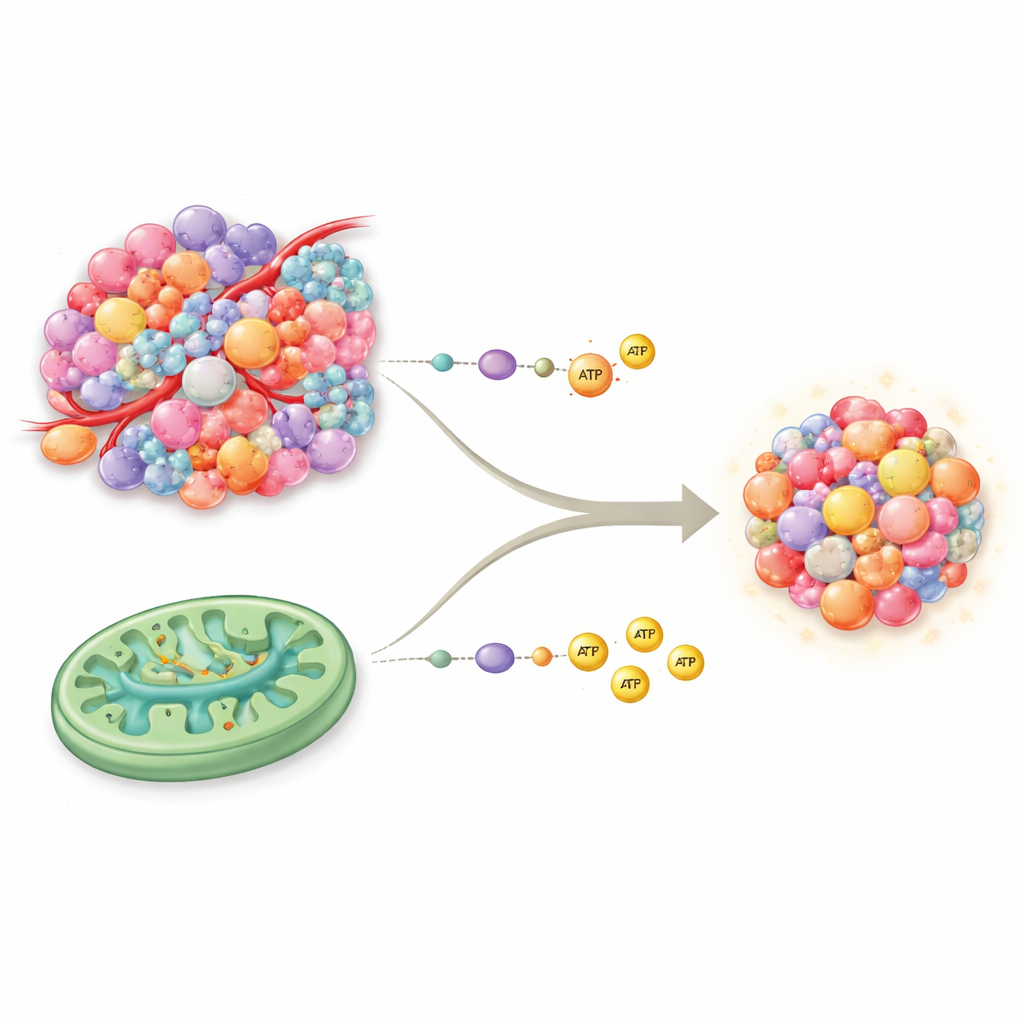
Deux principales voies de production d’énergie
Nos cellules produisent généralement de l’énergie par deux voies centrales. La glycolyse est le système rapide, « liquidités immédiates », qui dégrade le sucre rapidement mais produit relativement peu d’énergie par unité. La phosphorylation oxydative, ou OXPHOS, fonctionne à l’intérieur des mitochondries et ressemble davantage à une centrale à haute efficacité : elle génère beaucoup plus d’énergie mais requiert un bon apport en oxygène et en nutriments. Pendant des décennies, on a pensé que le cancer reposait presque exclusivement sur la glycolyse, même en présence d’oxygène — un schéma connu sous le nom d’effet Warburg. De nouvelles preuves renversent cette vision simpliste : de nombreuses tumeurs possèdent des mitochondries pleinement fonctionnelles et peuvent utiliser l’OXPHOS et le cycle des acides tricarboxyliques (TCA) parallèlement à la glycolyse, leur fournissant un éventail énergétique plus riche et plus flexible qu’on ne le pensait.
Plusieurs types cellulaires, plusieurs choix énergétiques
Une tumeur n’est pas une masse homogène. C’est un petit écosystème contenant des cellules cancéreuses, des cellules de soutien, des vaisseaux sanguins et des cellules immunitaires, chacune ayant des besoins énergétiques distincts. Certaines cellules cancéreuses vivent près des vaisseaux sanguins et bénéficient d’un apport abondant en oxygène et en nutriments ; d’autres sont enfouies dans des régions mal irriguées. En conséquence, des cellules d’une même tumeur peuvent privilégier la glycolyse, dépendre principalement de l’OXPHOS, ou utiliser les deux simultanément. Cette diversité métabolique — appelée hétérogénéité — découle de différences de flux sanguin, de niveaux de nutriments, de types cellulaires et de signaux de l’environnement environnant. De plus, les tumeurs présentent souvent une symbiose métabolique : les cellules glycolytiques exportent du lactate comme produit apparemment résiduel, que les cellules voisines dépendantes de l’OXPHOS importent et oxydent comme carburant précieux. Un partage similaire du lactate a lieu entre les cellules cancéreuses et les cellules de soutien telles que les fibroblastes, les cellules vasculaires et les cellules immunosuppressives, contribuant collectivement à la prospérité de la tumeur et à sa résistance aux thérapies.
En perpétuel changement : comment l’énergie tumorale évolue dans le temps
Le métabolisme tumoral n’est pas seulement divers à un instant donné ; il est aussi hautement dynamique. À mesure que les tumeurs croissent, elles rencontrent des conditions changeantes telles que l’hypoxie, l’accumulation d’acide, la pénurie de nutriments et des variations de la rigidité des tissus. Dans des conditions difficiles et pauvre en oxygène, de nombreuses cellules cancéreuses se tournent vers la glycolyse. En cas d’accumulation d’acide ou de privation de sucre, elles peuvent basculer vers un recours accru à l’OXPHOS. La même flexibilité se manifeste lors de jalons biologiques clés. Les cellules en division rapide s’appuient sur la glycolyse pour générer les blocs de construction nécessaires à la synthèse d’ADN, de lipides et de membranes. Les cellules au repos ou circulantes dans le sang dépendent souvent davantage de l’OXPHOS. Lors de l’invasion et de la métastase, les cellules cancéreuses ajustent à plusieurs reprises leur choix de carburant : certaines étapes favorisent la glycolyse, d’autres l’OXPHOS, et les cellules métastatiques qui colonisent de nouveaux organes adaptent leur métabolisme au « sol » du tissu de destination.
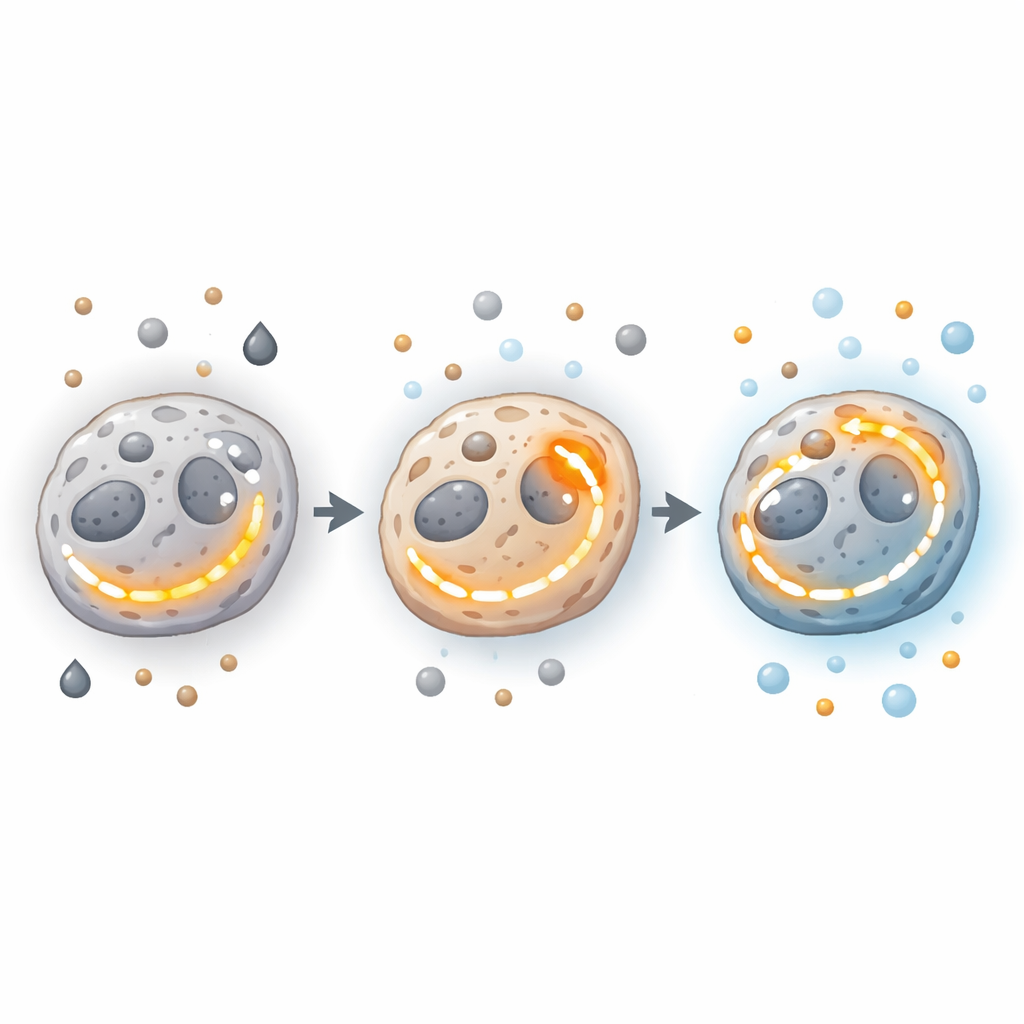
Gènes, enzymes et « centrales » derrière la bascule
Au cœur de la machinerie cellulaire, gènes et enzymes orientent ces décisions énergétiques. Oncogènes et suppresseurs de tumeurs peuvent pousser les cellules vers la glycolyse ou l’OXPHOS, ou leur permettre d’intensifier les deux. Des mutations ou des altérations d’enzymes clés du TCA, comme celles impliquées dans la gestion du citrate, du succinate ou de l’isocitrate, peuvent faire pencher la balance et parfois activer des signaux favorisant le cancer tels que l’angiogenèse et l’invasion. Des enzymes situées à des carrefours cruciaux — comme la pyruvate kinase M2, qui aide à décider si le carbone dérivé du sucre sert à l’énergie ou à la synthèse de constituants — relient la glycolyse et la fonction mitochondriale. Parallèlement, des différences dans le nombre, la structure et la performance des mitochondries selon les régions tumorales élargissent encore le spectre des états énergétiques possibles.
Repenser le traitement autour d’une cible énergétique mouvante
Parce que les cellules tumorales peuvent basculer entre glycolyse et OXPHOS, bloquer une seule voie suffit rarement ; le cancer peut rediriger son usage de carburant et survivre. Les auteurs soutiennent que le métabolisme énergétique tumoral n’est stable que brièvement et qu’il est fondamentalement et constamment changeant. Ils proposent d’envisager les tumeurs à travers un « spectre du métabolisme énergétique » qui doit être mesuré au fil du temps, et non pas une seule fois. En pratique, cela pourrait signifier suivre les préférences énergétiques d’une tumeur au cours des différentes étapes de la maladie et associer, de manière personnalisée, des inhibiteurs de la glycolyse et de l’OXPHOS. De telles stratégies thérapeutiques dynamiques guidées par le métabolisme pourraient mieux couper l’alimentation de la tumeur, limiter sa capacité d’adaptation et améliorer le contrôle à long terme de la maladie.
Citation: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Mots-clés: métabolisme du cancer, glycolyse, phosphorylation oxydative, microenvironnement tumoral, plasticité métabolique