Clear Sky Science · fr
Le S100A9 exosomal favorise les métastases pulmonaires du carcinome adénoïde kystique en activant les fibroblastes associés au cancer
Comment un cancer salivaire silencieux gagne les poumons
Le carcinome adénoïde kystique est un cancer à croissance lente mais tenace qui débute souvent dans les glandes salivaires et réapparaît plus tard dans les poumons, parfois des années après l’ablation de la tumeur initiale. Pour les patients et leurs proches, cette dissémination différée est effrayante et difficile à prévoir ou à prévenir. Cette étude décrypte la manière dont les cellules de ces tumeurs préparent discrètement le tissu pulmonaire distant à l’invasion cancerogène, révélant une conversation cachée entre les cellules tumorales et les cellules de soutien environnantes qui pourrait enfin offrir de nouvelles cibles thérapeutiques.
Un cancer qui persiste et revient
Le carcinome adénoïde kystique (CAK) est un cancer des glandes de la tête et du cou, en particulier des glandes salivaires. La chirurgie et la radiothérapie contrôlent souvent la tumeur principale, mais de nombreux patients développent finalement des métastases pulmonaires, principale cause de décès. Les traitements disponibles pour les formes disséminées de CAK restent limités, en partie parce que les mécanismes permettant aux cellules de la tumeur d’origine de s’implanter et de proliférer dans les poumons ne sont pas entièrement compris. Les auteurs de cet article ont cherché à identifier les signaux clés qui permettent aux cellules de CAK de remodeler leur environnement et de créer un « sol » favorable pour de futures tumeurs pulmonaires.
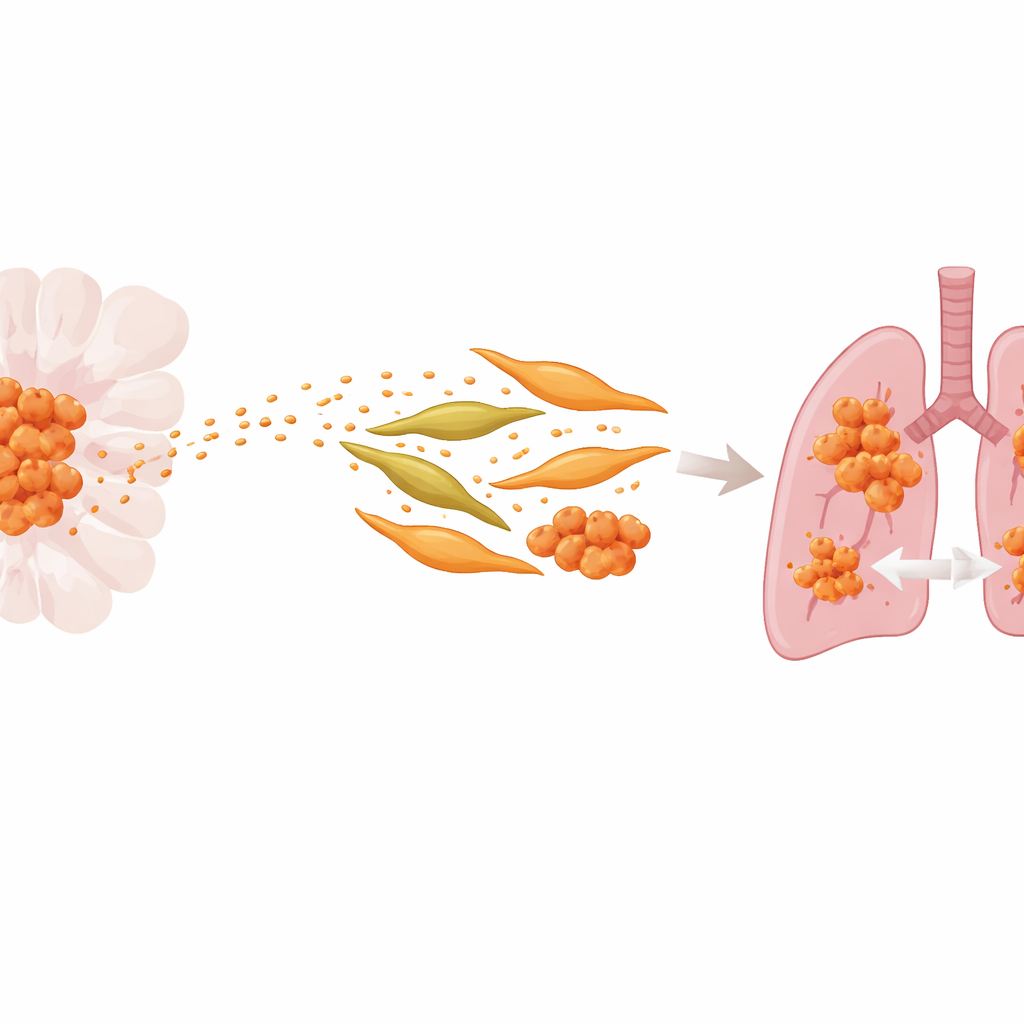
De minuscules colis à fort impact
Les chercheurs se sont intéressés aux exosomes, de petites vésicules membranaires que les cellules cancéreuses libèrent dans le sang. Ces vésicules transportent des protéines et du matériel génétique capables de reprogrammer des cellules à distance. En comparant une lignée cellulaire standard de CAK à une version sélectionnée pour sa forte capacité à coloniser les poumons, l’équipe a constaté que les cellules agressives et leurs exosomes étaient enrichis en une protéine nommée S100A9, liée à l’inflammation. Les patients dont les tumeurs et les exosomes sanguins contenaient davantage de S100A9 avaient plus de chances de développer des métastases pulmonaires et des périodes sans récidive plus courtes, ce qui suggère que cette protéine favorise la dissémination du cancer.
Reprogrammer l’équipe de soutien de la tumeur
À l’aide du séquençage ARN unicellulaire, les auteurs ont construit une carte détaillée de tous les types cellulaires présents dans les tumeurs de CAK et les glandes normales adjacentes. Ils ont découvert une communication intense entre les cellules épithéliales tumorales et les fibroblastes voisins, ces cellules structurelles qui produisent le tissu conjonctif. Dans le cancer, ces fibroblastes peuvent être « recrutés » et transformés en fibroblastes associés au cancer (CAF), qui rigidifient les tissus, alimentent l’inflammation et aident les cellules tumorales à migrer. L’étude montre que les exosomes riches en S100A9 issus de cellules de CAK agressives peuvent convertir des fibroblastes normaux en CAF activés : ceux-ci deviennent plus contractiles, plus mobiles et commencent à produire des enzymes et des molécules inflammatoires qui remodèlent la matrice tissulaire et favorisent la croissance tumorale.
De signaux locaux à des colonies pulmonaires
L’équipe a ensuite examiné si ces fibroblastes activés par des exosomes facilitaient effectivement la colonisation pulmonaire par le CAK. Chez la souris, l’injection d’exosomes chargés en S100A9 dans la circulation a préparé les poumons : les fibroblastes pulmonaires ont exprimé des marqueurs d’activation et le tissu pulmonaire a commencé à produire des facteurs associés à la néovascularisation et à la dégradation de la matrice. Quand des cellules de CAK ont été introduites par la suite, les souris prétraitées avec des exosomes S100A9 ont développé davantage et de plus grandes métastases pulmonaires. Des analyses complémentaires ont montré que ce processus dépendait d’une chaîne de signaux inflammatoires centrée sur le messager IL-17, ainsi que TNF et NF-κB, qui amplifiaient ensemble l’activation des fibroblastes et remodelaient le microenvironnement pulmonaire.
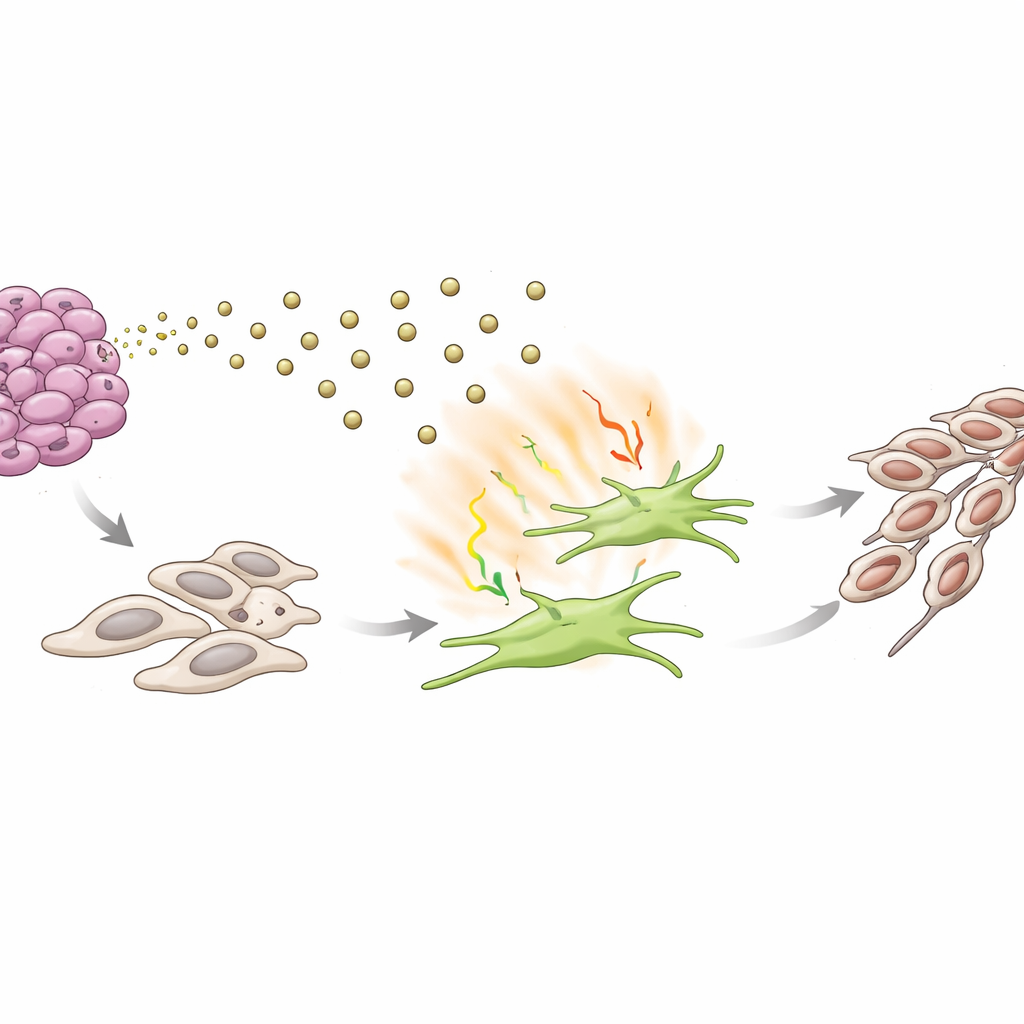
Un cercle vicieux qui favorise la transformation du cancer
Dans des systèmes de co-culture en laboratoire, les fibroblastes « éduqués » par des exosomes riches en S100A9, ou par la voie de signalisation pilotée par IL-17, rendaient les cellules de CAK avoisinantes plus agressives. Les cellules tumorales devenaient meilleures pour se déplacer, envahir des barrières, former des colonies et adopter une morphologie plus mobile et fusiforme associée à une transition épithélio-mésenchymateuse, étape clé vers la métastase. Bloquer IL-17 avec un anticorps neutralisant inversait nombre de ces changements, tandis que l’ajout d’IL-17 pur à lui seul poussait les cellules de CAK vers cet état plus invasif. Ensemble, ces résultats décrivent une boucle autorenforçante : les cellules tumorales envoient S100A9 dans des exosomes pour activer les fibroblastes ; les fibroblastes activés libèrent IL-17 et d’autres signaux qui, à leur tour, rendent les cellules tumorales plus enclines à se disséminer.
Rompre la boucle de communication cachée
Pour un non-spécialiste, le message est que la dissémination du CAK vers les poumons n’est pas due au hasard. Au contraire, la tumeur d’origine prépare secrètement les cellules de soutien et les tissus distants pour faciliter sa croissance ailleurs, en utilisant de petits colis protéiques comme messagers. Ce travail identifie S100A9 et la voie de signalisation en aval impliquant IL-17 comme des carrefours centraux de ce processus. En ciblant cet axe de communication — en bloquant S100A9, en atténuant la signalisation IL-17 ou en perturbant l’activation des fibroblastes — des thérapies futures pourraient interrompre cette « phase de préparation » des métastases pulmonaires, offrant de nouvelles stratégies pour empêcher ce cancer discret mais dangereux de réapparaître loin de son point de départ.
Citation: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
Mots-clés: carcinome adénoïde kystique, exosomes, fibroblastes associés au cancer, métastases pulmonaires, axe S100A9 IL-17