Clear Sky Science · fr
La transition endothéliale-mésenchymateuse médiée par APOA2 et le reprogrammation du métabolisme lipidique tumoral confèrent une résistance aux antiangiogéniques via le TGF-β
Pourquoi cette découverte importe pour les patients
Les médecins utilisent de plus en plus des médicaments qui affament les tumeurs hépatiques en coupant leur apport sanguin, mais de nombreux patients voient leur cancer cesser de répondre après un bénéfice initial. Cette étude pose une question cruciale : pourquoi certains cancers du foie deviennent-ils résistants à ces traitements qui bloquent les vaisseaux sanguins, et comment pourrions-nous les contourner ? Les chercheurs mettent au jour un partenariat insoupçonné entre une protéine sanguine liée aux lipides et un puissant signal de croissance, qui permet aux tumeurs de reconfigurer à la fois leurs vaisseaux et leur utilisation de l’énergie, indiquant une voie alternative pour traiter un cancer difficile à guérir.
Une tumeur qui apprend à vivre sans son habituel câble d’alimentation
Le carcinome hépatocellulaire, forme la plus fréquente de cancer du foie, dépend fortement de la néo-vascularisation pour croître. Les traitements standard pour les formes avancées visent à bloquer une voie clé de formation vasculaire centrée sur le VEGF et son récepteur VEGFR2. Pourtant, chez de nombreux patients, les tumeurs prospèrent malgré ces médicaments. En comparant des échantillons tumoraux de patients ayant répondu ou non à l’antiangiogénique apatinib, les auteurs ont identifié un gène marquant : APOA2. Les tumeurs résistantes présentaient des niveaux nettement plus élevés d’APOA2, une protéine surtout connue pour son rôle dans le transport des lipides dans le sang. Cela a suggéré qu’APOA2 pourrait aider les tumeurs à échapper aux traitements ciblant les vaisseaux.
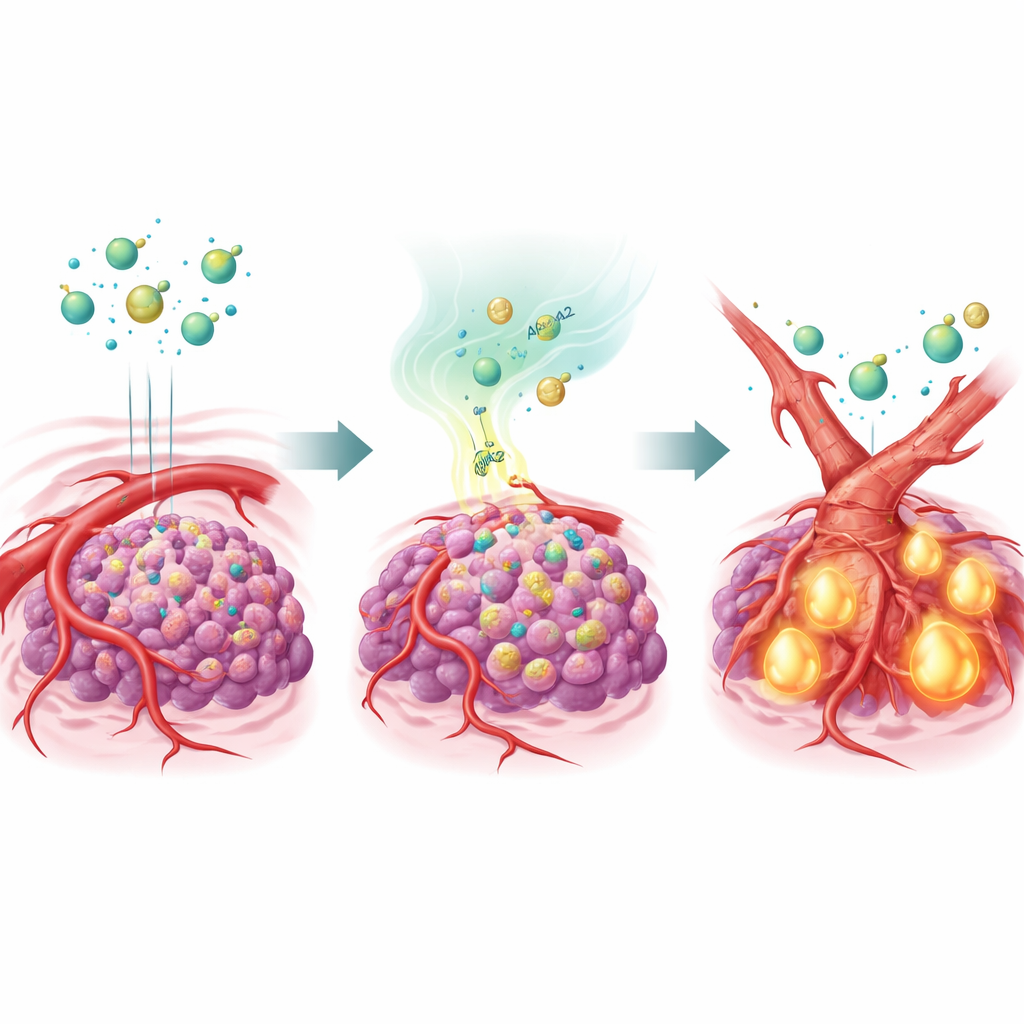
Une protéine de transport des lipides qui remodèle les vaisseaux
Pour tester cette hypothèse, l’équipe a modifié des cellules de cancer du foie pour qu’elles produisent beaucoup d’APOA2, puis les a implantées chez la souris. Lors du traitement par plusieurs antiangiogéniques, ces tumeurs riches en APOA2 ont largement ignoré la thérapie : leurs vaisseaux ont persisté et les cancers ont continué de croître. Des analyses détaillées ont montré qu’un signal maître, le TGF-β, était fortement activé dans ces tumeurs, avec des niveaux augmentés à la fois dans le microenvironnement tumoral et dans le sang des animaux. Le TGF-β a agi sur les cellules qui bordent les vaisseaux, les poussant à changer d’identité par un processus appelé transition endothéliale-mésenchymateuse. En évoluant vers un état plus cicatriciel, mésenchymateux, ces cellules ont perdu une grande partie de leur VEGFR2, la cible même des antiangiogéniques. En pratique, les vaisseaux se sont remodelés en une forme que les médicaments ne pouvaient plus atteindre.
Une déviation métabolique qui maintient l’alimentation des cellules cancéreuses
L’histoire ne s’est pas arrêtée à la paroi vasculaire. Le même signal TGF-β, induit par APOA2, a aussi reprogrammé la façon dont les cellules tumorales se procurent de l’énergie. Plutôt que de compter principalement sur la dégradation du glucose, les cellules riches en APOA2 ont commencé à capter davantage d’acides gras libres de leur environnement et à les brûler dans leurs mitochondries par oxydation des acides gras. Des expériences mesurant l’usage des nutriments et la consommation d’oxygène ont montré que ces cellules devenaient plus dépendantes des lipides comme source d’énergie et produisaient plus d’ATP. Ce basculement a permis aux cellules tumorales de continuer à se diviser rapidement et d’éviter la mort cellulaire, même lorsque l’apport sanguin était mis sous pression par le traitement antiangiogénique.
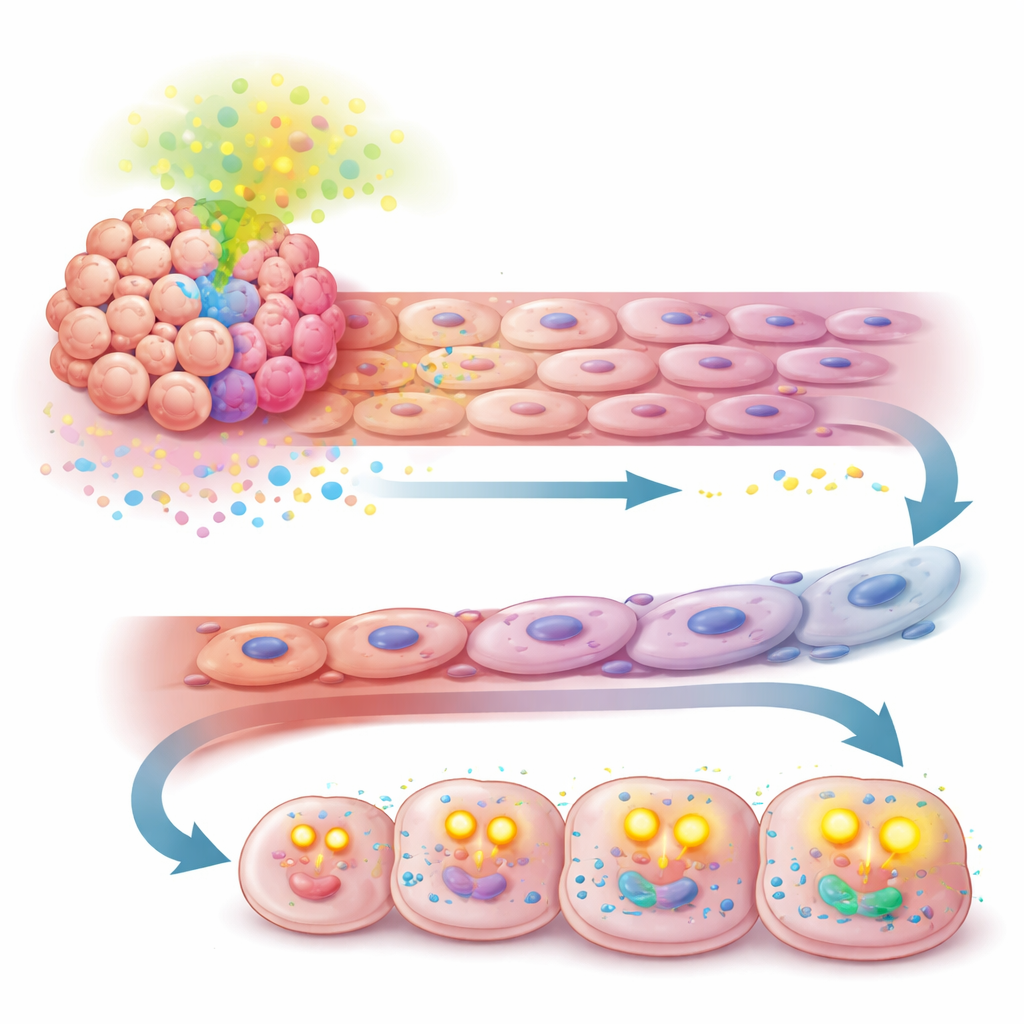
Transformer une faiblesse en nouvelle cible thérapeutique
De façon cruciale, lorsque les chercheurs ont bloqué le TGF-β, les avantages conférés par APOA2 se sont effondrés. Inhiber ce signal dans des modèles murins a réduit les changements vasculaires anormaux, restauré la sensibilité à la thérapie et ralenti la croissance tumorale. Encore plus prometteur, un anticorps bifonctionnel bloquant simultanément le TGF-β et le point de contrôle immunitaire PD-1 a mieux fonctionné que chaque approche prise isolément dans les tumeurs à forte expression d’APOA2. Ces résultats suggèrent que, dans un sous-ensemble de cancers du foie marqués par une forte APOA2, la maladie a discrètement changé sa dépendance de la voie VEGF habituelle vers une route centrée sur le TGF-β qui soutient à la fois les vaisseaux et le métabolisme tumoral.
Ce que cela signifie pour la prise en charge future du cancer du foie
Pour un non-spécialiste, le message clé est que certaines tumeurs hépatiques échappent aux médicaments anti-vaisseaux actuels en reconfigurant à la fois leur plomberie et leur source d’énergie. Une protéine associée aux lipides, APOA2, amplifie le signal TGF-β, qui à son tour masque les vaisseaux pour que les médicaments existants ne puissent plus les cibler et apprend aux cellules cancéreuses à vivre des lipides plutôt que du sucre. L’étude suggère que le dosage d’APOA2 dans les tumeurs pourrait identifier les patients peu susceptibles de bénéficier des antiangiogéniques standard mais susceptibles de répondre à des médicaments bloquant le TGF-β, en particulier en combinaison avec l’immunothérapie moderne. En bref, en révélant comment les tumeurs s’adaptent, ce travail pointe vers une stratégie plus personnalisée qui attaque à la fois les vaisseaux et la source d’énergie sur laquelle ces cancers résistants comptent.
Citation: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Mots-clés: carcinome hépatocellulaire, résistance aux antiangiogéniques, APOA2, signalisation TGF-bêta, métabolisme lipidique du cancer