Clear Sky Science · fr
L’irisine inhibe la différenciation adipogénique des cellules souches mésenchymateuses de la moelle osseuse via l’axe de signalisation SIRT1/RANBP2/FTO et protège contre l’ostéoporose
Pourquoi une hormone musculaire compte pour des os fragiles
L’ostéoporose semble souvent n’être qu’un problème d’« os faibles », mais au cœur de notre squelette se joue une lutte silencieuse. Les mêmes cellules souches de la moelle osseuse peuvent devenir soit des cellules formant l’os, soit des adipocytes. En vieillissant, et particulièrement après la ménopause, cet équilibre bascule vers la formation de graisse, laissant les os plus fins et plus susceptibles de se fracturer. Cette étude examine comment une hormone libérée par les muscles lors de l’exercice, appelée irisine, peut repousser ces cellules souches vers la formation osseuse plutôt que la formation de graisse, ouvrant la voie à l’idée qu’une hormone liée à l’activité physique pourrait à l’avenir contribuer à protéger contre l’ostéoporose.
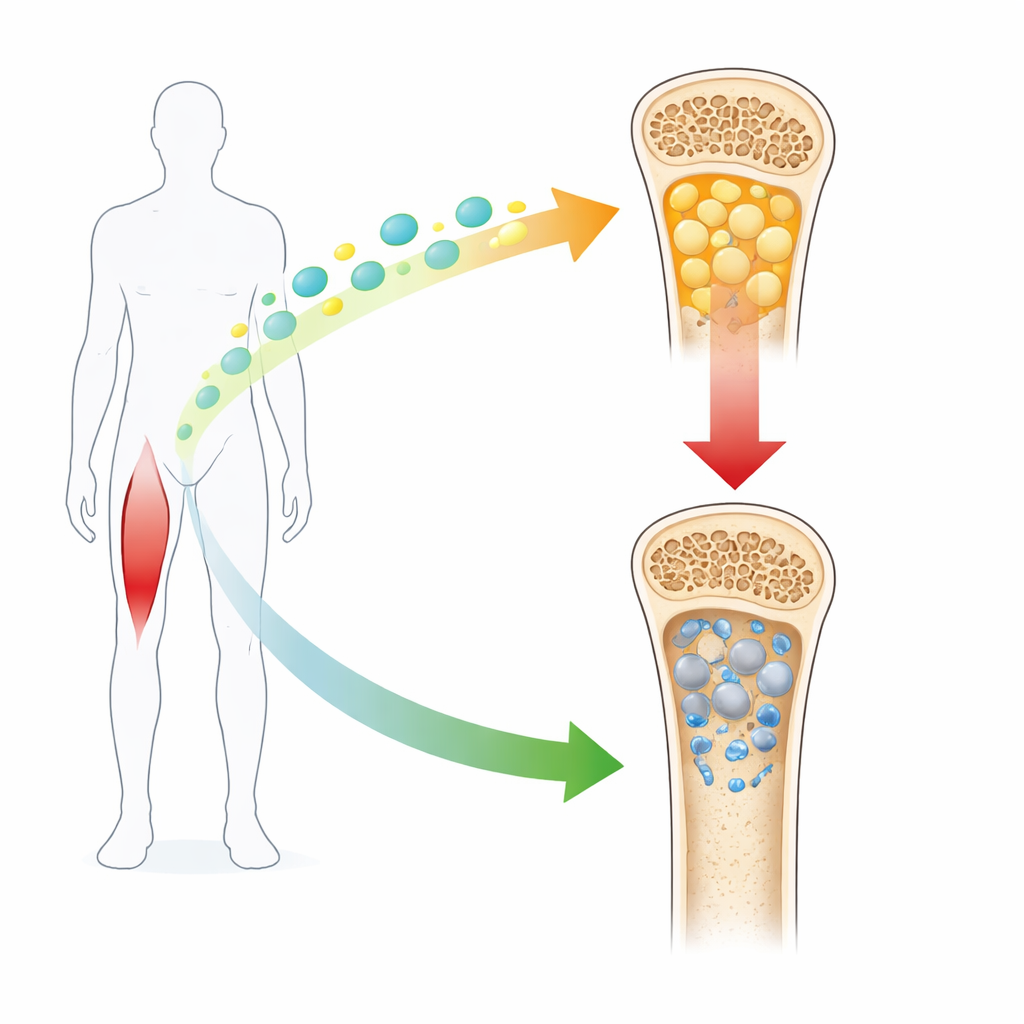
Quand l’os se transforme en graisse
La moelle osseuse n’est pas une cavité vide mais un atelier animé de cellules souches qui peuvent choisir des destins différents. Chez les adultes en bonne santé, suffisamment de ces cellules deviennent des bâtisseurs d’os pour maintenir un squelette solide. Dans l’ostéoporose, surtout chez les femmes postménopausées, davantage de ces cellules se convertissent en adipocytes stockant la graisse. Cette « obésité de la moelle osseuse » va de pair avec des os fragiles et des fractures. Les chercheurs ont commencé par confirmer que ce basculement vers la graisse s’accompagne de niveaux réduits d’irisine, aussi bien chez des souris privées d’estrogènes que chez des patientes humaines atteintes d’ostéoporose, reliant la chute de cette hormone à une détérioration de la santé osseuse.
Un signal lié à l’exercice avec un double rôle
L’irisine est libérée par les muscles pendant l’activité physique et a été étudiée pour ses effets sur le métabolisme et l’utilisation d’énergie. Ici, l’équipe a cherché à savoir si l’irisine aide aussi à décider si les cellules souches de la moelle osseuse deviennent graisse ou os. En culture, ils ont ajouté de l’irisine à des cellules souches de moelle osseuse de souris et observé les effets. L’irisine a renforcé la capacité des cellules à se différencier en ostéoblastes, augmentant les dépôts minéraux et l’activité de gènes clés de l’os. Parallèlement, elle a fortement supprimé leur transformation en adipocytes, réduisant les gouttelettes lipidiques et abaissant l’expression de gènes et de protéines qui pilotent la formation de graisse. Chez des souris ovariectomisées pour reproduire la perte osseuse postménopausique, des injections hebdomadaires d’irisine ont préservé la masse et la microarchitecture osseuses et réduit l’accumulation de graisse dans la cavité médullaire.
Dans la machinerie décisionnelle de la cellule
Pour comprendre comment l’irisine exerce ce contrôle, les chercheurs ont analysé les changements d’activité génique lorsque les cellules souches étaient exposées à l’irisine durant la formation de graisse. Un acteur remarquable fut SIRT1, une protéine connue pour réguler le vieillissement, le métabolisme et les réponses au stress. L’équipe a montré que diminuer SIRT1 rendait les cellules plus susceptibles de devenir des adipocytes, tandis qu’augmenter SIRT1 avait l’effet inverse. De manière importante, lorsque SIRT1 était réduit, l’irisine ne pouvait plus bloquer efficacement la formation de graisse, ni in vitro ni chez la souris, révélant que SIRT1 est un relais clé du signal protecteur de l’irisine sur l’os.
Une chaîne moléculaire qui désarme une protéine « graisse »
En approfondissant, l’étude s’est intéressée à une autre protéine, FTO, liée à l’obésité et au stockage lipidique. Des niveaux élevés de FTO favorisent le développement des adipocytes, en partie en stabilisant un régulateur majeur de la graisse appelé PPARγ. Les chercheurs ont constaté que SIRT1 ne modifiait pas la production de FTO au niveau génique, mais influençait plutôt la stabilité de la protéine FTO. L’activation de SIRT1 par l’irisine augmentait l’activité d’une troisième protéine, RANBP2, qui étiquette FTO d’une manière favorisant sa dégradation. Lorsque RANBP2 était réduit, SIRT1 ne pouvait plus diminuer les niveaux de la protéine FTO, et la formation de graisse réapparaissait. Par cette chaîne — irisine vers SIRT1, SIRT1 vers RANBP2, et RANBP2 vers la dégradation de FTO — les cellules se détournent de la voie adipogénique pour revenir vers un destin ostéogénique.
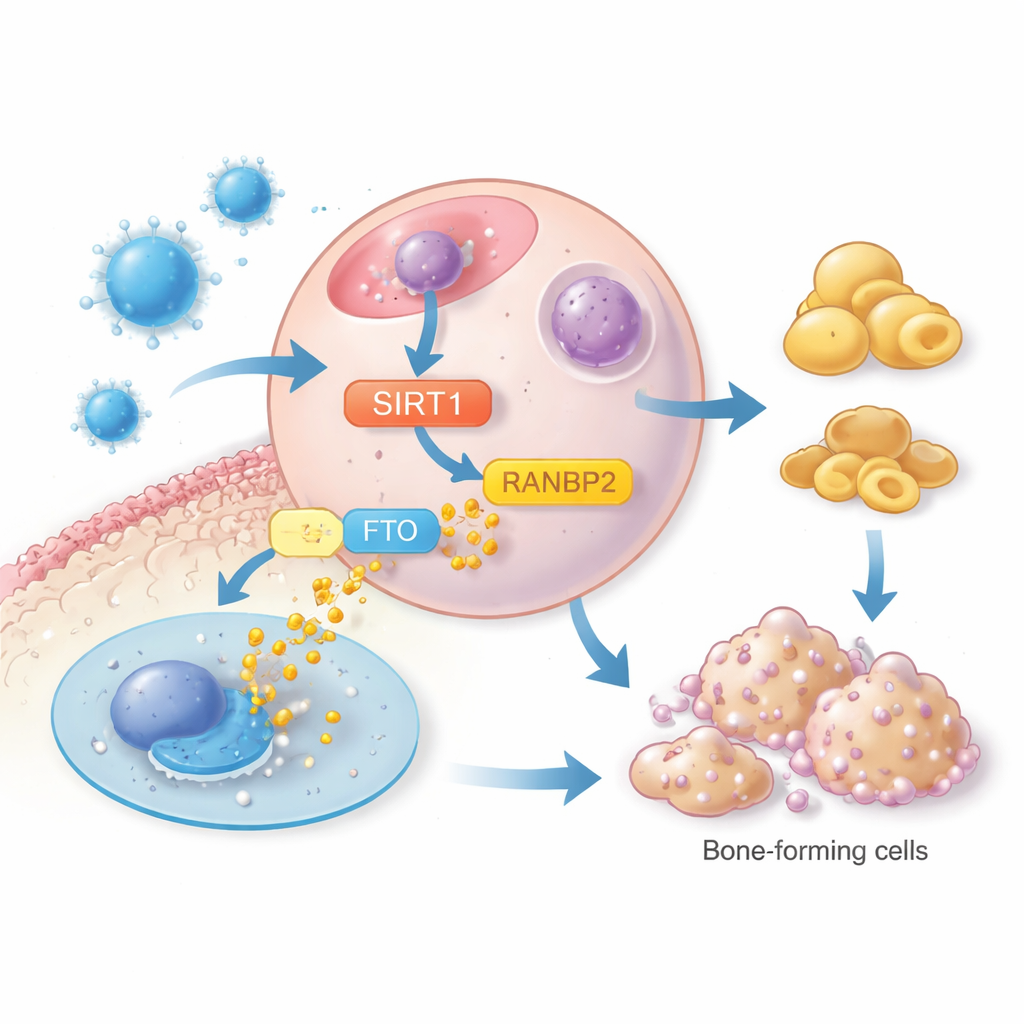
Ce que cela pourrait signifier pour la prise en charge future des os
En retraçant cette voie par étapes, l’étude révèle l’irisine comme plus qu’une simple hormone de l’exercice. Elle agit comme un agent molecular dans la moelle osseuse, orientant les cellules souches loin de la transformation en graisse et vers la construction osseuse, via un axe de signalisation SIRT1–RANBP2–FTO. Pour le grand public, cela signifie que maintenir ou imiter le signal naturel de l’irisine pourrait un jour devenir une stratégie pour prévenir ou traiter l’ostéoporose, en complément des mesures de style de vie comme l’exercice. Bien que des études humaines plus larges soient encore nécessaires, ces résultats pointent vers un nouveau jeu de cibles moléculaires prometteuses pour conserver des os plus solides plus longtemps.
Citation: Chen, J., Liu, J., Fu, Q. et al. Irisin inhibits adipogenic differentiation of bone marrow mesenchymal stem cells through the SIRT1/RANBP2/FTO signaling axis and protects against osteoporosis. Cell Death Discov. 12, 114 (2026). https://doi.org/10.1038/s41420-026-02976-5
Mots-clés: ostéoporose, irisine, cellules souches de la moelle osseuse, équilibre os-graisse, signalisation SIRT1