Clear Sky Science · fr
KCTD1 stabilise c-Myc pour augmenter PD-L1 et supprimer l’immunité anti-tumorale dans le carcinome hépatocellulaire
Pourquoi cela compte pour les soins oncologiques futurs
Beaucoup de personnes atteintes d’un cancer du foie ne bénéficient pas des immunothérapies les plus prometteuses d’aujourd’hui, conçues pour libérer les cellules T du patient contre les tumeurs. Cette étude examine pourquoi une forme majeure de cancer du foie, le carcinome hépatocellulaire, peut encore échapper à l’attaque immunitaire même pendant le traitement — et identifie un nouvel interrupteur moléculaire, nommé KCTD1, qui pourrait améliorer l’efficacité des médicaments d’immunothérapie existants.
Un assistant caché des « arrêts » tumoraux
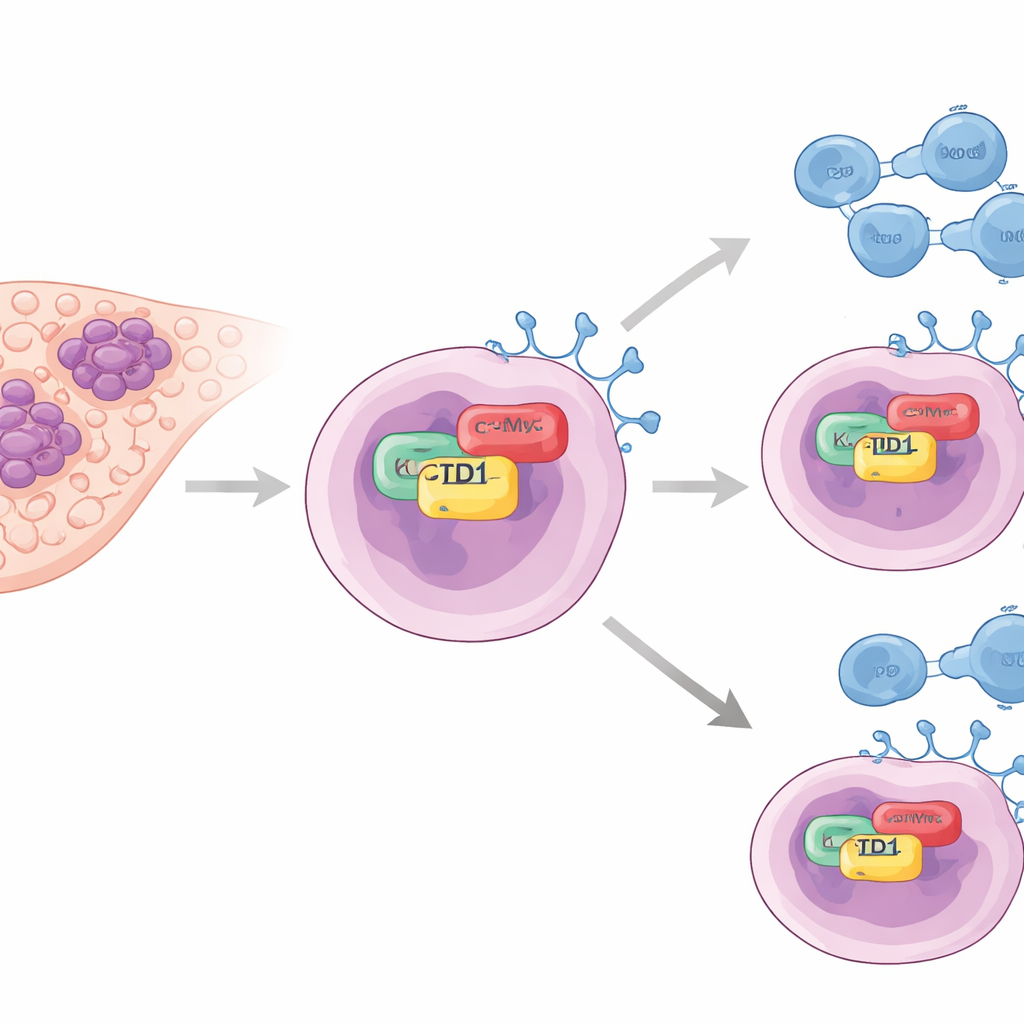
Les auteurs se sont concentrés sur une protéine nommée KCTD1, auparavant liée à la croissance tumorale hépatique mais peu étudiée pour l’échappement immunitaire. Dans des échantillons tumoraux de patients, ils ont constaté que les niveaux de KCTD1 étaient nettement plus élevés dans le tissu hépatique cancéreux que dans le foie normal. Fait important, les tumeurs riches en KCTD1 présentaient aussi des taux élevés de PD-L1, une protéine de surface des cellules cancéreuses qui se lie à PD-1 sur les cellules T et indique au système immunitaire de se retirer. Les patients dont les tumeurs avaient moins de KCTD1 avaient tendance à vivre plus longtemps, ce qui suggère que cette protéine est liée à la fois à la gravité de la maladie et à la force du bouclier immunitaire tumoral.
Relier les points moléculaires à l’intérieur des cellules cancéreuses
Pour comprendre comment KCTD1 augmente PD-L1, l’équipe s’est tournée vers des lignées cellulaires de cancer du foie cultivées en laboratoire. Lorsqu’ils ont réduit KCTD1, les niveaux de la protéine PD-L1 ont diminué et le PD-L1 restant s’est dégradé plus rapidement, indiquant que KCTD1 aide à stabiliser PD-L1 plutôt que de simplement activer son gène. À l’aide d’expériences biochimiques d’affinité et de microscopie à fluorescence, ils ont montré que KCTD1 se lie physiquement à un autre acteur clé du cancer, l’oncoprotéine c-Myc, dans le noyau cellulaire. Cette interaction se produit via des régions de contact spécifiques sur les deux protéines et conduit à une plus grande stabilité de c-Myc, ce qui à son tour augmente la production de PD-L1. Lorsque c-Myc seul était réduit, PD-L1 chutait même si KCTD1 était abondant, plaçant c-Myc comme le maillon central crucial de la chaîne KCTD1–c-Myc–PD-L1.
Réanimer les cellules T en laboratoire
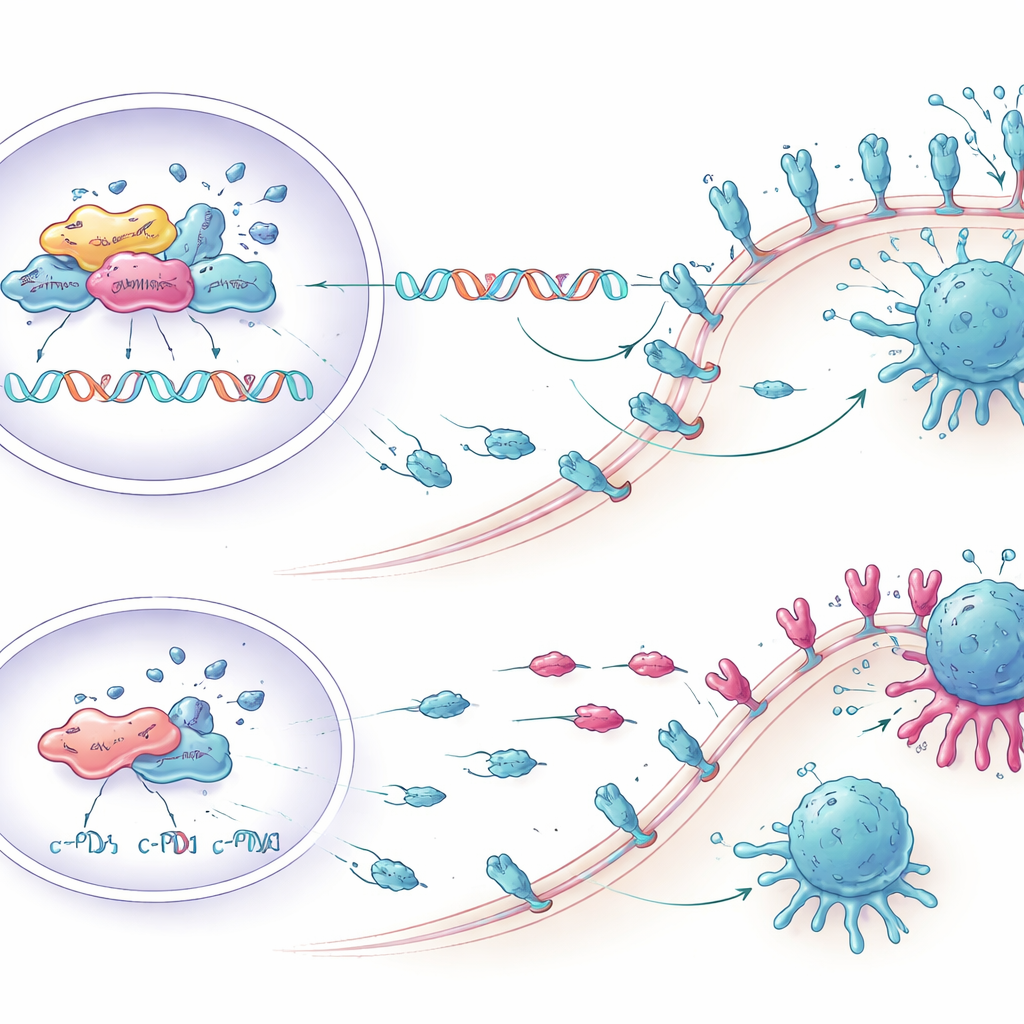
Les chercheurs ont ensuite demandé si la diminution de KCTD1 pouvait réellement renforcer l’attaque immunitaire. Ils ont co-cultivé des cellules de cancer du foie humain avec des cellules immunitaires prélevées sur des donneurs sanguins. Les cellules tumorales conçues pour exprimer moins de KCTD1, et donc moins de PD-L1, ont déclenché des réponses plus fortes des cellules T CD8 — les principaux effecteurs cytotoxiques du système immunitaire contre les cellules cancéreuses. Un plus grand nombre de ces cellules T ont produit des molécules inflammatoires telles que le TNF-α et l’interféron‑gamma, ont montré des marqueurs accrus de prolifération et d’activation, et présentaient moins de signes d’épuisement. En conséquence, davantage de cellules tumorales ont subi une mort cellulaire programmée lorsque KCTD1 était supprimé, démontrant que les changements moléculaires se traduisaient par de réels gains en matière de destruction immunitaire.
Tester le mécanisme chez la souris
Pour vérifier si le même schéma s’applique chez des organismes vivants, l’équipe a implanté des cellules de cancer hépatique de souris dépourvues de KCTD1 directement dans le foie de rongeurs. Les tumeurs avec KCTD1 réduit formaient moins de nodules et de plus petite taille, présentaient une division cellulaire plus lente et un nombre accru de cellules tumorales en cours de mort. Ces tumeurs exprimaient également moins de c-Myc et de PD-L1. L’élimination des cellules T CD8 chez les souris annulait en grande partie cet avantage, indiquant que le ralentissement tumoral dépendait fortement de l’activité des cellules T. Enfin, lorsque les chercheurs ont combiné l’extinction de KCTD1 avec un anticorps anti‑PD‑1 — un médicament existant ciblant les points de contrôle immunitaires — les souris présentaient la plus faible charge tumorale et les niveaux les plus élevés de cellules T CD4 et CD8 infiltrant leurs tumeurs.
Ce que cela pourrait signifier pour les patients
Dans l’ensemble, ces travaux révèlent KCTD1 comme un coordinateur central qui stabilise c-Myc, augmente PD-L1 à la surface des cellules hépatiques cancéreuses et affaiblit l’attaque des cellules T CD8. Perturber cette voie rend les tumeurs à la fois plus vulnérables au système immunitaire et plus réceptives aux médicaments bloquant PD-1 chez la souris. Pour les patients, cela suggère que des médicaments visant KCTD1 ou sa surface de contact avec c-Myc pourraient, à l’avenir, être associés aux immunothérapies actuelles pour permettre à davantage de personnes atteintes d’un cancer du foie de bénéficier d’un contrôle immunitaire durable de leur maladie.
Citation: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Mots-clés: carcinome hépatocellulaire, immunothérapie tumorale, voie PD-1 PD-L1, signalisation c-Myc, immunité antitumorale des cellules T