Clear Sky Science · fr
Une approche multi-omique révèle l’hétérogénéité et des populations fonctionnelles de cellules progénitrices oligodendrocytaires induites par des cellules souches neuronales humaines
Pourquoi protéger l’isolation du cerveau est important
Le câblage du cerveau dépend d’un enrobage graisseux appelé myéline, qui entoure les fibres nerveuses comme l’isolation autour des câbles électriques. Lorsque la myéline est endommagée, comme dans la sclérose en plaques et d’autres troubles, les signaux ralentissent ou échouent, entraînant des problèmes de mouvement, de vision et de pensée. Cette étude examine un groupe particulier de cellules humaines capables de reconstruire la myéline et pose une question pratique : quelles cellules sont les mieux adaptées pour de futures thérapies cellulaires visant à réparer cette isolation cruciale ?
Des cellules souches initiales aux fabriques de myéline
Les chercheurs ont commencé avec des cellules souches neuronales humaines — des cellules initiales polyvalentes issues de tissus cérébraux fœtaux déjà engagées à devenir des cellules du système nerveux. Ils ont progressivement orienté ces cellules en laboratoire pour les convertir en cellules progénitrices oligodendrocytaires, ou hOPC, qui sont les précurseurs directs des cellules productrices de myéline. Au microscope, les cellules sont passées de formes rondes simples à des morphologies plus complexes à multiples branches, et elles ont activé des protéines caractéristiques marquant des étapes vers des cellules matures productrices de myéline. Cela a fourni une source fiable et relativement sûre de précurseurs humains formant la myéline pour une analyse détaillée.
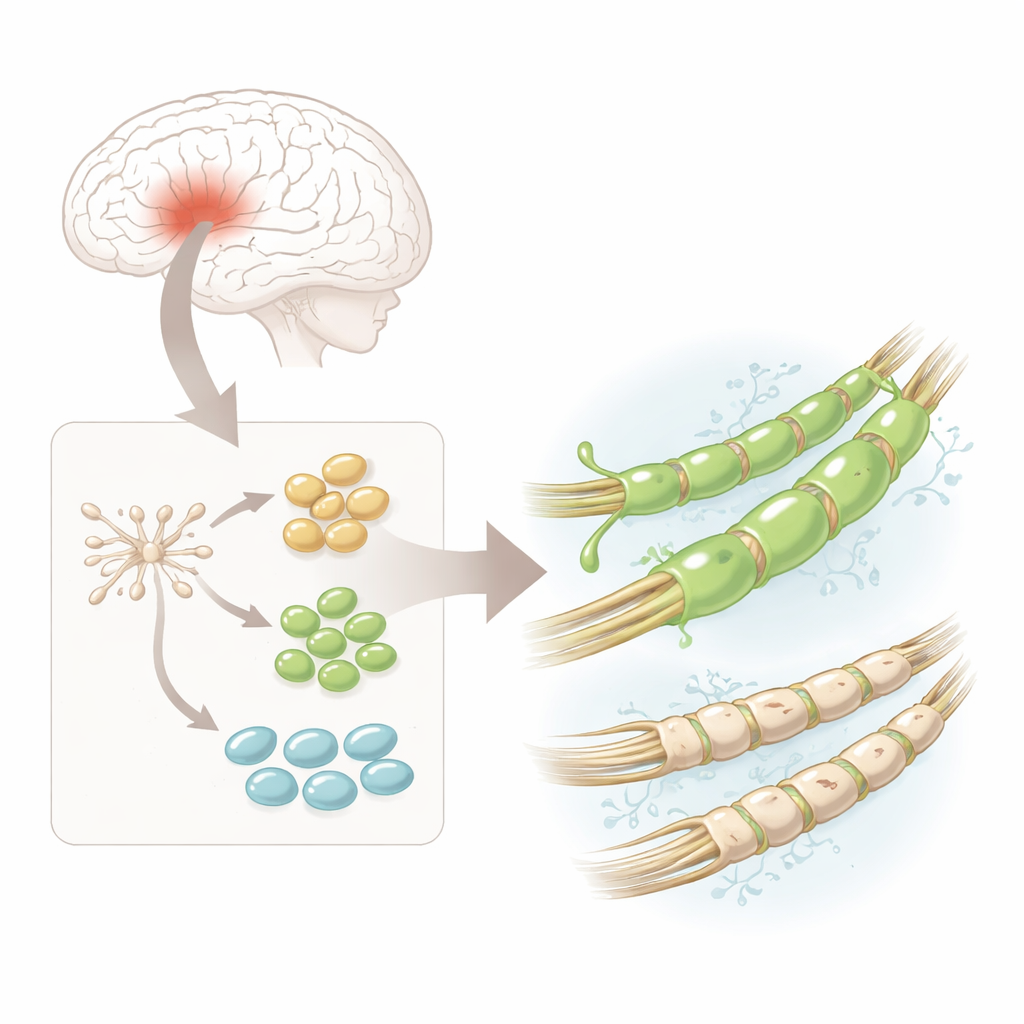
Une seule catégorie cellulaire, de nombreuses variantes cachées
Grâce au séquençage ARN unicellulaire — une méthode qui lit quels gènes sont actifs dans des milliers de cellules individuelles — l’équipe a découvert que les hOPC n’étaient pas toutes identiques. Elles se répartissaient en trois stades principaux : des « pré-progéniteurs » précoces, des progéniteurs plus engagés et des cellules approchant l’identité complète d’oligodendrocytes. À tous ces stades, un gène se distinguait : PDGFRA, qui code pour un récepteur à la surface cellulaire. Une méthode d’imagerie très sensible appelée RNA-Scope a confirmé que l’ARNm et la protéine de PDGFRA étaient plus abondants que d’autres marqueurs clés à chaque stade, suggérant que ce récepteur pourrait définir des cellules particulièrement capables de fabriquer la myéline.
Identifier les cellules de réparation les plus puissantes
Pour tester cette idée, les scientifiques ont séparé les hOPC en deux groupes selon la présence du récepteur PDGFR-α à leur surface. Ils ont ensuite comparé les cellules PDGFR-α–positives, les cellules PDGFR-α–négatives et des cellules non triées dans une série de tests fonctionnels. Lorsqu’elles ont été transplantées chez des souris « shiverer » — incapables de former une myéline normale — les cellules PDGFR-α–positives ont produit une myéline plus dense et plus compacte autour des fibres nerveuses que les autres groupes. Ces cellules ont aussi migré plus loin et proliféré plus rapidement dans des essais en laboratoire. Autrement dit, la population PDGFR-α–positive était la plus vigoureuse pour se déplacer vers l’endroit nécessaire, augmenter en nombre et reconstruire l’isolation.
Les signaux internes qui stimulent croissance et réparation
En creusant davantage, l’équipe a comparé l’activité génique entre cellules PDGFR-α–positives et –négatives. Ils ont constaté que les cellules positives activaient des réseaux de gènes impliqués dans la croissance gliale et la formation de myéline, ainsi que plusieurs voies de signalisation intracellulaire clés. Deux voies se détachaient en particulier : PI3K–AKT–mTOR, longtemps associée à la croissance cellulaire et à la production de myéline, et la signalisation TGF-β, qui influence le choix du destin des jeunes cellules cérébrales. Les données suggèrent que l’activation de PDGFR-α s’alimente dans PI3K–AKT–mTOR, qui à son tour renforce les signaux liés à TGF-β, poussant ensemble les cellules vers un devenir d’assembleurs de myéline efficaces.
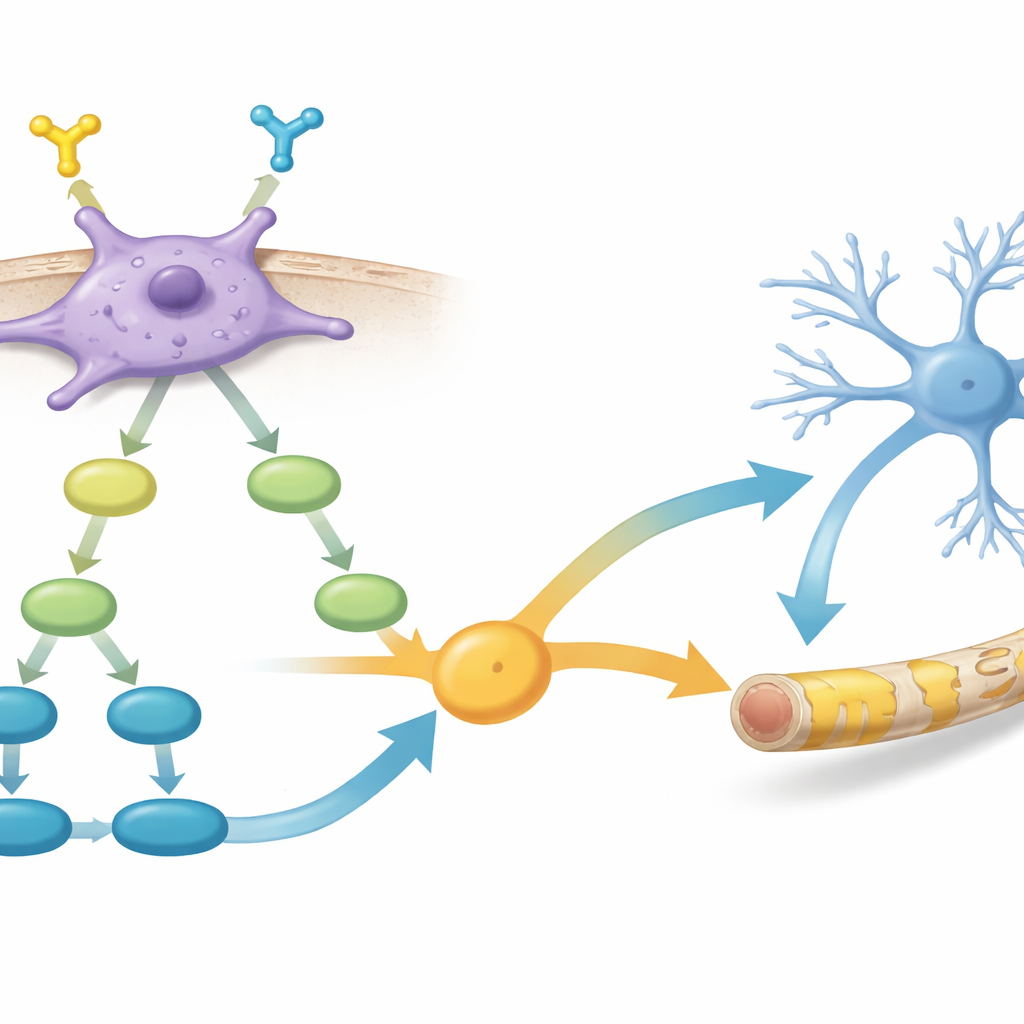
Renforcer la réparation de la myéline avec un adjuvant chimique
Les chercheurs ont ensuite cherché à savoir s’ils pouvaient améliorer encore ces cellules prometteuses. Ils ont traité les hOPC PDGFR-α–positives avec une petite molécule activant la voie TGF-β et ont examiné à la fois l’activité génique et le comportement. Après traitement, ces cellules présentaient des niveaux plus élevés de plusieurs gènes liés à la myéline et produisaient des gaines de myéline plus épaisses et plus complètes lorsqu’elles ont été transplantées dans des souris shiverer, comparées aux cellules PDGFR-α–positives non traitées. Ceci soutient l’idée que l’ajustement fin des signaux internes dans des progéniteurs déjà bien choisis peut améliorer davantage leurs performances comme outils vivants de réparation de la myéline.
Ce que cela signifie pour les traitements futurs
Pour le grand public, le message principal est que tous les précurseurs de myéline ne se valent pas. En combinant des outils puissants de lecture génétique et d’imagerie, cette étude identifie un sous-groupe remarquable — les hOPC PDGFR-α–positifs — qui migrent mieux, se divisent davantage et reconstruisent la myéline plus efficacement que leurs homologues. Elle met aussi en lumière des voies de signalisation internes que l’on peut moduler chimiquement pour rendre ces cellules encore plus puissantes. Ensemble, ces connaissances tracent une feuille de route pour concevoir des thérapies cellulaires plus sûres et plus efficaces visant à restaurer l’isolation du cerveau dans les maladies où la myéline est perdue.
Citation: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Mots-clés: réparation de la myéline, cellules progénitrices oligodendrocytaires, cellules souches neuronales, thérapie cellulaire, séquençage ARN unicellulaire