Clear Sky Science · fr
La bioénergétique mitochondriale et le dialogue avec le SASP déterminent l’efficacité des sénolytiques dans la sénescence induite par traitement
Pourquoi il est si difficile d’éliminer les cellules cancéreuses « zombies »
Beaucoup de traitements anticancéreux modernes ne tuent pas toutes les cellules tumorales sur le champ. Certaines cellules basculent plutôt dans un état de limbes appelé sénescence : elles arrêtent de se diviser mais restent vivantes, un peu comme des cellules « zombies ». Ces cellules sénescentes induites par les thérapies peuvent être utiles au départ, mais si elles persistent elles peuvent favoriser les rechutes, la résistance et des effets secondaires. Les chercheurs testent donc des médicaments sénolytiques conçus pour tuer sélectivement les cellules sénescentes. Cet article pose une question apparemment simple : pourquoi certaines cellules cancéreuses sénescentes meurent-elles sous l’effet des sénolytiques, alors que d’autres résistent obstinément ?
Des centrales électriques qui se souviennent de leur passé
Au cœur de l’étude se trouvent les mitochondries, ces petites centrales énergétiques intracellulaires. Les auteurs ont examiné si la façon dont les mitochondries brûlent différents carburants — sucres, lipides et acides aminés — influence la sensibilité des cellules cancéreuses sénescentes aux sénolytiques visant une protéine de survie appelée BCL‑xL. À l’aide d’un test à haut débit (MitoPlate S‑1), ils ont « profilé » fonctionnellement l’activité mitochondriale dans plusieurs lignées tumorales avant et après induction de la sénescence par différents traitements (agents génotoxiques, bloqueurs de la mitose, stress oxydatif ou inhibiteurs du cycle cellulaire). Ils ont constaté que la sénescence induite par traitement n’engendrait pas un état mitochondrial unique et uniforme. Chaque médicament laissait plutôt une « empreinte bioénergétique » distincte, modifiant l’étendue et l’intensité avec lesquelles les mitochondries pouvaient exploiter diverses sources d’énergie. Crucialement, cette flexibilité se superposait à une configuration mitochondriale préexistante : l’état initial des mitochondries des cellules parentes fixait une limite supérieure — un « plafond » — à la réponse sénolytique maximale possible.
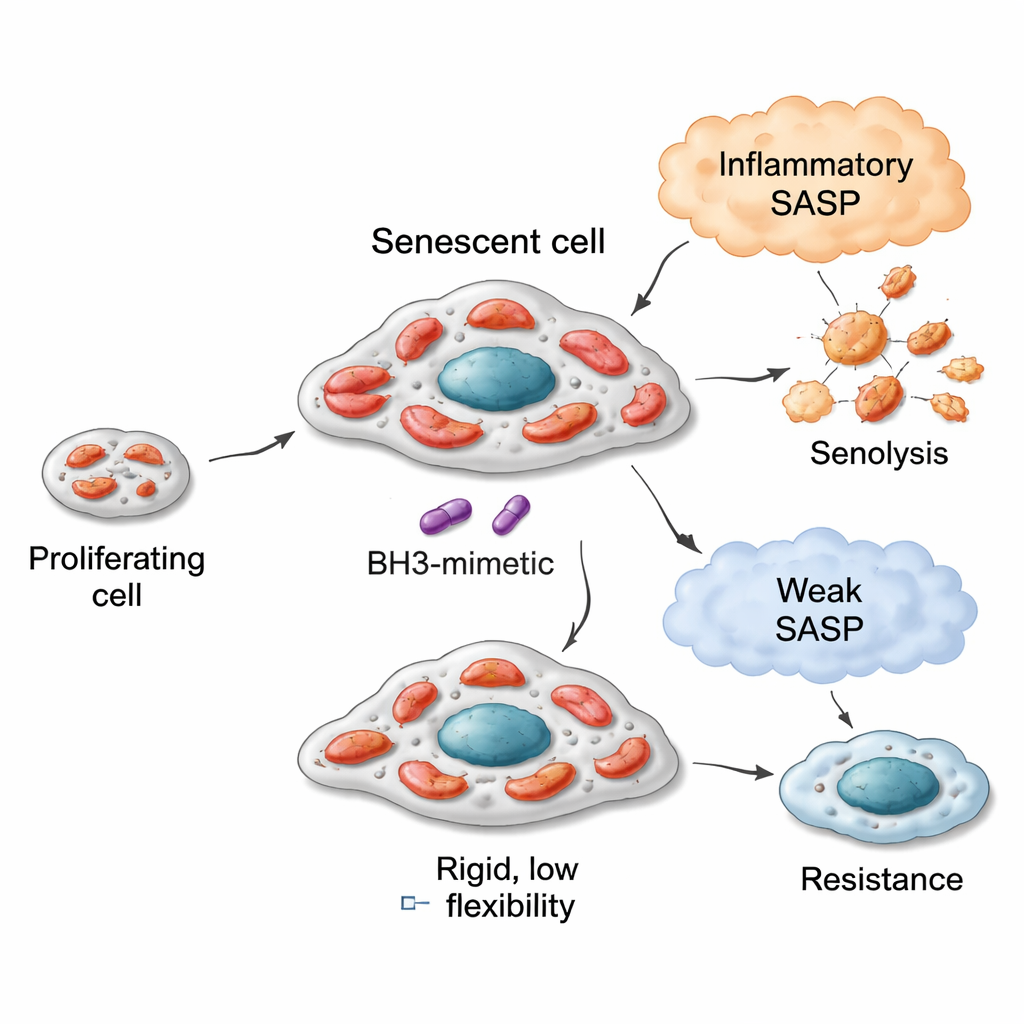
Moteurs flexibles, carburants différents et sensibilité aux sénolytiques
Dans des modèles de cancer du poumon, du sein et du côlon, les cellules sénescentes dont les mitochondries étaient plus flexibles — capables d’oxyder une plus large palette de carburants — avaient tendance à être plus vulnérables aux sénolytiques ciblant BCL‑xL, comme le navitoclax (ABT‑263) et l’A1331852. Par exemple, des cellules pulmonaires rendues sénescentes par la bléomycine développaient des mitochondries utilisant vigoureusement de nombreux substrats, en particulier ceux liés à la β‑oxydation des acides gras et à certaines voies des acides aminés. Ces cellules étaient très sensibles aux sénolytiques. En revanche, des cellules poussées en sénescence par un inhibiteur de CDK4/6 (palbociclib) présentaient un répertoire métabolique plus restreint et répondaient mal aux mêmes agents sénolytiques. Pourtant, cette relation avait des limites : des cellules mammaires pouvaient aussi devenir métaboliquement flexibles après sénescence, mais comme leurs mitochondries initiales étaient moins « prêtes » pour l’apoptose, leur réponse sénolytique maximale restait modeste. Les cellules du côlon avec un appareil apoptotique défectueux demeuraient résistantes indépendamment des changements métaboliques. Une mesure simple — la capacité d’oxyder le succinate au repos — s’est révélée un indicateur facile de cette capacité mitochondriale héritée.
Quand le métabolisme dialogue avec l’inflammation
Les cellules sénescentes sont connues pour le SASP, un cocktail de facteurs inflammatoires et de croissance sécrétés qui peuvent influencer les tissus environnants. L’équipe a exploré comment le métabolisme mitochondrial se relie à ce comportement sécrétoire en utilisant des cellules modifiées portant un rapporteur pour la miR‑146a, un microARN activé par le régulateur inflammatoire maître NF‑κB. Ils ont trouvé que, si les profils globaux du SASP étaient largement dictés par le type cellulaire, seuls certains états sénescents activaient cet axe NF‑κB/miR‑146a. Ce furent les mêmes états qui répondaient bien aux sénolytiques ciblant BCL‑xL. Fait important, ces cellules sénescentes « SASP inflammatoire‑positives » montraient aussi une utilisation accrue de l’oxydation des acides gras et une hausse transcriptionnelle des gènes impliqués dans l’importation des acides gras à longue chaîne vers les mitochondries. Bloquer l’entrée des acides gras avec l’étoxomir atténuait l’activation de la miR‑146a sans inverser complètement la sénescence, suggérant que le choix du carburant mitochondrial contribue à autoriser un SASP inflammatoire propice aux sénolytiques.
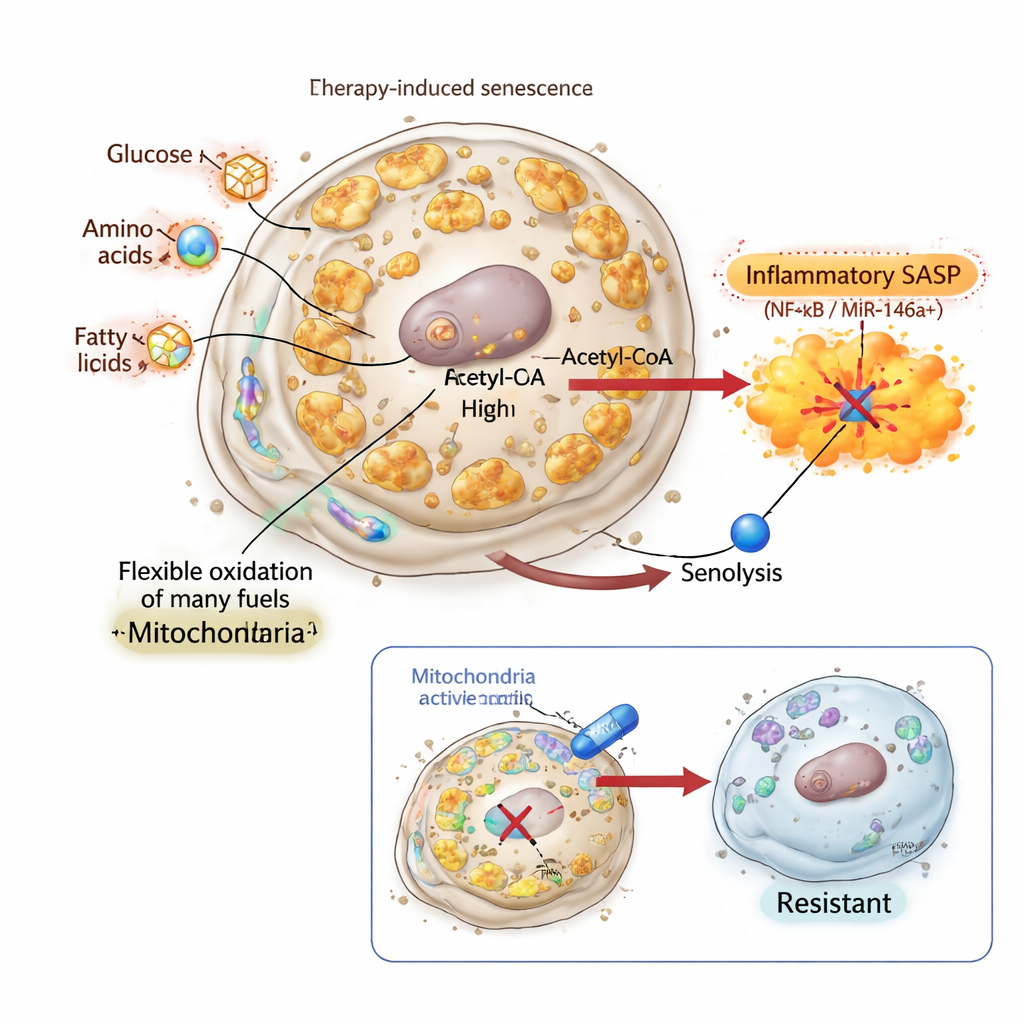
Éteindre le signal et créer des cellules sénescentes invincibles
Pour tester si le SASP inflammatoire est réellement nécessaire à l’élimination par les sénolytiques, les chercheurs ont utilisé l’inflachromène, un composé qui se lie aux protéines de la chromatine HMGB1 et HMGB2 et bloque leur rôle dans l’activation des gènes du SASP. Dans des cellules pulmonaires et mammaires, l’inflachromène a induit un phénotype sénescent classique : les cellules ont grossi, cessé de se diviser et accumulé des marqueurs de sénescence. Leur masse mitochondriale et leur activité bioénergétique ont augmenté substantiellement, et l’utilisation des carburants a été clairement remodelée. Pourtant, leur SASP était atténué et le rapporteur miR‑146a restait en grande partie silencieux. De manière frappante, ces cellules sénescentes dépourvues de SASP étaient complètement résistantes aux sénolytiques ciblant BCL‑xL, malgré des mitochondries bioénergétiquement actives et reprogrammées et une moindre expression du gène anti‑apoptotique classique BCL2. Cela montre que les changements mitochondriaux seuls ne suffisent pas ; sans cette sortie inflammatoire pilotée par les mitochondries, la « seconde frappe » sénolytique échoue.
Ce que cela signifie pour les traitements anticancéreux futurs
Pour un lecteur non spécialiste, la conclusion de l’étude est que l’élimination des cellules cancéreuses « zombies » induites par traitement est gouvernée par un circuit à plusieurs couches. D’abord, la santé et le câblage initiaux des mitochondries d’une cellule tumorale déterminent jusqu’où les sénolytiques peuvent aller. Ensuite, le traitement qui provoque la sénescence peut orienter le métabolisme mitochondrial vers plus ou moins de flexibilité, rapprochant ou éloignant les cellules du seuil d’apoptose. Troisièmement — et de manière décisive — les sénolytiques ne fonctionnent bien que si le reformatage métabolique active avec succès un programme SASP inflammatoire qui parle au noyau. Sans ce dialogue inflammatoire, les cellules sénescentes peuvent devenir un état final résistant aux médicaments. Concrètement, cela suggère que les thérapies futures pourraient être optimisées en testant fonctionnellement à la fois la flexibilité mitochondriale et l’inflammation SASP dans les tumeurs, puis en choisissant des combinaisons d’inducteurs de sénescence et de sénolytiques garantissant que les cellules « zombies » ne sont pas seulement figées, mais prêtes à être éliminées.
Citation: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Mots-clés: sénescence cellulaire, mitochondries, sénolytiques, métabolisme du cancer, SASP inflammatoire