Clear Sky Science · fr
La réduction de SREBP1 déclenche la ferroptose en supprimant l’axe Nrf2‑XCT/GPX4 dans le cancer de l’ovaire
Retourner contre lui l’usine à graisses du cancer
Le cancer de l’ovaire est souvent détecté tardivement et peut être très difficile à traiter. Cette étude met au jour une faiblesse surprenante de ces tumeurs : leur dépendance à la synthèse des graisses. Les chercheurs montrent que couper l’un des interrupteurs maîtres de la production lipidique dans les cellules cancéreuses ralentit leur croissance et active un type particulier de mort cellulaire, tout en facilitant l’attaque de la tumeur par le système immunitaire.
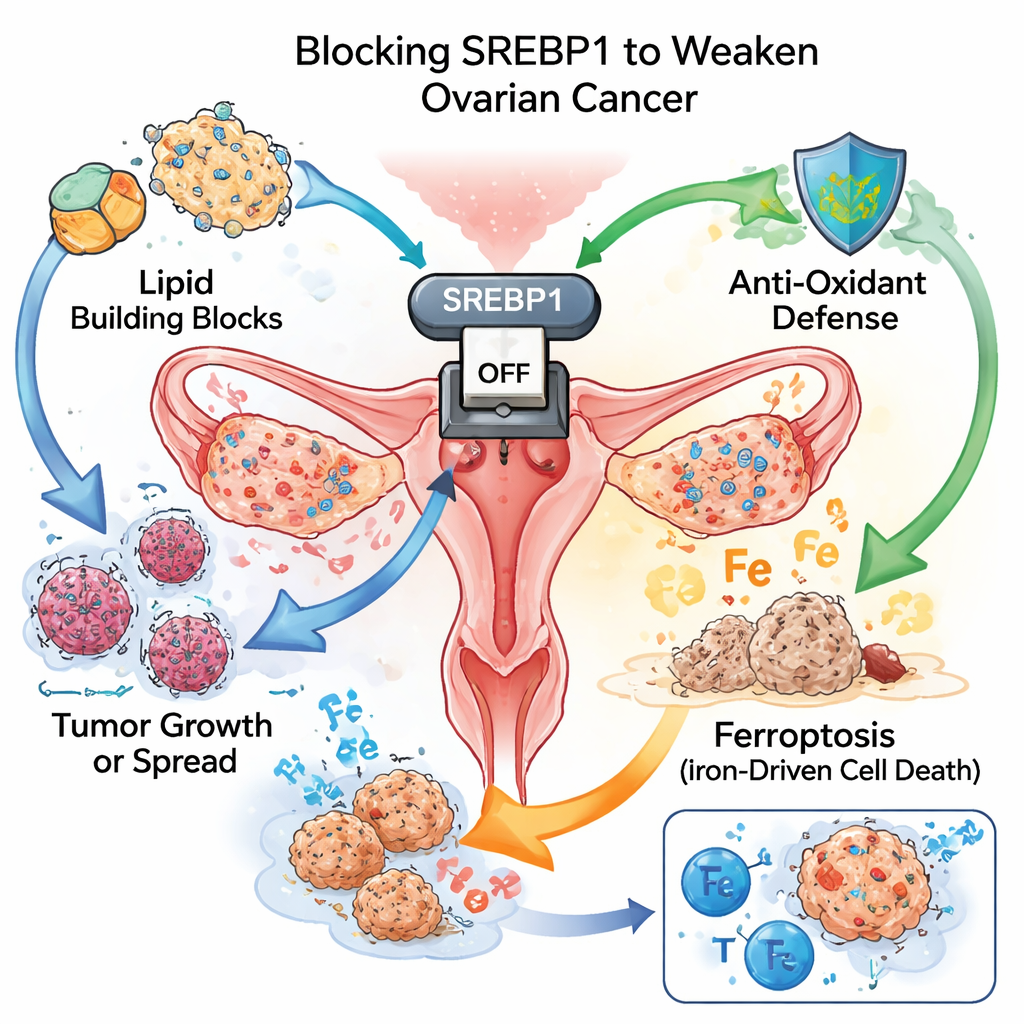
Un commutateur maître pour le carburant tumoral
Comme des mauvaises herbes à croissance rapide, les cellules cancéreuses ont besoin d’énormes quantités de blocs de construction et d’énergie. Une façon d’y parvenir est de réorienter leur synthèse et leur utilisation des lipides. L’équipe s’est concentrée sur SREBP1, une protéine qui joue le rôle d’interrupteur principal de la production lipidique. Dans des prélèvements tissulaires provenant de plus d’une centaine de patientes, les tumeurs ovariennes présentaient des niveaux de SREBP1 bien plus élevés que les tissus sains adjacents. Les femmes dont les tumeurs montraient une coloration plus intense pour SREBP1 avaient tendance à développer des maladies plus agressives et à avoir une survie plus courte, faisant de cette protéine à la fois un moteur de progression et un marqueur de mauvais pronostic.
Ralentir la croissance et la dissémination en coupant les lipides
Dans des lignées cellulaires de cancer de l’ovaire cultivées en laboratoire, la réduction de SREBP1 a fortement diminué la capacité des cellules à se multiplier et à former des colonies. Les cellules se sont bloquées à des étapes spécifiques du cycle cellulaire, ce qui les empêchait de se diviser efficacement. Les chercheurs ont aussi observé moins de signes de mobilité et d’invasion : des tests de cicatrisation et de Transwell ont montré que les cellules privées de SREBP1 migraient moins, et les marqueurs clés d’un processus de changement de forme appelé EMT revenaient vers un état plus « normal ». Parallèlement, les niveaux de triglycérides et de cholestérol ont chuté et la coloration a révélé moins de gouttelettes lipidiques à l’intérieur des cellules, confirmant que leur machinerie interne de production de graisses avait été réduite.
Déclencher une mort cellulaire alimentée par le fer
L’effet le plus marquant du blocage de SREBP1 a été l’activation de la ferroptose, une forme de mort cellulaire récemment reconnue, provoquée par le fer et la peroxydation des membranes lipidiques. Seul un bloqueur de la ferroptose, et non des inhibiteurs des autres voies de mort cellulaire, a pu sauver les cellules privées de SREBP1, ce qui indique que la ferroptose est la cause principale de leur disparition. Des analyses chimiques ont mis en évidence davantage de produits de dégradation issus de lipides oxydés, moins de glutathion antioxydant et des niveaux plus élevés de molécules lipidiques réactives. Deux protéines qui protègent normalement les cellules de la ferroptose, appelées xCT et GPX4, ont été fortement réduites lorsque SREBP1 a été abaissé, éliminant une protection cruciale contre ce processus destructeur.
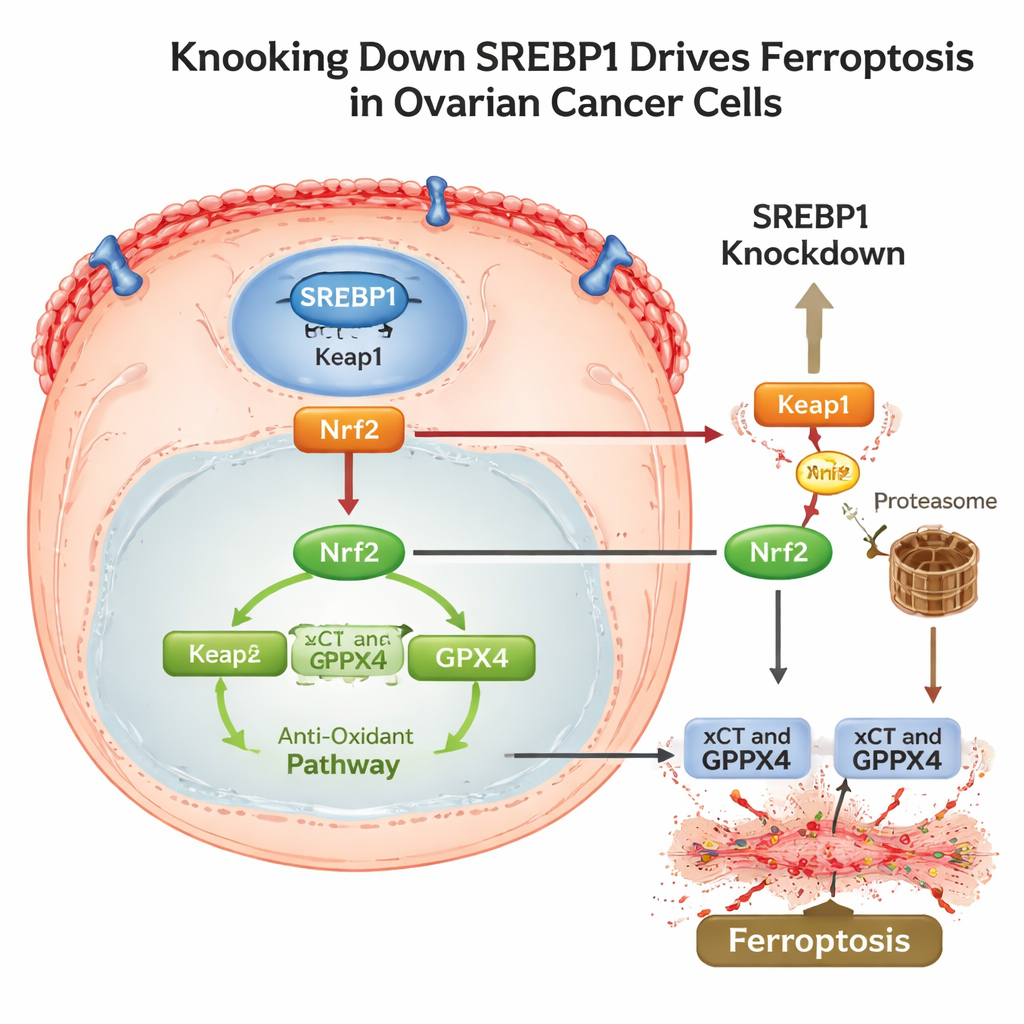
Désarmer le bouclier antioxydant et les mécanismes d’évasion
Pour comprendre comment SREBP1 se relie à ce programme de mort, les scientifiques ont tracé une voie impliquant une autre protéine majeure de la réponse au stress, Nrf2. Dans des conditions normales, Nrf2 aide les cellules à survivre en activant des gènes antioxydants, dont xCT et GPX4. L’étude a montré que la diminution de SREBP1 augmentait les niveaux de Keap1, une protéine qui marque Nrf2 pour sa dégradation, entraînant plus de destruction de Nrf2 et moins de protéine atteignant le noyau. Avec la baisse de Nrf2, ses défenses en aval se sont affaiblies et la ferroptose a suivi. Fait important, les tumeurs riches en SREBP1 présentaient également des niveaux plus élevés de PD‑L1, une protéine de surface qui aide les cellules cancéreuses à se cacher des lymphocytes T attaquants. Lorsque SREBP1 a été réduit dans des tumeurs murines, les cancers ont crû plus lentement, ont montré davantage de signes de dommages lipidiques, moins de Nrf2 et de GPX4, et une expression réduite de PD‑L1, accompagnés d’une activité immunitaire accrue.
Pourquoi cela compte pour les traitements futurs
En termes clairs, les tumeurs ovariennes semblent utiliser SREBP1 comme un outil de survie à double tranchant : il alimente leur croissance en stimulant la production de lipides et, en même temps, leur confère un bouclier antioxydant et un déguisement immunitaire. Ce travail montre que couper SREBP1 peut priver la tumeur en lipides, lui enlever sa protection contre les dommages induits par le fer et réduire sa capacité à échapper au système immunitaire. Cela fait de SREBP1 une cible attrayante pour de nouveaux médicaments et suggère que combiner des inhibiteurs de SREBP1 avec des traitements qui déclenchent la ferroptose ou libèrent la réponse immunitaire pourrait offrir aux patientes un contrôle de la maladie plus efficace et durable.
Citation: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Mots-clés: cancer de l’ovaire, métabolisme des lipides, ferroptose, SREBP1, immunité tumorale