Clear Sky Science · fr
L’activation des caspases favorise l’acantholyse induite par les anti‑Desmoglein 3 dans l’épiderme humain
Quand le corps s’attaque à sa propre colle cutanée
Le pemphigus vulgaire est une maladie rare mais dangereuse dans laquelle le système immunitaire attaque la « colle » qui maintient les cellules de la peau ensemble, provoquant des cloques douloureuses et des lésions ouvertes. Cette étude examine le phénomène au microscope pour répondre à une question centrale : ces cloques se forment‑elles uniquement parce que des anticorps bloquent cette colle, ou bien des signaux supplémentaires de mort cellulaire contribuent‑ils à déchirer les cellules cutanées ? Mieux comprendre cela pourrait ouvrir la voie à des traitements plus ciblés et plus doux pour les patients.
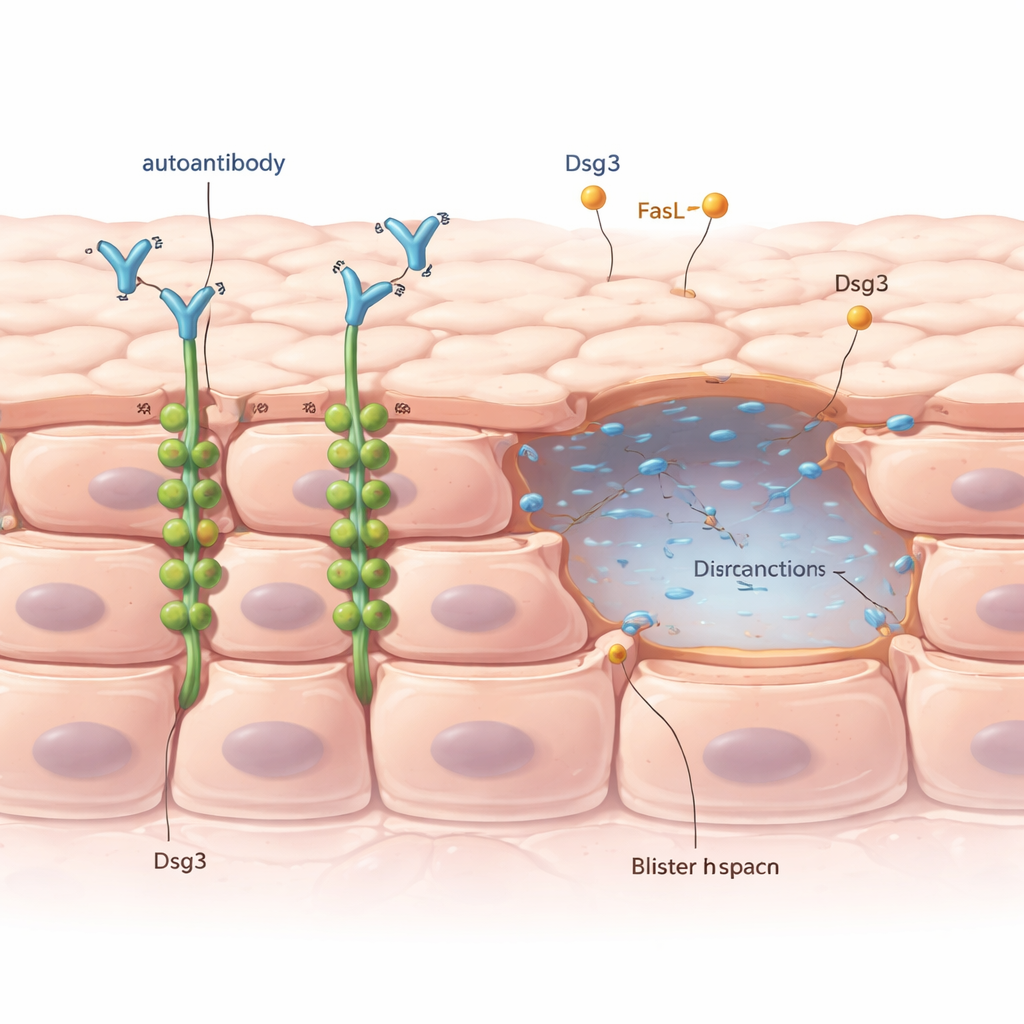
Comment les cellules cutanées restent normalement attachées
La couche externe de notre peau est constituée de cellules étroitement assemblées reliées par de petites structures appelées desmosomes, qui font office de rivets entre cellules voisines. Un composant clé de ces rivets est une protéine nommée desmogleine 3, ou Dsg3. Dans le pemphigus vulgaire, les patients produisent des anticorps qui se lient par erreur à la Dsg3. Les médecins savent depuis longtemps que cette attaque anticorps conduit à un processus appelé acantholyse, où les cellules cutanées perdent contact et des cloques apparaissent. Mais, de façon troublante, les cloques n’apparaissent qu’à certains endroits et à certains moments, alors que les anticorps nuisibles sont présents dans toute la peau.
Les anticorps seuls peuvent initier les dégâts
Pour observer l’effet direct des anticorps, les chercheurs ont utilisé des fragments de peau humaine saine et une lignée cellulaire cutanée cultivée en laboratoire. Ils les ont exposés à un anticorps anti‑Dsg3 bien caractérisé. Ils ont constaté que cet anticorps pouvait affaiblir l’adhésion cellule‑cellule et déclencher l’acantholyse sans activer la machinerie habituelle de mort cellulaire à l’intérieur des cellules. L’événement clé était le retrait de la Dsg3 de la surface cellulaire vers l’intérieur de la cellule, souvent emballée dans de petites vésicules. Ce retrait de la Dsg3 des « rivets » entre cellules raccourcissait et rendait les desmosomes moins efficaces, permettant aux cellules de commencer à se séparer.
Quand les signaux de mort cellulaire s’en mêlent, la situation empire
L’équipe s’est ensuite demandé si un signal de mort cellulaire connu dans le pemphigus, une molécule appelée ligand Fas (FasL), modifiait ce tableau. Le FasL peut activer des enzymes appelées caspases, en particulier la caspase‑8, qui poussent normalement les cellules vers une mort programmée. Dans des échantillons de peau de patients et dans leur modèle cutané, les chercheurs ont observé une caspase‑8 active dans les zones endommagées mais sans signes classiques de cellules en train de mourir. Lorsqu’ils ont ajouté de petites quantités non létales de FasL conjointement à l’anticorps anti‑Dsg3, les cloques se sont formées plus rapidement et de façon plus sévère, en particulier dans les couches profondes de l’épiderme. En culture cellulaire, le FasL seul n’affaiblissait pas l’adhésion, mais en combinaison avec l’anticorps il augmentait fortement la dissociation cellulaire — et cet effet d’amplification disparaissait lorsque la caspase‑8 était bloquée.
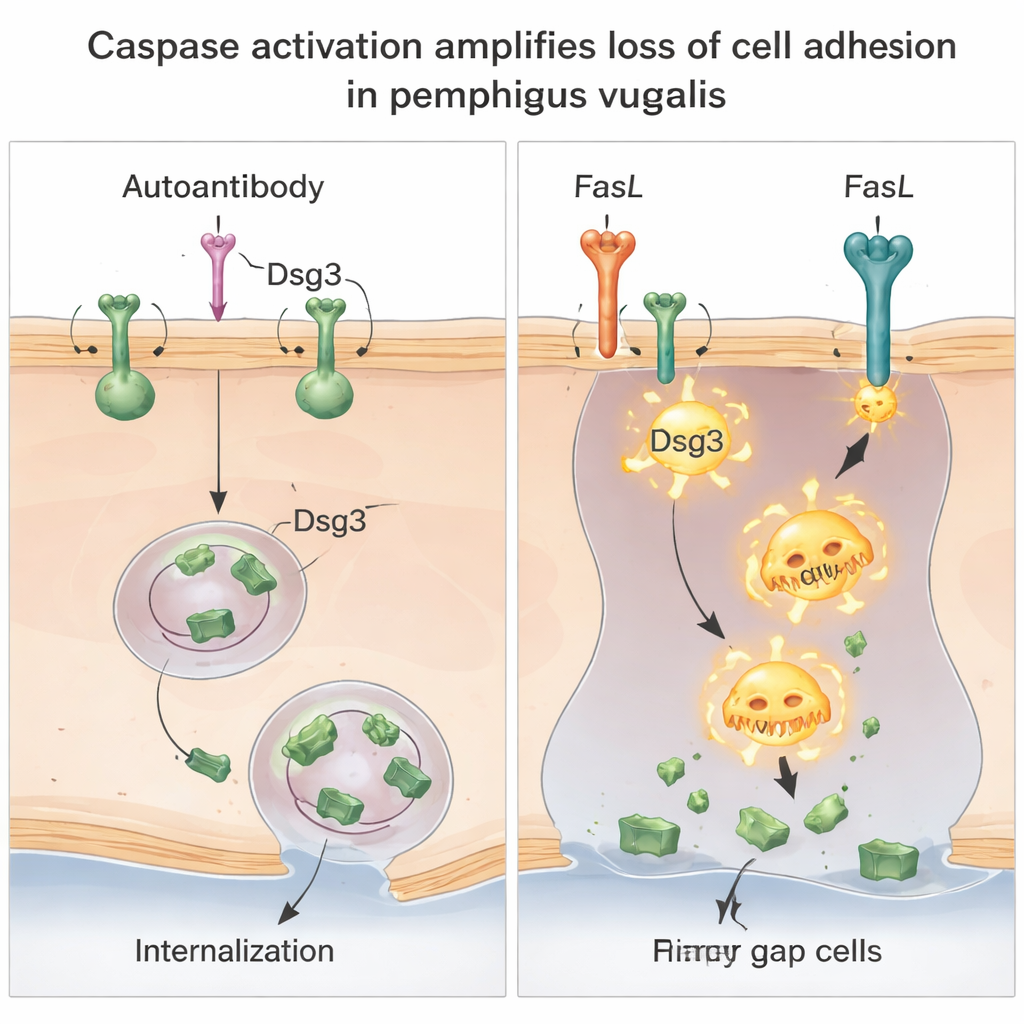
Deux manières de rompre la même liaison
En creusant davantage, les scientifiques ont montré qu’il existe en réalité deux mécanismes distincts mais coopératifs par lesquels la Dsg3 est perdue. D’abord, l’anticorps favorise l’internalisation de complexes Dsg3–anticorps intacts depuis la surface cellulaire vers des compartiments membranaires spécialisés, réduisant la quantité de Dsg3 disponible aux jonctions cellulaires. Cette étape n’était pas dépendante des caspases et n’était pas interrompue par le blocage des voies courantes de dégradation des protéines, ce qui suggère un réarrangement spécifique de la Dsg3 à l’intérieur de la cellule. Ensuite, en présence de FasL, la caspase‑8 devient active et clive la Dsg3 en fragments plus petits, surtout dans les régions de la membrane moins solidement attachées. Cette coupure dirigée par les caspases réduit encore la quantité de Dsg3 pleine longueur et fonctionnelle et amplifie la perte d’adhésion déclenchée par les anticorps.
Ce que cela signifie pour les patients et les traitements futurs
Pris ensemble, les résultats suggèrent que dans le pemphigus vulgaire, les anticorps dirigés contre la Dsg3 initient le processus de formation de cloques en retirant la Dsg3 de la surface cellulaire, tandis que l’activation des caspases induite par le FasL agit comme un amplificateur qui aggrave fortement les lésions en clivant la Dsg3 restante. Il est important de noter qu’une grande partie de ces phénomènes survient avant que les cellules cutanées ne meurent réellement. Pour les patients, cela signifie que des thérapies efficaces pourraient non seulement réduire les anticorps nuisibles mais aussi bloquer le FasL ou les caspases afin d’empêcher la formation ou la propagation des cloques. Ce mécanisme dual pourrait aider à expliquer pourquoi la maladie peut se présenter et évoluer si différemment d’une personne — ou d’un site cutané — à l’autre, et indique des pistes nouvelles et plus précises pour préserver la « colle » naturelle de la peau.
Citation: Schmidt, M.F., Feoktistova, M.A., Panayotova-Dimitrova, D. et al. Caspase-activation powers anti-Desmoglein 3-induced acantholysis in human epidermis. Cell Death Discov. 12, 102 (2026). https://doi.org/10.1038/s41420-026-02963-w
Mots-clés: pemphigus vulgaire, clivage cutané auto‑immun, desmogleine 3, caspase‑8, ligand Fas