Clear Sky Science · fr
PDHA1 renforce la résistance à la ferroptose dans le cancer de la prostate résistant à l’anoïkis en surexprimant AIFM2
Pourquoi certaines cellules du cancer de la prostate refusent de mourir
Quand des cellules cancéreuses se détachent d’une tumeur et entrent dans la circulation sanguine, la plupart devraient mourir avant d’atteindre un nouvel organe. Pourtant, une minorité dangereuse survit, migre et ensemence des métastases souvent mortelles. Cette étude pose une question cruciale : qu’est-ce qui permet à certaines cellules du cancer de la prostate de résister à une forme de mort cellulaire qui survient normalement lorsque les cellules perdent le contact avec leur tissu d’origine ? En révélant un circuit de survie caché à l’intérieur de ces cellules, la recherche indique de nouvelles façons de bloquer les métastases à la source.
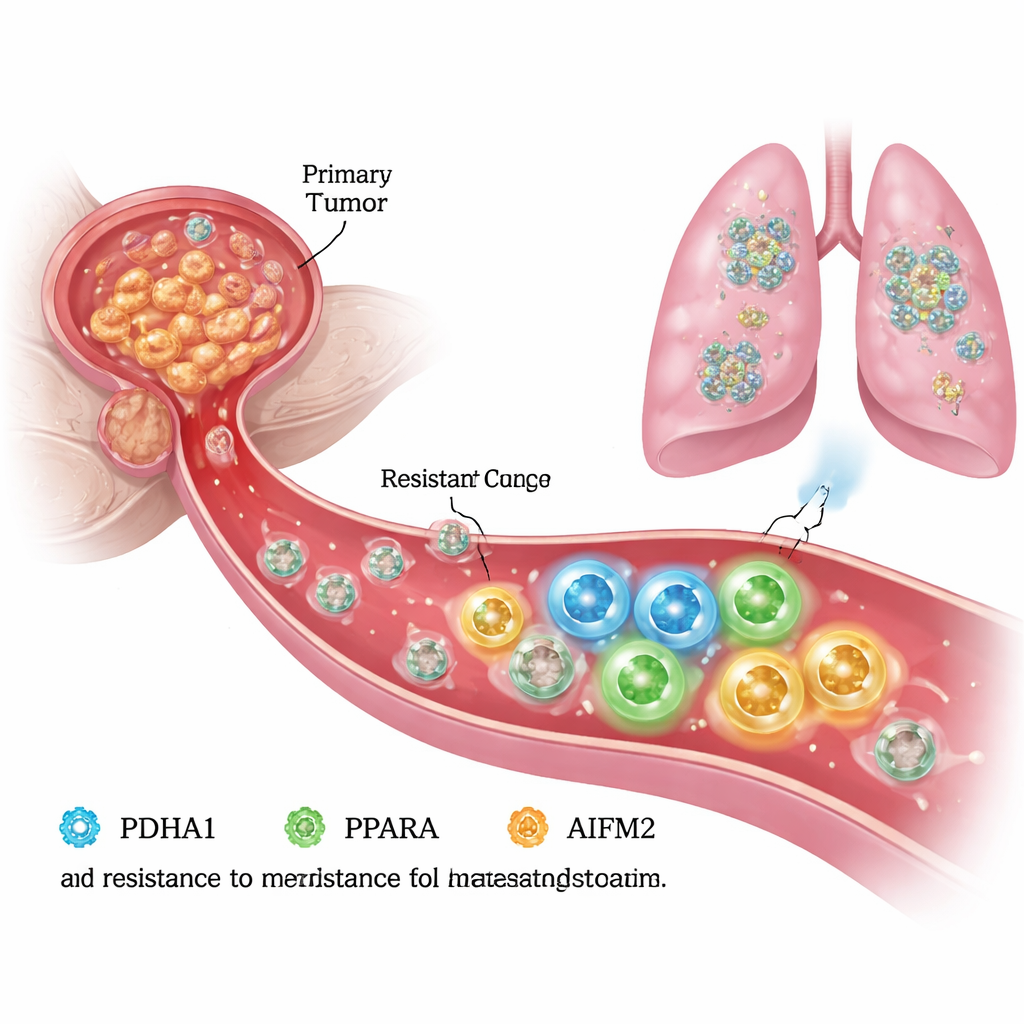
Échapper à la mort dans la circulation sanguine
Pour se disséminer, les cellules du cancer de la prostate doivent supporter la vie sans le soutien du tissu environnant, appelé matrice extracellulaire. Dans ces conditions de « détachement », les cellules saines subissent une mort programmée appelée anoïkis, et de nombreuses cellules cancéreuses sont également vulnérables à un processus de mort lié au fer, la ferroptose. Les auteurs ont créé en laboratoire des cellules de cancer de la prostate résistantes à l’anoïkis et les ont comparées à leurs cellules « parentales » d’origine. Ils ont constaté que les cellules résistantes migraient et envahissaient de façon plus agressive, mais survivaient aussi mieux en condition de détachement, suggérant qu’elles avaient reconfiguré leur machinerie interne pour éviter la ferroptose et continuer de proliférer.
Un commutateur métabolique avec une seconde fonction
En creusant davantage, l’équipe s’est concentrée sur une enzyme métabolique appelée PDHA1, surtout connue pour aider les cellules à transformer le pyruvate dérivé du glucose en acétyl-CoA dans les mitochondries, alimentant la production d’énergie. Dans les cellules résistantes à l’anoïkis, les niveaux et l’activité de PDHA1 étaient sensiblement plus élevés, et des échantillons de patients montraient davantage de PDHA1 dans les tumeurs primaires d’hommes dont le cancer de la prostate s’était étendu aux ganglions lymphatiques ou à des sites distants. Lorsque les chercheurs ont diminué PDHA1, les cellules résistantes ont perdu une grande partie de leur capacité à migrer, envahir et survivre. De façon surprenante, une fraction substantielle de PDHA1 dans ces cellules n’était plus confinée aux mitochondries ; elle s’était relocalisée dans le noyau, où l’ADN est emballé avec des histones qui peuvent être modifiées chimiquement pour activer ou réprimer des gènes.
Réécrire l’activité génique pour bloquer la ferroptose
Dans le noyau, PDHA1 semblait alimenter la production locale d’acétyl-CoA, un élément clé pour l’acétylation des histones. Les auteurs ont montré que PDHA1 nucléaire augmentait une marque spécifique, l’acétylation de H3K9, dans la région de contrôle d’un gène appelé PPARA. Ce changement agissait comme un relâchement des « bobines » de chromatine, rendant plus facile l’activation de PPARA. PPARA, à son tour, servait de commutateur principal en augmentant la production d’une autre protéine, AIFM2, en se liant à son promoteur et en élevant sa transcription. Plutôt que d’ajuster directement le gène AIFM2, PDHA1 agissait donc via PPARA, établissant une voie en plusieurs étapes reliant le métabolisme altéré à la régulation génique modifiée.
Construire un bouclier contre les dégâts oxydatifs liés au fer
AIFM2 est connu comme un frein interne à la ferroptose : il aide à protéger les lipides des membranes cellulaires contre l’oxydation destructive. Dans les cellules résistantes du cancer de la prostate, la surexpression de PDHA1 augmentait les niveaux d’AIFM2, tandis que l’inhibition de PDHA1 les réduisait. Des tests fonctionnels ont montré que la réduction de PDHA1 intensifiait les signes caractéristiques de la ferroptose — plus d’espèces réactives de l’oxygène, davantage de dommages lipidiques, une baisse du potentiel de membrane mitochondrial et un rétrécissement mitochondrial caractéristique — surtout lorsque les cellules étaient exposées à l’erastine, un médicament induisant la ferroptose. La surexpression d’AIFM2 a inversé ces effets, restaurant la survie cellulaire en culture et rétablissant les métastases pulmonaires chez la souris, même lorsque PDHA1 était supprimé. Cela confirme qu’AIFM2 est un effecteur critique en aval de la résistance à la ferroptose induite par PDHA1.
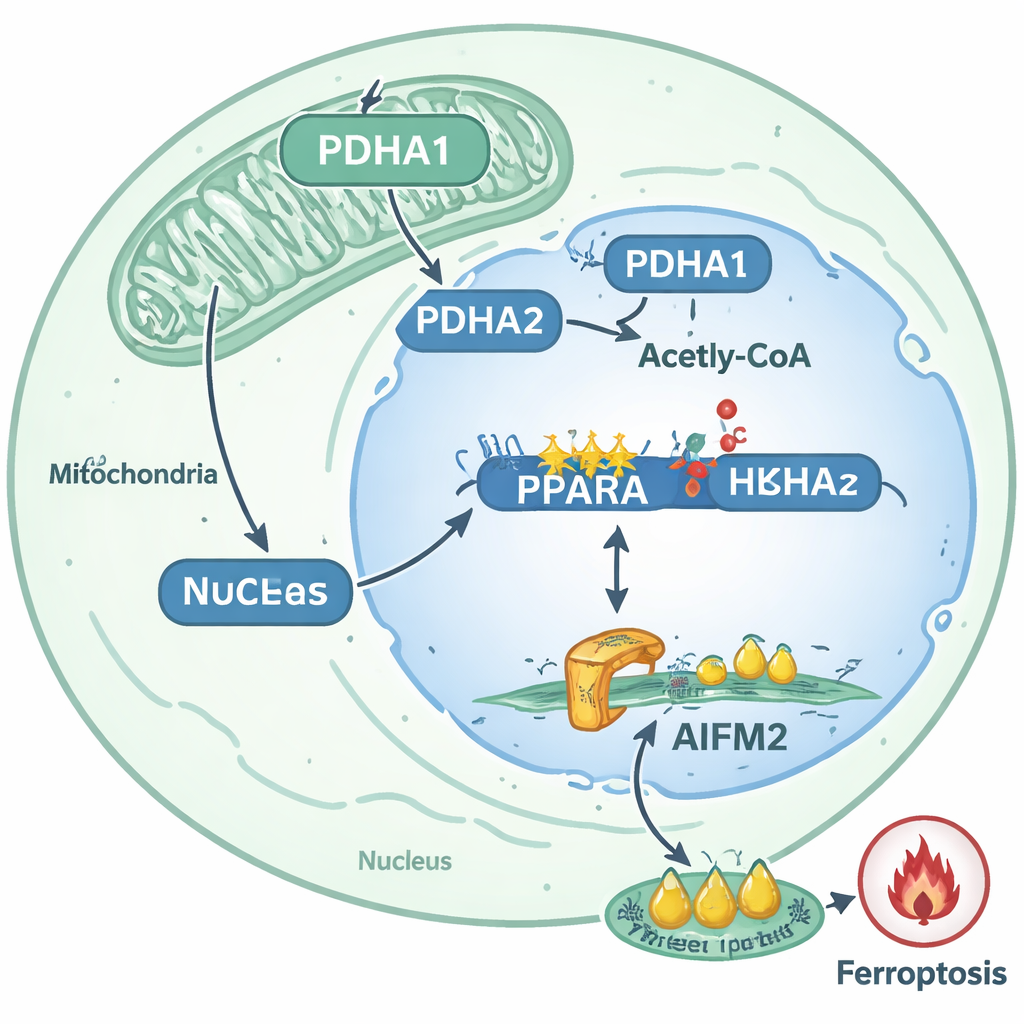
Du circuit moléculaire aux pistes thérapeutiques
En cartographiant ces événements, l’étude décrit une voie claire par laquelle des cellules de cancer de la prostate détachées deviennent plus difficiles à éliminer : PDHA1 migre vers le noyau, augmente l’acétylation des histones au niveau du gène PPARA, stimule l’activité de PPARA et élève ainsi les niveaux d’AIFM2 pour bloquer la ferroptose. Cette voie est fortement liée au comportement métastatique dans les tumeurs de patients et dans des modèles animaux. Pour un public non spécialiste, la conclusion est que certaines cellules cancéreuses réaffectent une enzyme métabolique courante en un outil épigénétique qui reprogramme l’activité génique et construit un bouclier biochimique contre une forme puissante de mort cellulaire. Les auteurs suggèrent que des médicaments ciblant PDHA1, PPARA ou AIFM2 — ou des thérapies qui déclenchent délibérément la ferroptose — pourraient un jour être combinés pour priver les cellules métastatiques du cancer de la prostate de cet avantage de survie et les rendre beaucoup plus vulnérables lors de leur parcours le plus périlleux : le saut d’un organe à un autre.
Citation: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Mots-clés: métastases du cancer de la prostate, ferroptose, résistance à l’anoïkis, PDHA1, AIFM2