Clear Sky Science · fr
Modulation des signatures métaboliques pour atténuer la résistance au cabozantinib dans des modèles cellulaires de leucémie aiguë myéloblastique FLT3-ITD
Pourquoi cela importe pour le traitement du cancer
De nombreux traitements anticancéreux modernes visent une protéine défectueuse unique dans les cellules tumorales. Ces médicaments ciblés peuvent provoquer des rémissions spectaculaires, mais les cancers trouvent souvent des moyens de s’adapter et de renaître. Cet article examine comment un type de cancer du sang, la leucémie aiguë myéloblastique (LAM), devient résistant à l’un de ces médicaments ciblés, le cabozantinib, et comment la reconfiguration de l’utilisation d’énergie par les cellules cancéreuses pourrait aider les cliniciens à contourner cette résistance.
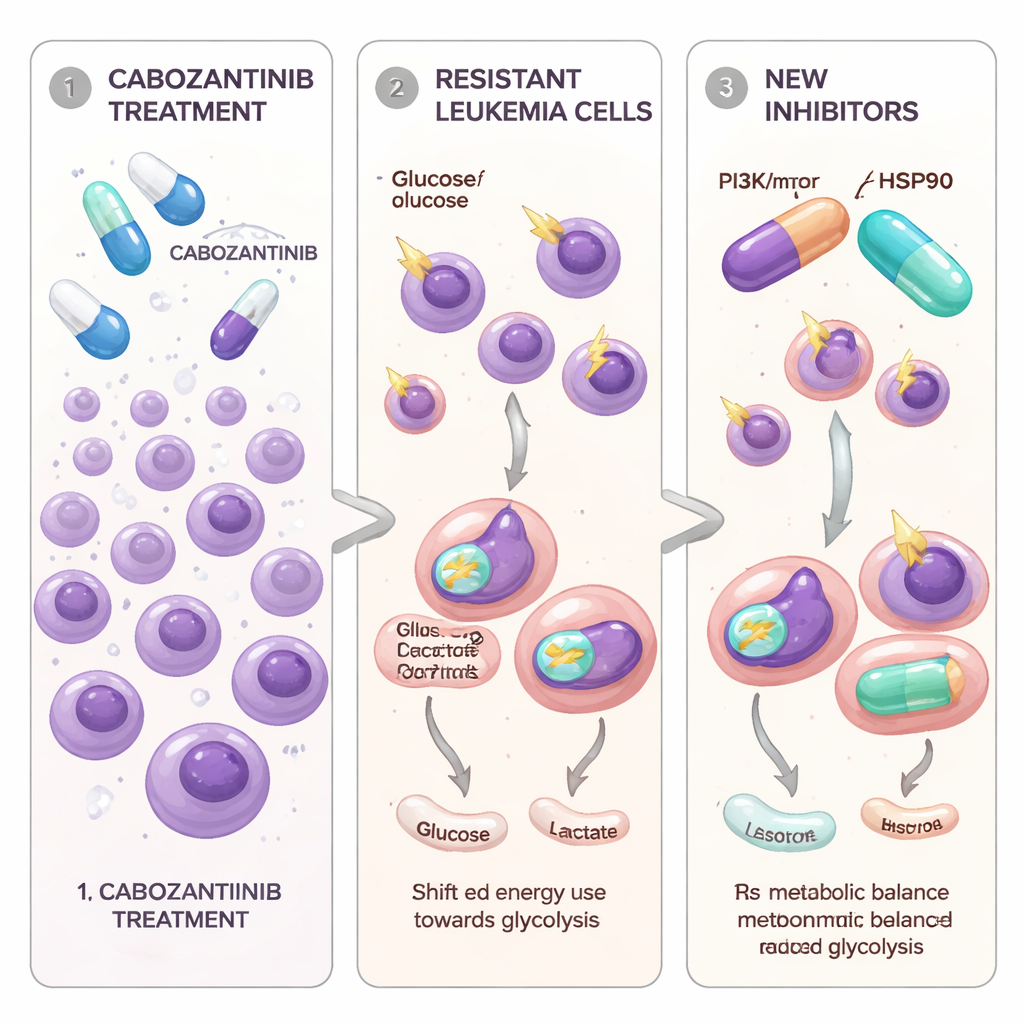
Cellules leucémiques qui apprennent à éviter un médicament ciblé
Les chercheurs se sont concentrés sur des cellules de LAM portant une mutation dans un commutateur de signal de croissance appelé FLT3-ITD, connu pour entraîner une maladie particulièrement agressive. Le cabozantinib, un comprimé déjà utilisé pour plusieurs tumeurs solides, peut fortement bloquer les cellules leucémiques dépendantes de FLT3 en laboratoire. Pour modéliser ce qui se passe chez les patients au fil du temps, l’équipe a exposé progressivement deux lignées cellulaires de LAM mutantes FLT3 à des doses croissantes de cabozantinib jusqu’à ce que certaines cellules survivent et recommencent à proliférer. Ces nouvelles populations cellulaires, appelées Molm13-XR et MV4-11-XR, pouvaient tolérer des concentrations de cabozantinib bien supérieures à celles de leurs cellules « parentales » d’origine. Elles sont également devenues moins sensibles à deux autres médicaments approuvés ciblant FLT3, le sorafénib et le quizartinib, tout en restant vulnérables à un inhibiteur différent, le gilteritinib.
Ajustements génétiques qui aident le cancer à survivre
En examinant de plus près, les scientifiques ont découvert que ces cellules leucémiques résistantes portaient de nouvelles altérations dans leur gène FLT3. Les deux lignées résistantes avaient acquis la même mutation ponctuelle, appelée D835Y, dans une région cruciale du domaine kinase de FLT3, un point chaud connu pour la résistance à plusieurs médicaments. Une des lignées, MV4-11-XR, a également présenté une délétion inhabituelle de 1,3 kilobase supprimant un exon entier de FLT3, effaçant une partie du domaine importante pour la liaison des médicaments. Ces changements semblent avoir été sélectionnés pendant l’exposition prolongée au cabozantinib : les versions mutantes de FLT3 sont devenues beaucoup plus fréquentes dans les cellules résistantes que dans la population de départ. Parallèlement, des voies de signalisation clés en aval de FLT3 — comme ERK, STAT5 et AKT — étaient plus fortement activées, soutenant une croissance plus rapide et une formation de colonies accrue dans les cellules résistantes.
Les cellules cancéreuses changent leur mode d’alimentation
L’équipe s’est ensuite demandé si la résistance était liée non seulement à la génétique, mais aussi à la façon dont les cellules se « nourrissent ». À l’aide du séquençage ARN et de tests métaboliques dédiés, ils ont trouvé un schéma cohérent : les cellules résistantes au cabozantinib dépendaient beaucoup plus de la glycolyse — la dégradation rapide du glucose dans le cytosol — même lorsque l’oxygène était abondant. Ces cellules absorbaient plus de glucose, produisaient davantage de lactate, montraient une activité accrue d’une enzyme clé appelée GAPDH et augmentaient l’expression de plusieurs gènes liés à la glycolyse. En revanche, les mitochondries, structures supportant une production d’énergie plus efficace, étaient moins actives et moins abondantes. Les mesures de la consommation d’oxygène ont révélé que la respiration mitochondriale basale et maximale était réduite, et que les espèces réactives de l’oxygène à l’intérieur des cellules étaient élevées, signe de mitochondries stressées et sous‑performantes.
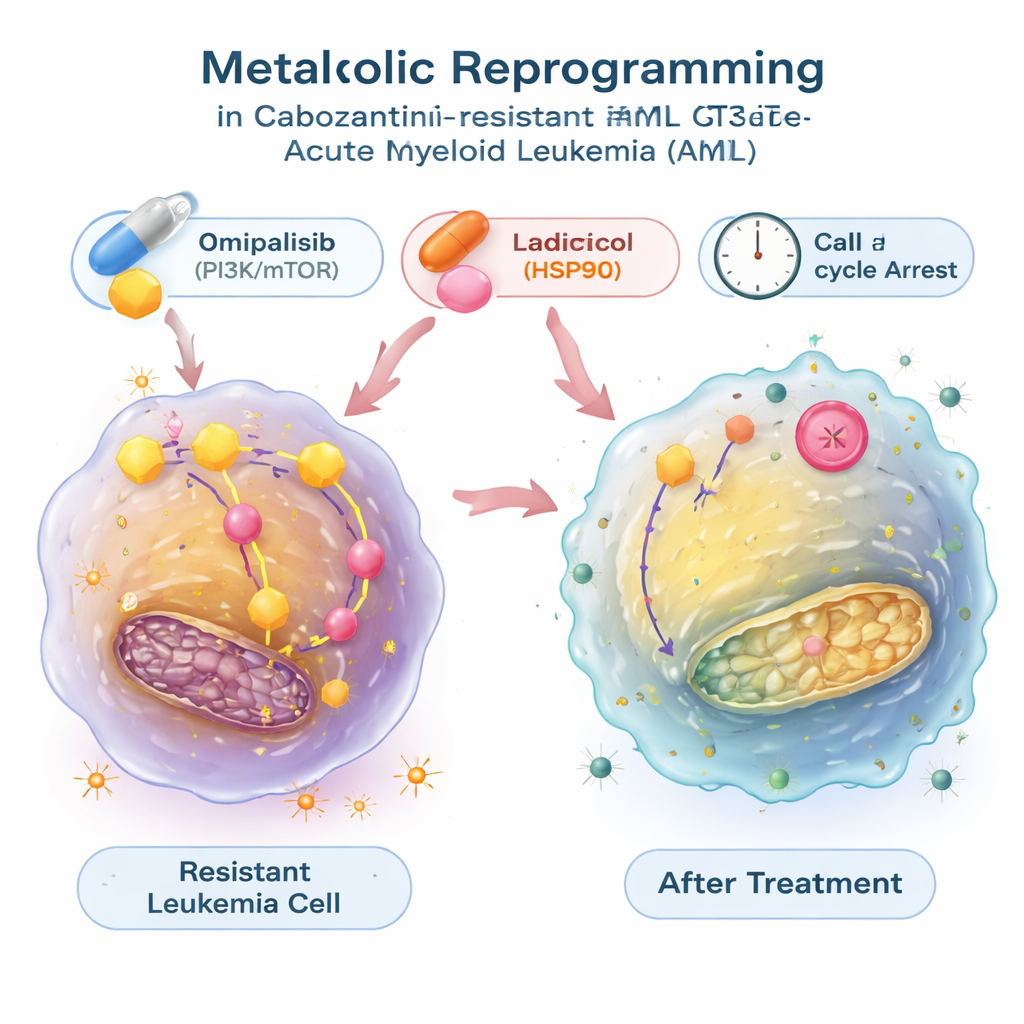
Identifier des médicaments qui inversent l’interrupteur métabolique
Pour vérifier si ce changement énergétique pouvait être renversé, les chercheurs ont utilisé une grande base de données publique reliant les profils d’expression génique aux effets de milliers de composés. Ils ont recherché des médicaments prédits pour contrecarrer la signature métabolique des cellules leucémiques résistantes et ont retenu deux molécules : le radicicol, qui bloque une protéine chaperonne appelée HSP90, et l’omipalisib, qui inhibe la voie de signalisation PI3K/mTOR contrôlant la croissance et le métabolisme. Dans des tests en laboratoire, ces deux molécules ont non seulement ralenti la croissance des cellules résistantes, mais aussi réduit leur glycolyse excessive, normalisant la captation du glucose et la libération de lactate et diminuant l’expression des gènes liés à la glycolyse. Ces composés ont poussé les cellules leucémiques dans une phase de repos du cycle cellulaire et, dans le cas du radicicol, ont aussi déclenché une mort cellulaire programmée importante. En association avec le cabozantinib, l’omipalisib — et, dans un modèle, le radicicol — ont agi de manière synergique, facilitant l’élimination des cellules résistantes.
Ce que cela signifie pour les thérapies futures contre la leucémie
Pour les non‑spécialistes, le message est que les cellules leucémiques peuvent échapper à un médicament ciblé non seulement en mutant sa cible directe, mais aussi en modifiant leur façon de produire et d’utiliser l’énergie. L’étude montre que les cellules de LAM résistantes au cabozantinib adoptent une stratégie de « combustion du sucre » tout en négligeant leurs mitochondries. En ciblant les voies qui soutiennent ce métabolisme reconfiguré — par des médicaments comme l’omipalisib ou des inhibiteurs de HSP90 — il pourrait être possible de restaurer la sensibilité au cabozantinib et à des traitements similaires. Bien que ces résultats proviennent de modèles cellulaires et non de patients, ils suggèrent que l’association d’agents ciblés et d’anti‑métabolisme pourrait être une voie prometteuse pour retarder ou surmonter la résistance dans la LAM à mutation FLT3.
Citation: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
Mots-clés: leucémie aiguë myéloblastique, résistance aux médicaments, mutation FLT3, métabolisme du cancer, cabozantinib