Clear Sky Science · fr
La lipocaline-2 ostéocytaire régule localement la formation osseuse via la ferroptose dépendante du fer et la suppression de Wnt
Quand les cellules osseuses façonnent discrètement la santé de tout le corps
La plupart d’entre nous considèrent les os comme une charpente rigide, mais ils hébergent des cellules vivantes qui reconstruisent et réparent constamment notre squelette. Cette étude révèle comment une petite protéine produite par les cellules osseuses, appelée lipocaline-2, peut affaiblir silencieusement les os de l’intérieur en perturbant la gestion du fer et de l’énergie par les cellules. Comprendre ce processus caché pourrait ouvrir la voie à de nouveaux traitements contre l’ostéoporose et la perte osseuse liée à l’âge.
Une protéine messagère à double visage
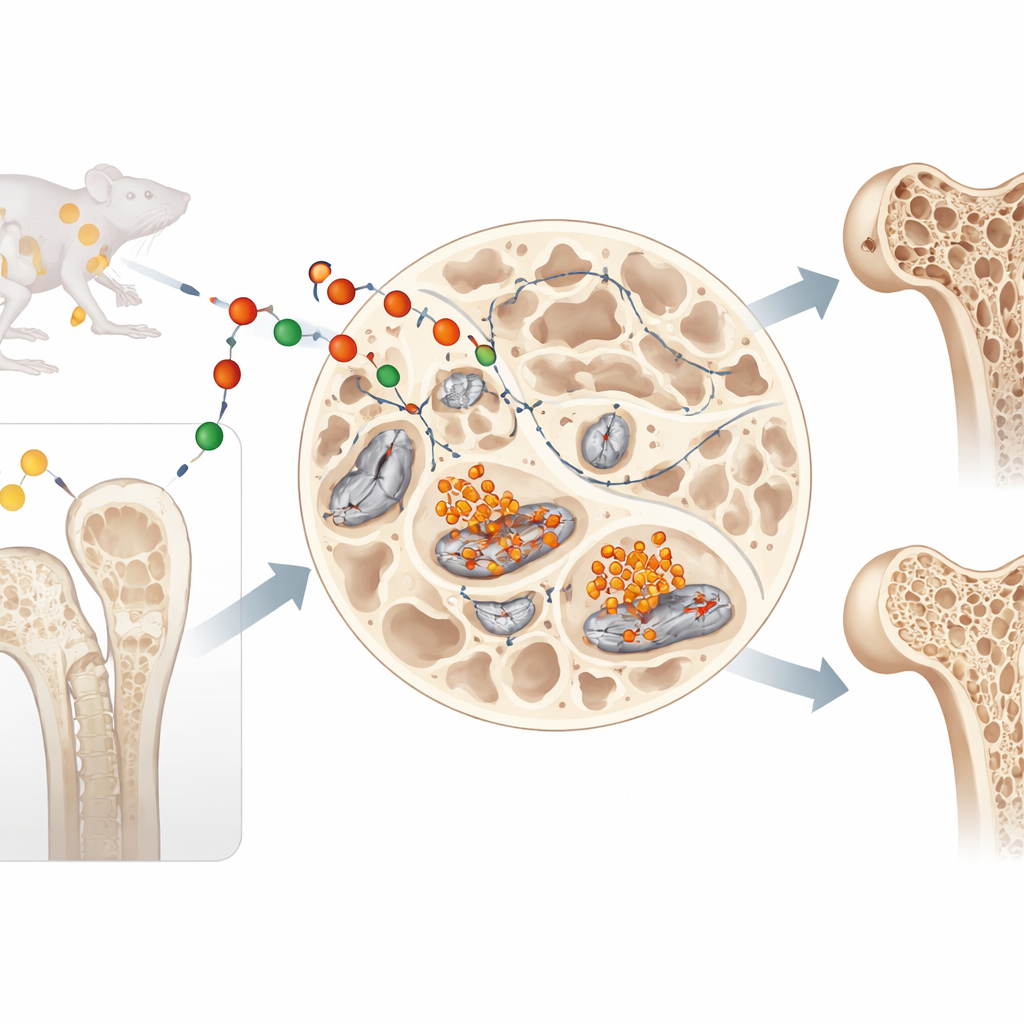
La lipocaline-2 est connue comme une hormone circulante qui voyage dans le sang, participe au contrôle de l’appétit et du poids corporel et défend contre l’infection en liant le fer. Mais les auteurs de cet article se sont posé une autre question : que fait la lipocaline-2 là où elle est produite, à l’intérieur même de l’os ? Ils se sont concentrés sur les ostéocytes, ces cellules de longue durée de vie enfouies dans l’os qui détectent les forces mécaniques et dirigent le remodelage osseux. L’équipe a constaté que les ostéocytes non seulement continuent de produire de la lipocaline-2 en mûrissant, mais augmentent même sa production, ce qui suggère un rôle local important au sein du squelette.
Surcharge en fer et une mort cellulaire semblable à la rouille
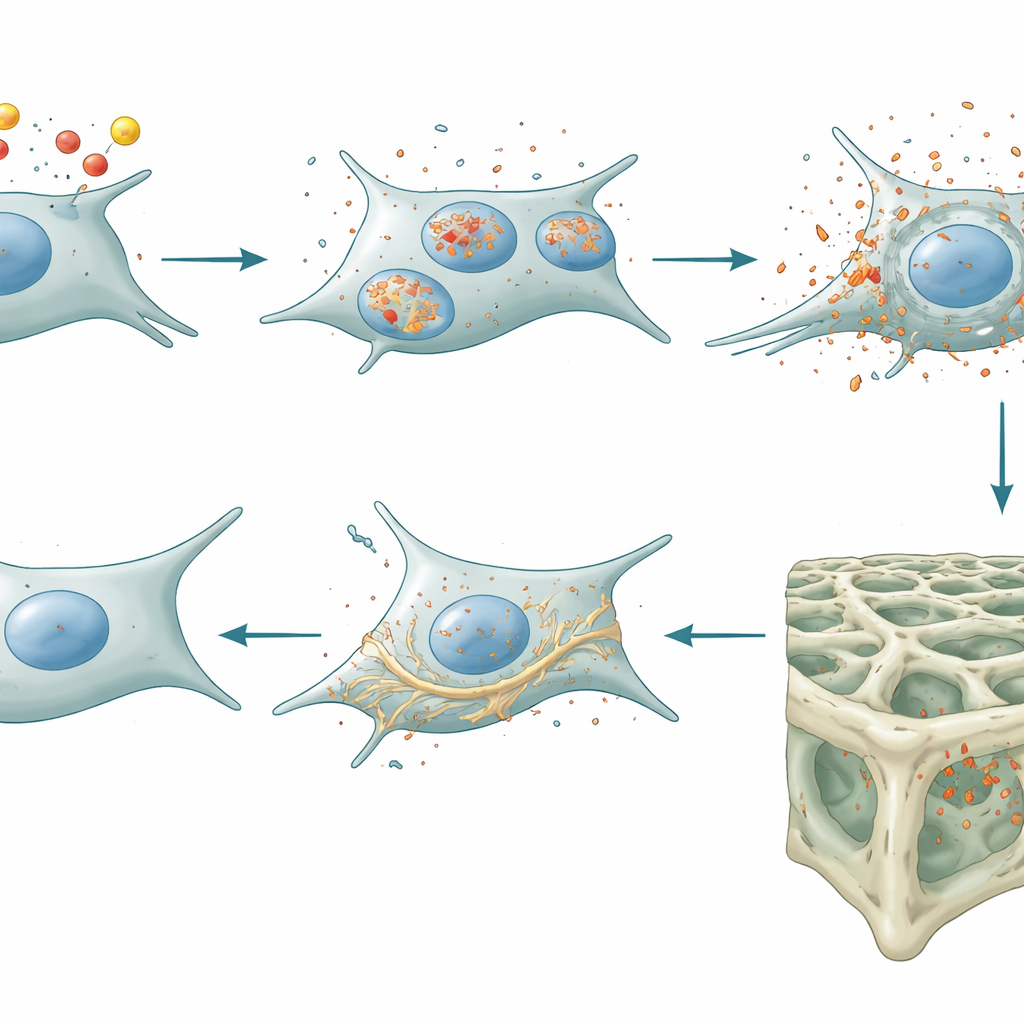
Parce que la lipocaline-2 peut transporter du fer, les chercheurs ont testé si elle favorisait l’accumulation de fer dans les ostéocytes. Dans des cultures de cellules osseuses, l’ajout de lipocaline-2 provoquait l’accumulation de fer à l’intérieur des cellules, augmentait les molécules réactives d’oxygène nocives et déclenchait de lourds dommages aux membranes riches en lipides. Ce sont des signes caractéristiques d’une forme de mort cellulaire récemment reconnue, appelée ferroptose, dans laquelle le fer agit un peu comme de la rouille en déclenchant des réactions chimiques destructrices. Bloquer le fer avec un agent chélateur a complètement prévenu les dommages et la mort cellulaire, confirmant que le processus dépendait du fer.
Le récepteur gardien et les conséquences mitochondriales
Pour comprendre comment la lipocaline-2 fait entrer sa cargaison de fer dans les ostéocytes, l’équipe s’est tournée vers un récepteur spécifique à la surface cellulaire, SLC22A17. Lorsqu’ils ont réduit l’expression de ce récepteur dans des cellules de type ostéocyte, la lipocaline-2 n’entraînait plus l’entrée de fer, le stress oxydatif ni la mort par ferroptose, même en conditions de surcharge en fer. L’étude a également montré que la lipocaline-2 compromet les centrales énergétiques de la cellule : les mitochondries. Un excès de lipocaline-2 faisait perdre à la membrane mitochondriale son potentiel normal et réduisait la production d’énergie, tandis que l’élimination de la lipocaline-2 restaurait la fonction mitochondriale. Chez des souris dont les ostéocytes étaient dépourvus de lipocaline-2, les gènes soutenant la respiration mitochondriale et le contrôle de la qualité mitochondriale étaient activés, suggérant que ces cellules étaient plus énergétiquement robustes.
Du stress cellulaire à l’os plus fragile, et comment lever le frein aide
Les chercheurs ont ensuite étudié des souris intactes génétiquement modifiées pour supprimer la lipocaline-2 spécifiquement dans les cellules en phase terminale de formation osseuse et les ostéocytes. Ces animaux accumulaient moins de fer à l’intérieur des cellules osseuses et présentaient des défenses antioxydantes renforcées contre la ferroptose. Surtout, ils produisaient des niveaux réduits de deux protéines clés — la sclérostine et DKK1 — qui agissent normalement comme des freins sur la voie Wnt/β-caténine, un moteur majeur de la formation osseuse. Avec ces freins relâchés, la signalisation favorisant les ostéoblastes formateurs d’os augmentait. Les micro-CT et les expériences de marquage osseux ont confirmé le résultat : les souris sans lipocaline-2 ostéocytaire formaient davantage d’os spongieux (trabéculaire) mieux connecté, principalement en augmentant la formation osseuse plutôt qu’en réduisant la résorption. Malgré ces changements squelettiques, leur poids corporel, le contrôle glycémique, le métabolisme et le niveau d’activité restaient normaux, montrant que l’effet était local à l’os plutôt qu’une action hormonale systémique.
Ce que cela signifie pour maintenir des os solides
En résumé, ce travail montre que la lipocaline-2 à l’intérieur des cellules osseuses fonctionne comme un interrupteur local qui augmente les niveaux de fer, met à mal les mitochondries, prédispose les cellules aux dommages par ferroptose et atténue une voie de croissance clé, limitant ainsi la formation osseuse nouvelle. Lorsqu’on supprime ce frein interne, les ostéocytes restent en meilleure santé, envoient davantage de signaux pro-formation et l’os trabéculaire devient plus dense et mieux connecté sans perturber le métabolisme global. Comme les niveaux de lipocaline-2 et le déséquilibre en fer augmentent avec l’âge et l’inflammation chronique, cibler le système lipocaline-2–récepteur pourrait offrir une nouvelle façon de protéger les os contre une « rouille » interne.
Citation: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
Mots-clés: santé osseuse, ostéocytes, métabolisme du fer, ferroptose, signalisation Wnt