Clear Sky Science · fr
La polymérase d’ADN kappa stabilisée par Ptbp2 interagit avec MRE11 et favorise l’instabilité génomique dans la leucémie
Comment les cellules leucémiques conservent l’ADN cassé et survivent quand même
Notre ADN est constamment attaqué, mais les cellules saines sont en général très efficaces pour détecter et réparer les lésions. Dans la leucémie, cependant, certaines cellules apprennent à vivre avec un ADN cassé et instable — et transforment même cette instabilité en avantage de survie. Cette étude révèle une « coopération » moléculaire entre une protéine d’épissage (Ptbp2), une enzyme spéciale de copie de l’ADN (la polymérase d’ADN kappa, ou Polk) et un capteur de dommages (MRE11) qui aide les cellules leucémiques à réparer juste assez de dégâts pour rester en vie, tout en accumulant le chaos génétique qui favorise la progression du cancer.
Un aide caché dans les cellules leucémiques
Les auteurs se sont concentrés sur la leucémie myéloïde chronique (LMC), un cancer du sang généralement provoqué par le gène de fusion BCR::ABL1. Si les médicaments modernes ciblant BCR::ABL1 sont efficaces en début de maladie, de nombreux patients en phase agressive dite « crise blastique » répondent mal. Des travaux antérieurs avaient montré que Ptbp2, une protéine qui se lie à l’ARN et influence le traitement des messages, est stimulée par BCR::ABL1 et agit comme un oncogène dans la LMC. Ici, l’équipe a découvert que Ptbp2 se fixe à l’extrémité 3′ non traduite (3′ UTR) de l’ARN messager de Polk et le protège de la dégradation. En conséquence, les cellules leucémiques produisent davantage de protéine Polk lorsque les niveaux de Ptbp2 sont élevés.
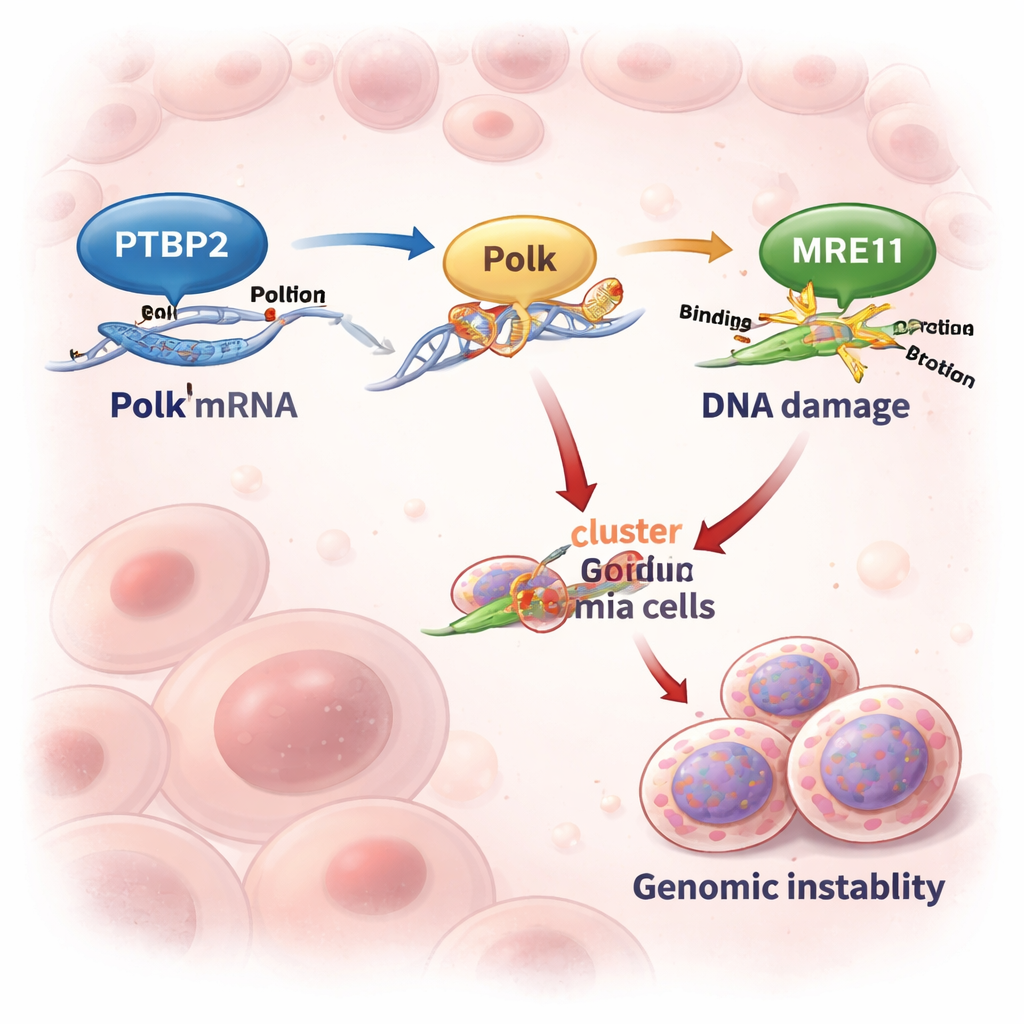
Activation d’une machine de copie de l’ADN sujette aux erreurs
Polk est une polymérase d’appoint qui peut recopier l’ADN endommagé quand la machinerie de réplication habituelle s’arrête. Cette capacité peut sauver des cellules stressées — mais au prix d’erreurs, car Polk est propice aux mutations. Dans des lignées cellulaires et des échantillons de patients en LMC avancée, les niveaux de Ptbp2 et de Polk variaient de concert. Lorsque les chercheurs ont supprimé Ptbp2 dans les cellules leucémiques, les niveaux de Polk ont chuté fortement et l’ARN de Polk s’est dégradé presque deux fois plus vite. La réintroduction de Polk dans des cellules déficientes en Ptbp2 a restauré leur comportement, montrant que le rôle principal de Ptbp2 ici est de maintenir Polk abondant et actif.
Réparer les dégâts — mais pas parfaitement
Pour évaluer l’effet de ce duo sur la réparation de l’ADN, les chercheurs ont traité les cellules par de l’hydroxyurée, un médicament qui bloque la réplication de l’ADN et est souvent utilisé chez les patients atteints de LMC. Les cellules dépourvues de Ptbp2 ont montré bien plus de dommages à l’ADN, visibles sous forme de longues « traînées de comète » et de foyers γH2AX intenses — des signes caractéristiques de chromosomes cassés. Ces cellules endommagées étaient plus susceptibles de mourir. En revanche, les cellules avec des taux élevés de Ptbp2 et de Polk toléraient mieux le médicament, réparaient les dégâts plus efficacement et survivaient, même si leur réparation était bâclée. La surexpression de Polk dans des cellules knock-out pour Ptbp2 a corrigé cette sensibilité, confirmant que le partenariat Ptbp2–Polk aide les cellules leucémiques à surmonter le stress de réplication et à éviter l’apoptose.
Un réseau de réponse aux dommages de l’ADN qui favorise l’instabilité
L’histoire ne s’arrête pas à Polk. L’équipe a montré que Polk interagit physiquement avec MRE11, un acteur clé du complexe MRN qui détecte les cassures d’ADN et active la voie de réponse aux dommages ATM–CHK2. Quand Ptbp2 était éliminé, Polk diminuait, les niveaux et l’activité de MRE11 déclinaient, et la signalisation ATM–CHK2 s’affaiblissait. La remise en place de Polk a restauré MRE11 et son activation. Des expériences détaillées sur la dynamique des fourches de réplication ont révélé que Ptbp2 et Polk aident à protéger les fourches arrêtées contre la dégradation, en grande partie via MRE11. Bloquer MRE11 par un médicament a compromis cette protection des fourches et accru les lésions d’ADN. Paradoxalement, les cellules avec une signalisation Ptbp2–Polk–MRE11 active accumulaient davantage d’anomalies chromosomiques, comme des échanges entre chromatides sœurs, des cassures, des lacunes, des fuseaux multipolaires et des cellules géantes multinoyautées — signes classiques d’instabilité génomique qui peuvent alimenter une forme plus agressive du cancer.
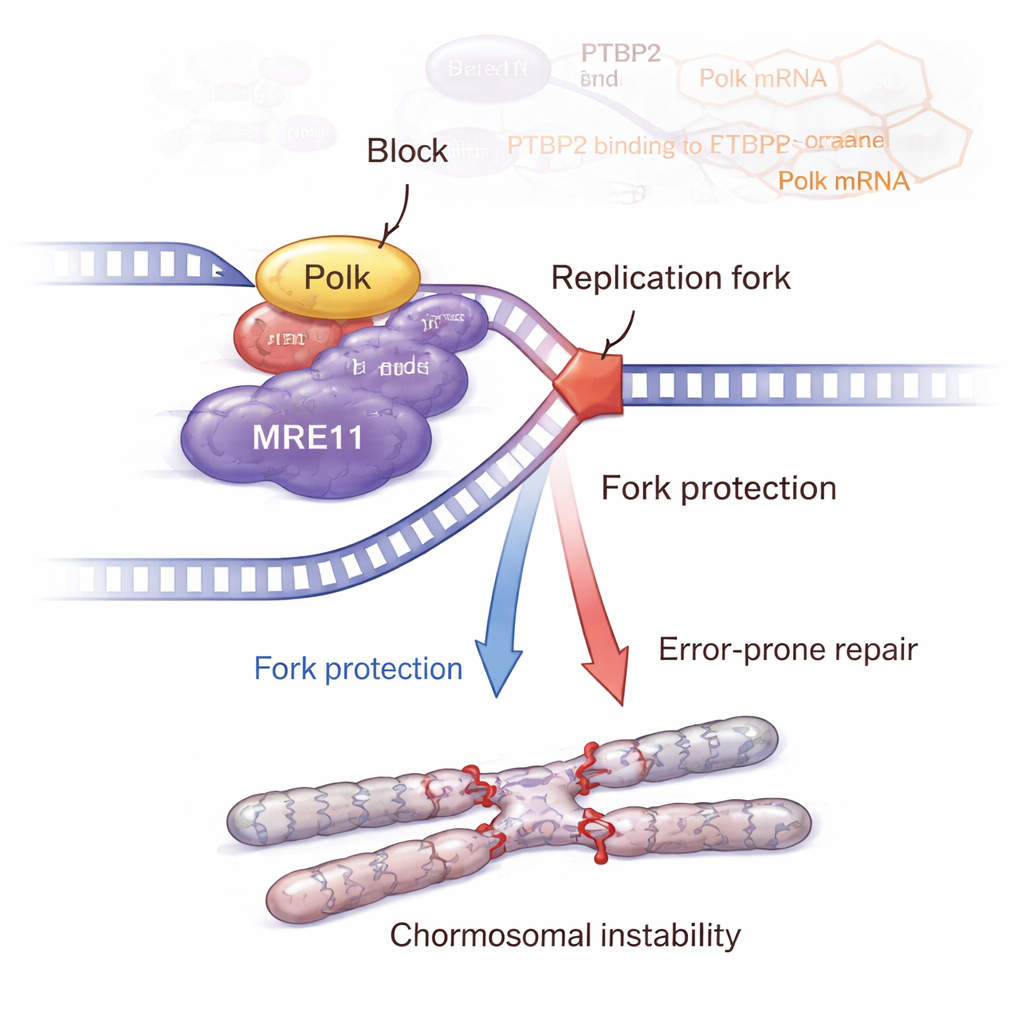
Des souris à de possibles nouveaux traitements
Chez la souris, les cellules leucémiques dotées de Ptbp2 ont donné des tumeurs plus volumineuses et plus anormales que les cellules privées de Ptbp2. Les tissus de ces animaux présentaient des niveaux accrus de Ptbp2, de Polk, du marqueur de prolifération Ki-67 et des structures de division cellulaire déformées. Dans un autre modèle murin de type LMC piloté par BCR::ABL1, l’ajout de Ptbp2 a renforcé Polk et augmenté le nombre de cellules en division atypiques et de foyers leucémiques infiltrants dans la rate et le foie, suggérant une progression plus rapide de la maladie. Ensemble, ces observations indiquent que l’axe Ptbp2–Polk–MRE11–ATM–CHK2 permet aux cellules leucémiques de survivre à un stress d’ADN intense tout en accumulant progressivement des mutations délétères.
Pourquoi cela compte pour les patients
Pour le grand public, le message clé est que certaines cellules leucémiques échappent au contrôle en marchant sur une corde raide : elles réparent leur ADN juste assez pour survivre, mais pas suffisamment pour éviter les mutations. Ptbp2 stabilise Polk, qui s’associe ensuite à MRE11 pour protéger l’ADN stressé et maintenir l’activation des signaux de dommage — pourtant cette réparation est imparfaite et favorise le désordre génétique. Comme la LMC avancée et d’autres cancers semblent dépendre de cet équilibre fragile, cibler Ptbp2 ou sa régulation de Polk pourrait faire pencher les cellules vers la mort plutôt que la survie, offrant une nouvelle piste thérapeutique prometteuse, notamment dans la difficile phase de crise blastique.
Citation: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Mots-clés: leucémie myéloïde chronique, instabilité génomique, réparation de l’ADN, polymérase d’ADN kappa, PTBP2