Clear Sky Science · fr
Exploiter les vulnérabilités des gliomes : cibler les voies de mort cellulaire régulée pour des thérapies innovantes
Pourquoi la mort des cellules tumorales cérébrales compte
Les gliomes font partie des tumeurs cérébrales les plus fréquentes et les plus mortelles chez l’adulte. Même après chirurgie, radiothérapie et chimiothérapie, ils rechutent souvent et sont difficiles à contrôler. Cette revue explore un nouvel angle d’attaque : exploiter les différentes manières dont les cellules peuvent être programmées pour mourir. En comprenant et en dirigeant ces voies d’« auto-destruction », les chercheurs espèrent révéler des faiblesses des cellules de gliome et rendre les traitements futurs plus efficaces et plus personnalisés.
Comment les gliomes déjouent les traitements standards
Les gliomes prennent naissance dans les cellules de soutien du cerveau et vont de formes à croissance lente à des formes très agressives comme le glioblastome. Leur mauvais pronostic résulte de plusieurs problèmes imbriqués : mutations génétiques, altérations épigénétiques, cellules souches résistantes, apport sanguin anormal et microenvironnement immunitaire fortement suppressif. De plus, la barrière hémato‑encéphalique limite l’accès des médicaments à la tumeur. Ensemble, ces facteurs permettent aux cellules tumorales de survivre à la chirurgie et aux traitements standards, de s’adapter au stress et, finalement, de repousser. 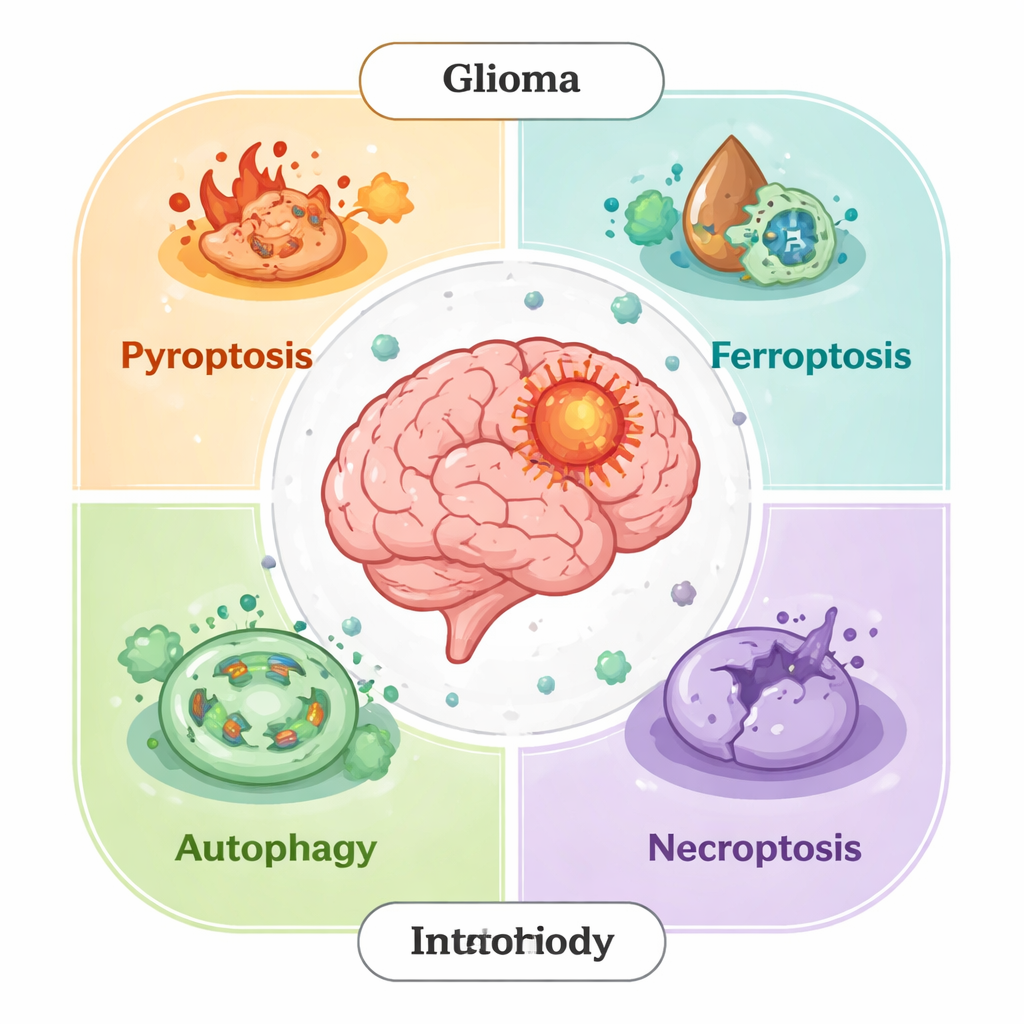
Les multiples visages de l’auto-destruction cellulaire
Pendant des décennies, les chercheurs se sont concentrés sur une forme principale de mort cellulaire programmée, l’apoptose. On sait aujourd’hui que ce n’est qu’une partie de l’histoire. Les cellules de gliome peuvent également mourir par d’autres voies régulées : la pyroptose (une explosion inflammatoire), la ferroptose (une atteinte membranaire entraînée par le fer), la nécroptose (une rupture cellulaire contrôlée) et la mort dépendante de l’autophagie (une autodigestion qui peut devenir létale). Dans les tissus sains, ces processus éliminent les cellules endommagées et préviennent le cancer. Dans les tumeurs, toutefois, les cellules de gliome réagencent souvent ces voies — en bloquant les signaux de mort, en renforçant les défenses antioxydantes ou en détournant l’autophagie en outil de survie — pour résister aux traitements et façonner un microenvironnement favorable à leur croissance.
Transformer les voies de mort en thérapie
Plutôt que de considérer ces voies comme un obstacle, les chercheurs apprennent à s’en servir comme d’armes. Les stratégies induisant la pyroptose utilisent des nanoparticules intelligentes, le chauffage par lumière, des virus modifiés ou des hydrogels chargés de médicaments pour faire gonfler, éclater les cellules de gliome et libérer des signaux de danger qui alertent le système immunitaire. Les approches fondées sur la ferroptose poussent les cellules tumorales à un effondrement alimenté par le fer en inhibant des enzymes protectrices clés comme GPX4, en perturbant la production de glutathion ou en modifiant la gestion des lipides par les cellules tumorales. Nombre de ces tactiques sont administrées avec des vecteurs avancés, y compris le graphdiyne et d’autres nanoparticules, pour aider les médicaments à traverser la barrière hémato‑encéphalique et se concentrer dans la tumeur tout en épargnant le tissu cérébral sain. 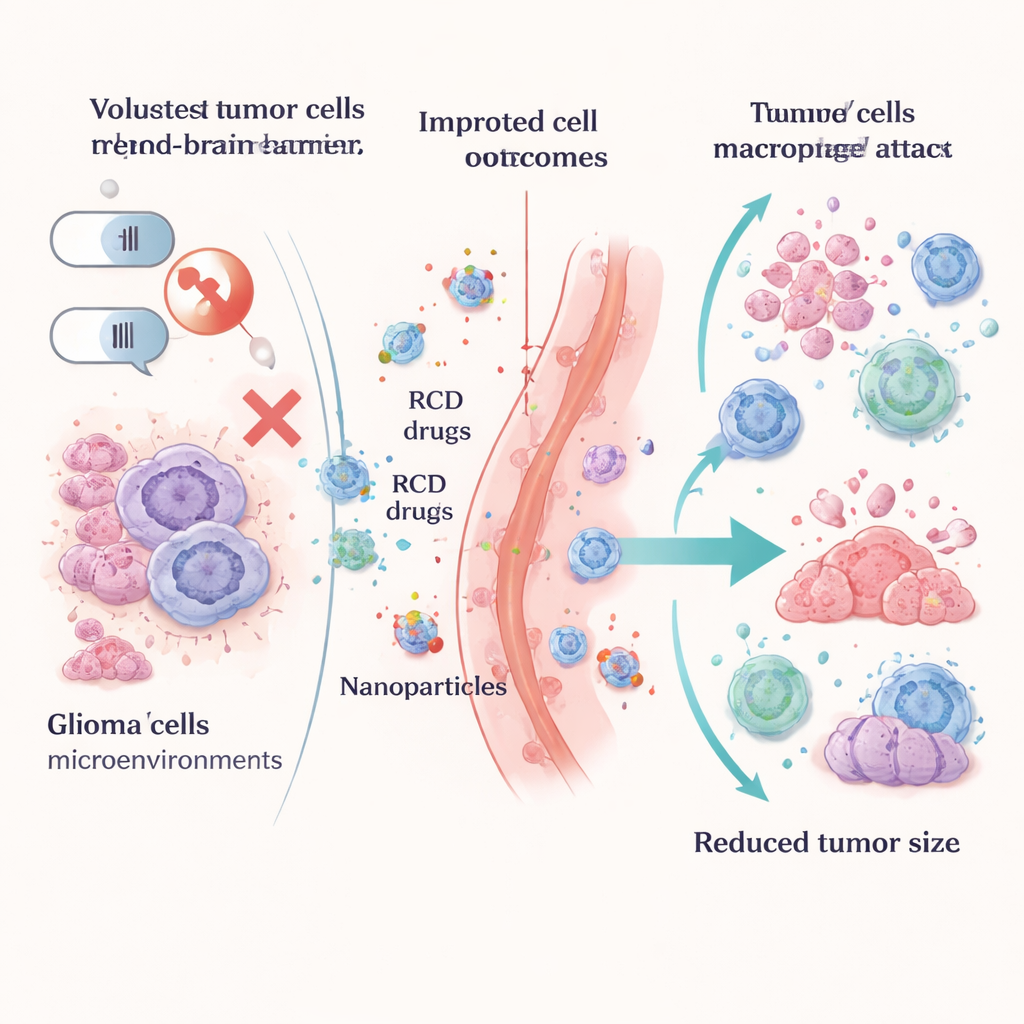
Reconfigurer le paysage immunitaire tumoral
Les thérapies axées sur la nécroptose visent à surmonter la résistance des cellules qui ne répondent plus aux signaux de mort classiques. Des produits naturels comme la shikonine, l’émodine et des dérivés de la célastrol peuvent entraîner les cellules de gliome en nécroptose, ce qui non seulement les tue mais libère aussi des molécules attirant les cellules immunitaires dans la tumeur. Parallèlement, les scientifiques explorent l’autophagie : parfois en la bloquant pour empêcher les cellules tumorales d’utiliser ce « nettoyage » pour survivre à la radio‑chimiothérapie, parfois en la poussant au‑delà de ses limites pour déclencher la mort cellulaire. Des essais cliniques précoces avec des médicaments comme la chloroquine et l’hydroxychloroquine montrent que l’autophagie peut être modulée en toute sécurité chez les patients, même si des bénéfices clairs sur la survie n’ont pas encore été démontrés.
Des découvertes en laboratoire aux soins personnalisés
La traduction de ces concepts en traitements concrets reste un défi. Les gliomes sont très hétérogènes d’un patient à l’autre, et au sein d’une même tumeur, de sorte qu’aucune stratégie fondée sur une seule voie de mort ne conviendra à tous. La barrière hémato‑encéphalique entrave toujours la délivrance des médicaments et le microenvironnement immunitaire peut atténuer même des combinaisons astucieuses de thérapies. Les auteurs soulignent des pistes prometteuses : associer des inducteurs de ferroptose à des inhibiteurs de points de contrôle immunitaires, combiner des virus oncolytiques avec des médicaments renforçant les signaux d’« avalez‑moi » des cellules cancéreuses, ou ajouter des modulateurs de l’autophagie à des schémas radio‑chimiothérapeutiques sélectionnés. Le profilage multi‑omique et de meilleurs biomarqueurs devraient aider à identifier les patients les plus susceptibles de bénéficier d’un mélange donné de stratégies.
Perspectives : amener les tumeurs à appuyer sur le bouton d’auto‑destruction
En termes simples, cet article conclut que l’avenir du traitement des gliomes pourrait résider dans la capacité à forcer les cellules tumorales à activer leurs propres mécanismes d’autodestruction de manière contrôlée. En apprenant à déclencher et à coordonner la pyroptose, la ferroptose, la nécroptose et la mort dépendante de l’autophagie — et en couplant ces approches aux immunothérapies modernes et à des systèmes de délivrance de précision — les chercheurs espèrent transformer un pronostic aujourd’hui sombre en un état plus gérable et, à terme, plus curable.
Citation: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
Mots-clés: gliome, mort cellulaire régulée, pyroptose, ferroptose, thérapie du glioblastome