Clear Sky Science · fr
Mitophagie dans le cancer du pancréas : aperçus mécanistiques et implications pour de nouvelles stratégies thérapeutiques
Pourquoi les centrales énergétiques de nos cellules comptent dans le cancer du pancréas
L’adénocarcinome canalaire du pancréas est l’un des cancers les plus meurtriers, en partie parce que les tumeurs apprennent rapidement à résister à presque tous les traitements. Cet article de synthèse explore un acteur surprenant dans cette histoire de résistance : la mitophagie, le système intégré de la cellule qui identifie et recycle les mitochondries usées, ces petites « centrales » produisant l’énergie. Comprendre comment le cancer du pancréas détourne ce processus de nettoyage pourrait ouvrir de nouvelles voies vers des thérapies plus efficaces et durables.
Les équipes de nettoyage cellulaires et les astuces de survie du cancer
Les mitochondries font bien plus que générer de l’énergie ; elles contribuent au contrôle du métabolisme, à la mort cellulaire et à la gestion des molécules nocives appelées espèces réactives de l’oxygène. Lorsque les mitochondries sont endommagées ou trop nombreuses, la cellule utilise la mitophagie pour les marquer et les éliminer. Cela peut se faire via deux voies principales. La première, connue sous le nom de voie PINK1/Parkin, dépend d’un capteur de dommages (PINK1) et d’une enzyme d’étiquetage (Parkin) pour marquer les mitochondries défectueuses en vue de leur destruction. L’autre utilise des protéines réceptrices telles que BNIP3, NIX et FUNDC1 situées à la surface des mitochondries pour les relier directement aux sacs d’élimination de la cellule, appelés autophagosomes, sans la même étape d’étiquetage. Ces voies fonctionnent souvent de concert, offrant aux cellules des moyens flexibles d’ajuster leurs réserves mitochondriales face au stress, comme l’hypoxie ou l’exposition aux médicaments. 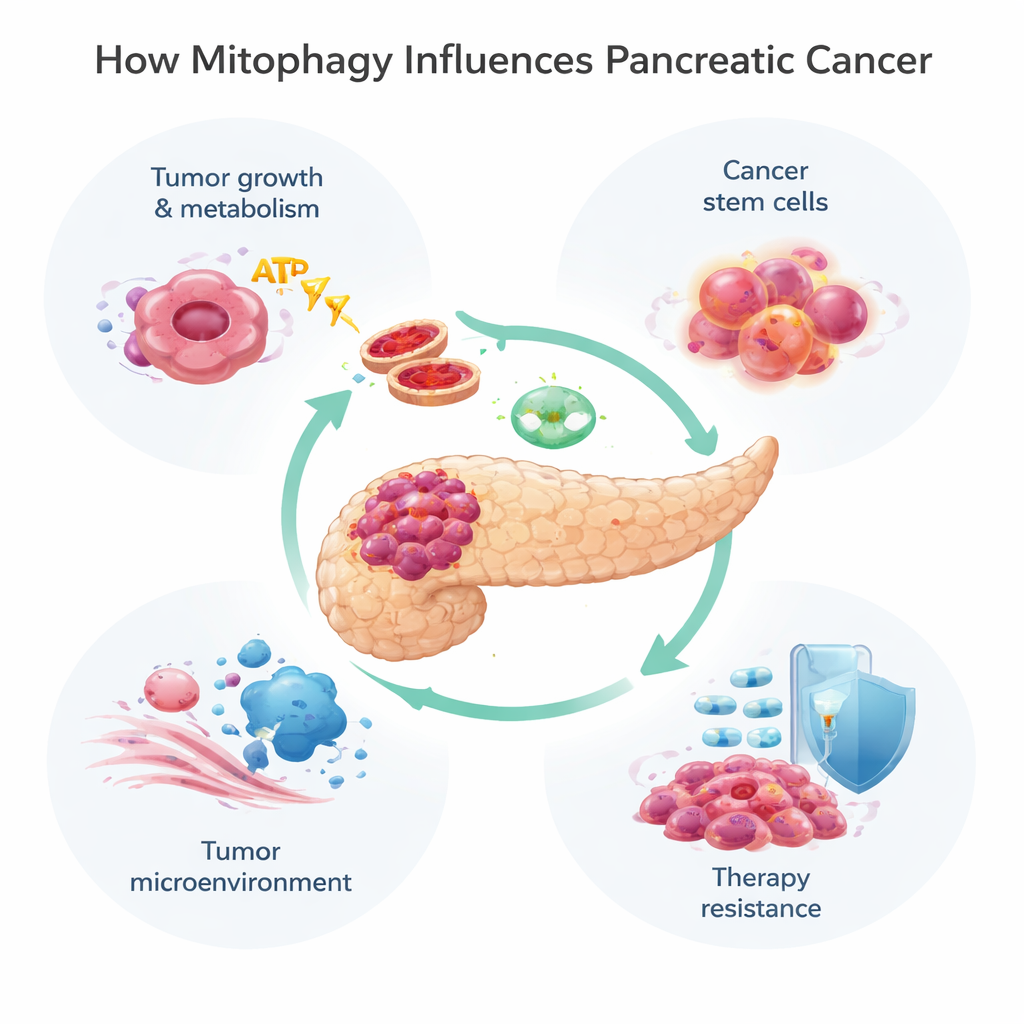
Comment les tumeurs pancréatiques remodèlent leur usage énergétique
Les tumeurs du pancréas vivent dans un environnement hostile : elles sont mal vascularisées et pauvrement oxygénées, et entourées d’un tissu dense semblable à une cicatrice. Pour survivre, les cellules cancéreuses reconfigurent leurs systèmes énergétiques, basculant souvent de la respiration mitochondriale dépendante de l’oxygène vers un processus plus primitif de combustion du sucre connu sous le nom de glycolyse. La mitophagie aide à peaufiner cette transition. Au cours du développement tumoral précoce, la perte de PINK1 ou Parkin accélère la formation du cancer en permettant l’accumulation de fer, un excès d’espèces réactives de l’oxygène et une poussée vers la glycolyse. Parallèlement, une autre protéine de mitophagie, NIX, peut aider à éliminer des mitochondries encore fonctionnelles, poussant les cellules davantage vers un métabolisme glycolytique et une croissance plus rapide. En revanche, BNIP3 montre un profil plus complexe : il apparaît précocement, est ensuite souvent silencieux dans de nombreuses tumeurs avancées, et lorsqu’il est réactivé peut ralentir la croissance des cellules cancéreuses, ce qui suggère que certaines voies de mitophagie freinent le cancer tandis que d’autres l’alimentent.
Cellules souches cancéreuses et microenvironnement tumoral
Toutes les cellules cancéreuses ne se valent pas. Un petit sous‑ensemble, souvent appelé cellules souches cancéreuses, peut s’auto‑renouveler, donner naissance à de nouvelles tumeurs et résister particulièrement bien à la chimiothérapie. Dans le cancer du pancréas, ces cellules dépendent de la mitophagie pour rester métaboliquement flexibles. Une protéine modifieuse appelée ISG15 soutient ce processus et aide à maintenir leurs traits de type souches, reliant directement la mitophagie à la rechute et à l’échec du traitement. Au‑delà des cellules cancéreuses elles‑mêmes, la mitophagie façonne aussi le microenvironnement tumoral — le mélange de cellules de soutien, de cellules immunitaires et de tissu conjonctif autour de la tumeur. Par exemple, les fibroblastes associés au cancer peuvent être entraînés dans un « effet Warburg inversé », où ils augmentent leur propre mitophagie et glycolyse, puis nourrissent la tumeur avec des sous‑produits riches en énergie. La mitophagie influence également la façon dont les cellules immunitaires reconnaissent et attaquent le cancer, en modifiant l’exposition de drapeaux immunitaires tels que le CMH‑I et des freins comme le PD‑L1 que les tumeurs utilisent pour se dissimuler.
Pourquoi bloquer ou stimuler le nettoyage peut modifier la réponse aux médicaments
De nombreux traitements standards et expérimentaux du cancer du pancréas, y compris la chimiothérapie par gemcitabine et un nouvel agent ciblé contre la mutation KRAS‑G12D fréquente, endommagent les mitochondries. Les cellules tumorales répondent souvent en activant la mitophagie, en éliminant les dommages et en échappant à la mort. Des études montrent que la mitophagie induite par PINK1 peut atténuer les effets létaux de la chimiothérapie et de certains composés naturels, permettant aux cellules cancéreuses de survivre. En revanche, dans certaines conditions, pousser excessivement la mitophagie — en particulier via BNIP3 et NIX — peut dépouiller les cellules d’un trop grand nombre de mitochondries fonctionnelles, les précipitant dans une crise énergétique et favorisant la mort cellulaire. Cette double nature signifie que la mitophagie peut soit protéger les tumeurs contre le traitement, soit, si elle est orientée correctement, les rendre plus vulnérables. 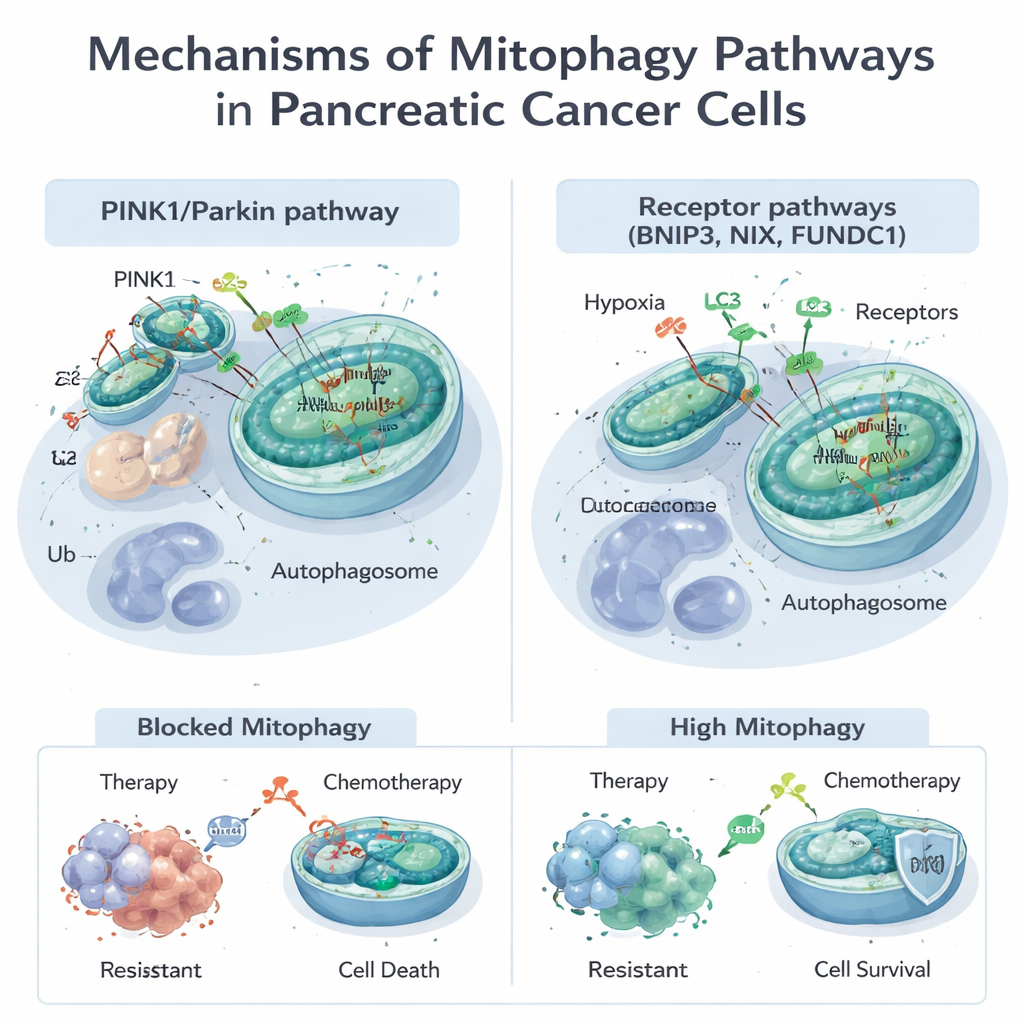
Nouvelles idées thérapeutiques et nécessité d’un meilleur appariement des patients
Parce que la mitophagie se situe au carrefour du métabolisme, des réponses au stress et de la mort cellulaire, elle constitue une cible intéressante pour les thérapies combinées. Les stratégies médicamenteuses actuelles agissent surtout de manière indirecte : certains composés interfèrent avec la fission et la fusion mitochondriales ; d’autres, comme la chloroquine et l’hydroxychloroquine, bloquent les derniers stades du processus de recyclage en empêchant la fusion des sacs de déchets avec les compartiments acides de dégradation. Plusieurs essais cliniques testent ces médicaments en association avec la chimiothérapie standard dans le cancer du pancréas. Pourtant, les résultats sont jusqu’ici mitigés — certains patients en tirent profit, d’autres non. Une partie du problème vient du fait que les tumeurs diffèrent largement dans leur niveau basal de mitophagie et leurs profils métaboliques : certaines dépendent fortement de la respiration mitochondriale, d’autres de la glycolyse. Les auteurs soutiennent que le succès futur dépendra de meilleurs biomarqueurs et signatures géniques pour regrouper les patients selon leur activité de mitophagie et leur utilisation énergétique, et du développement de médicaments plus précis qui ajustent sélectivement des voies de mitophagie spécifiques plutôt que d’activer ou d’inhiber bruyamment l’autophagie. Pour le grand public, l’idée principale est que savoir lire et moduler finement ce système de nettoyage mitochondrial pourrait aider à transformer le cancer du pancréas, d’un adversaire tenace, en une maladie plus contrôlable.
Citation: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Mots-clés: cancer du pancréas, mitophagie, mitochondries, résistance à la chimiothérapie, métabolisme tumoral