Clear Sky Science · fr
Des cellules souches mésenchymateuses « préparées » atténuent la fibrose liée à la schistosomiase en favorisant la conversion des sous‑types macrophagiques et l’efférocytose via l’axe Itgb2‑Rac1
Réduire les cicatrices hépatiques causées par un parasite courant
La schistosomiase, une maladie parasitaire qui touche plus de 200 millions de personnes dans le monde, laisse souvent des cicatrices tenaces dans le foie même après l’élimination des vers. Ces cicatrices, appelées fibrose, peuvent évoluer vers la cirrhose et une insuffisance hépatique potentiellement mortelle. Cette étude explore un nouveau traitement cellulaire qui apprend aux propres cellules immunitaires de l’organisme à mieux nettoyer les lésions, offrant une nouvelle approche pour inverser les cicatrices hépatiques induites par le parasite.
Pourquoi les cicatrices hépatiques sont difficiles à réparer
Lorsque les vers Schistosoma pondent des œufs dans le foie, le système immunitaire forme des amas cellulaires serrés — des granulomes — autour d’eux. Avec le temps, cette réponse protectrice dépose un excès de tissu cicatriciel, durcissant progressivement le foie. Un rôle central dans ce processus est joué par les macrophages, les équipes de nettoyage de l’organisme. Un sous‑type, qualifié d’« inflammatoire », alimente les lésions en libérant des signaux chimiques agressifs ; un autre, plus « résolvant », aide à décomposer la matrice cicatricielle et à calmer l’inflammation. La question centrale de ce travail est de savoir si l’on peut orienter en toute sécurité les macrophages de l’état nocif vers l’état réparateur.
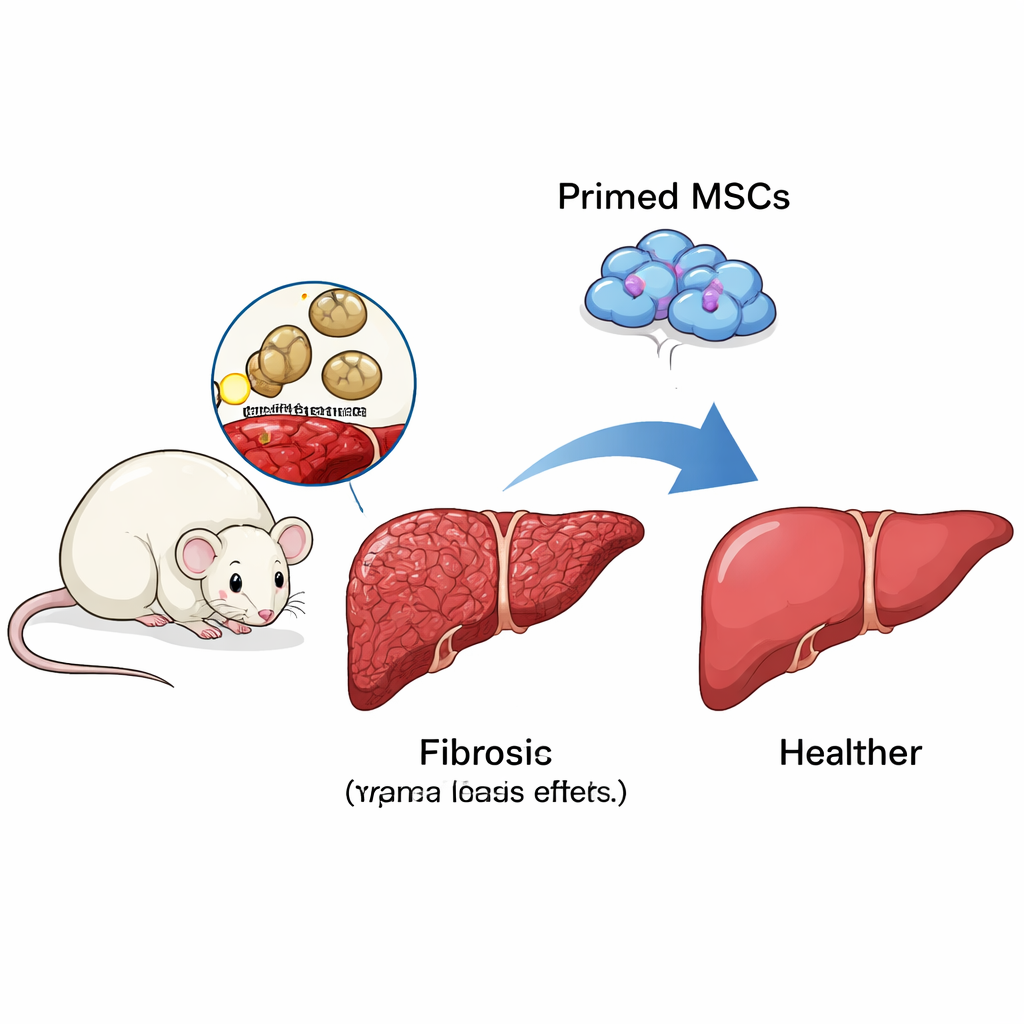
Former des cellules souches pour guider le système immunitaire
Les cellules souches mésenchymateuses (CSM) — des cellules polyvalentes présentes dans la moelle osseuse et d’autres tissus — ont suscité l’intérêt comme traitement potentiel de la fibrose hépatique. Isolées, elles ne donnent pas toujours de bons résultats. Les chercheurs ont constaté que le « préconditionnement » des CSM en laboratoire avec deux signaux immunitaires, IFN‑γ et LPS, améliorait considérablement leur efficacité chez des souris infectées par Schistosoma japonicum. Par rapport aux animaux non traités ou ayant reçu des CSM non préconditionnées, les souris ayant reçu des CSM préparées avaient des foies d’apparence plus saine, une prise de poids supérieure, et présentaient au microscope des granulomes beaucoup plus petits et une accumulation de collagène réduite. Les marqueurs des cellules activées qui forment la cicatrice ont également diminué, indiquant une réduction réelle de la fibrose et non de simples changements cosmétiques.
Reprogrammer l’équipe de nettoyage de l’organisme
En approfondissant l’analyse, l’équipe a mesuré l’effet des CSM préparées sur le comportement des macrophages. Dans les foies traités, le nombre de macrophages inflammatoires était moindre, tandis que la proportion du sous‑type pro‑résolvant, meilleur pour démanteler le tissu cicatriciel, augmentait. Parallèlement, les niveaux de molécules inflammatoires classiques ont chuté, alors que les facteurs favorables à la cicatrisation restaient dans une plage équilibrée plutôt que d’être poussés à l’excès. Lorsque les chercheurs ont bloqué l’arrivée de nouveaux macrophages inflammatoires dans le foie, tant le nombre de cellules résolvantes que les bénéfices sur la fibrose ont diminué. Cela suggère que les CSM préparées ne se contentent pas d’apporter de nouvelles cellules, mais convertissent au contraire les macrophages inflammatoires entrants en une forme plus pacifique et orientée réparation.
Aider les macrophages à « manger » pour mieux guérir
L’étude s’est ensuite intéressée à un processus appelé efférocytose — l’ingestion ordonnée de cellules en train de mourir, en particulier des neutrophiles épuisés, un autre type de cellule immunitaire. Chez les souris infectées traitées par CSM préparées, les macrophages hépatiques étaient bien plus souvent observés contenant des neutrophiles ingérés, signe d’un nettoyage actif. En culture, les macrophages exposés aux CSM préparées sont devenus meilleurs pour engloutir des neutrophiles apoptotiques marqués et, parallèlement, ont réorienté leur expression génétique vers un profil pro‑résolvant. Les chercheurs ont identifié une poignée moléculaire clé de ce changement : un récepteur appelé Itgb2 à la surface des macrophages, qui communique avec un interrupteur interne, Rac1, contrôlant le cytosquelette et le mouvement d’englobement de la cellule. Les CSM préparées ont renforcé l’activité d’Itgb2 et de Rac1 ; le blocage de l’un ou l’autre réduisait nettement l’efférocytose et annulait la bascule vers des macrophages de type réparateur.
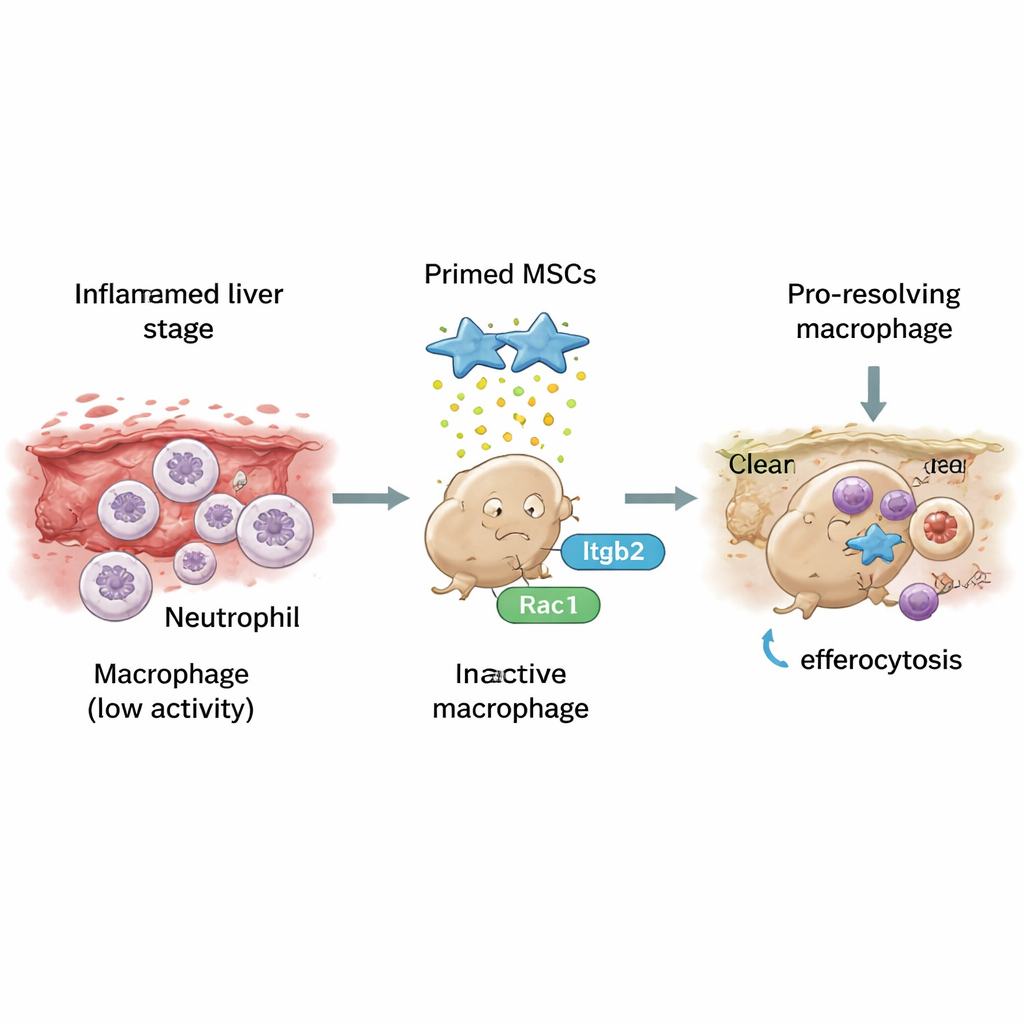
Ce que cela pourrait signifier pour les traitements futurs
Concrètement, ces travaux montrent que des cellules souches spécialement préparées peuvent agir comme des « entraîneurs » des cellules immunitaires après une schistosomiase, les incitant à cesser d’attiser l’inflammation et à débarrasser plus efficacement les débris et le tissu cicatriciel. En activant la voie Itgb2–Rac1, ces CSM préparées aident les macrophages à éliminer en douceur les cellules mourantes, puis à adopter un profil résolvant de la cicatrice. Bien qu’il reste beaucoup à faire avant d’essayer cette approche chez l’humain, l’étude fournit une feuille de route mécanistique claire pour concevoir des thérapies à base de CSM qui non seulement suppriment les lésions, mais aident activement le foie à se reconstruire après une infection parasitaire.
Citation: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
Mots-clés: schistosomiase, fibrose hépatique, cellules souches mésenchymateuses, macrophages, efférocytose