Clear Sky Science · fr
La phosphoprotéine ostéopontine dérivée du cancer colorectal reprogramme les macrophages en un état pro-métastatique M2 via l’axe PI3K/AKT/CSF1-CSF1R
Pourquoi cela compte pour les personnes atteintes d’un cancer du côlon
La plupart des décès dus au cancer colorectal (du côlon et du rectum) sont causés non pas par la tumeur primaire, mais par sa dissémination vers d’autres organes. Cette étude examine comment les cellules cancéreuses « dialoguent » avec les cellules immunitaires voisines pour favoriser la propagation tumorale. En dévoilant un message clé envoyé par les cellules cancéreuses pour reprogrammer les cellules immunitaires en complices plutôt qu’en combattantes, ce travail ouvre des pistes thérapeutiques susceptibles de ralentir ou d’interrompre les métastases dans les formes avancées du cancer colorectal.
Une protéine adhésive au côté sombre
Les chercheurs se sont concentrés sur une protéine appelée ostéopontine, ou OPN, produite à la fois par les cellules cancéreuses et par certains leucocytes présents dans les tumeurs. L’OPN est depuis longtemps associée à un mauvais pronostic dans de nombreux cancers, mais son rôle précis dans la promotion des métastases en cancer colorectal restait flou. En analysant de larges bases de données de patients et des échantillons tumoraux, l’équipe a constaté que les niveaux d’OPN étaient beaucoup plus élevés dans les tissus cancéreux colorectaux que dans le tissu colique normal, en particulier chez les patients atteints de maladie avancée et de métastases à distance. Les patients dont les tumeurs exprimaient davantage d’OPN présentaient généralement une survie plus courte, ce qui suggère que l’OPN est étroitement liée à des cancers agressifs et difficiles à traiter.
Ce ne sont pas seulement les cellules cancéreuses
De manière surprenante, lorsque les scientifiques ont forcé des cellules de cancer colorectal en culture à produire plus ou moins d’OPN, ces cellules ne sont pas devenues de manière autonome plus invasives ou mobiles. Leur croissance, leur migration et leur capacité à traverser des membranes artificielles ont peu changé. Cela remet en question l’idée commune selon laquelle l’OPN agirait principalement en renforçant directement les cellules cancéreuses. L’équipe s’est donc tournée vers le voisinage tumoral — le microenvironnement tumoral — et en particulier vers un groupe de cellules immunitaires appelées macrophages, qui peuvent soit attaquer les tumeurs (état « M1 »), soit les soutenir (état « M2 »).
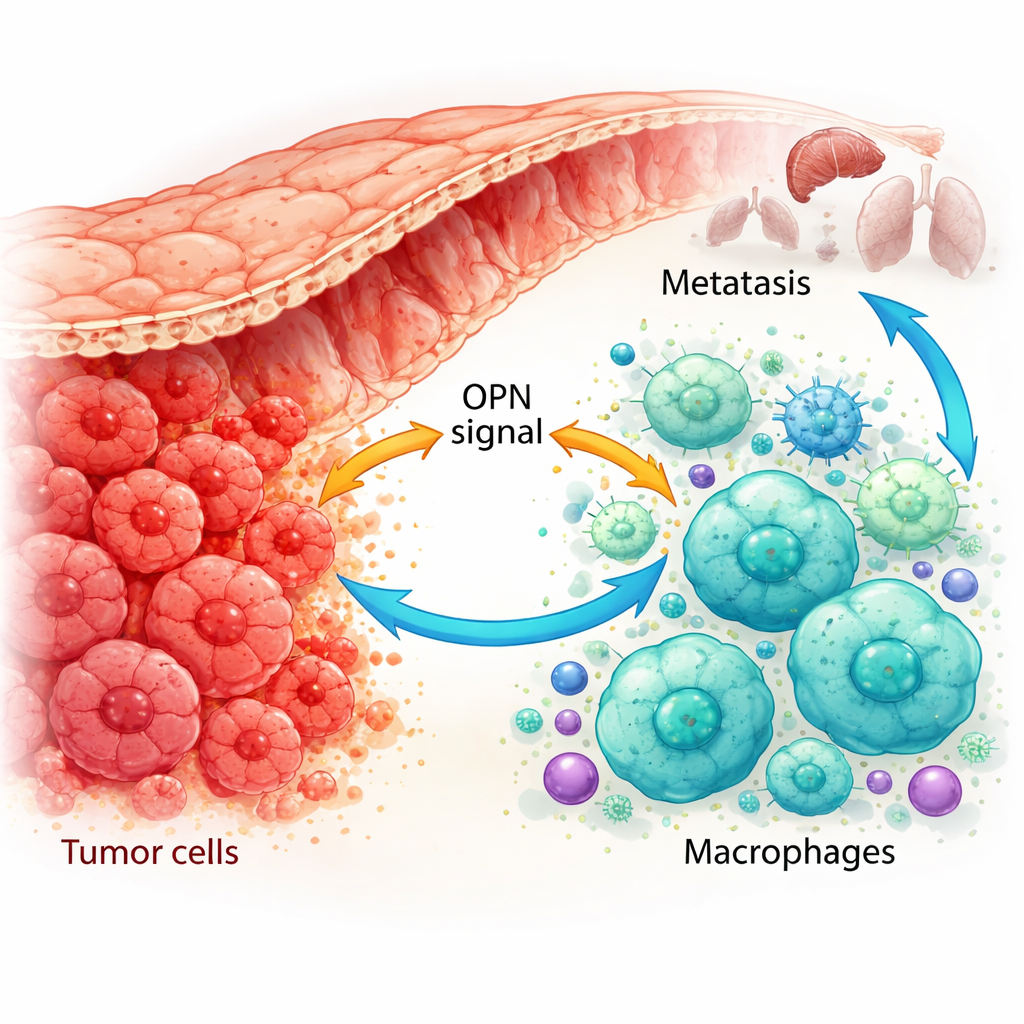
Comment les cellules immunitaires sont reprogrammées en aides tumoraux
Grâce à des cartographies génétiques unicellulaires et à des marquages avancés des tissus de patients, les chercheurs ont montré que l’OPN est produite non seulement par les cellules cancéreuses mais aussi par des macrophages associés à la tumeur. Dans les tumeurs ayant déjà métastasé, aussi bien les cellules cancéreuses qu’un sous-type spécifique de macrophages présentaient des niveaux élevés d’OPN. Ces macrophages avaient tendance à adopter un état de type M2, favorisant la tumeur, et étaient plus nombreux quand l’OPN tumorale était élevée. Dans des modèles murins, les tumeurs génétiquement modifiées pour produire plus d’OPN ont recruté davantage de ces macrophages de type M2 et ont crû plus rapidement, tandis que les tumeurs avec une OPN réduite hébergeaient moins de macrophages M2 et progressaient plus lentement. Cela suggère que l’OPN est un puissant agent de recrutement et de reprogrammation des macrophages dans l’environnement tumoral.
La chaîne de signalisation cachée : de l’OPN aux métastases
Pour élucider la chaîne moléculaire des événements, l’équipe a cultivé des macrophages humains en présence de cellules de cancer colorectal produisant des quantités variables d’OPN. Ils ont constaté que les cellules cancéreuses à forte expression d’OPN poussaient les macrophages vers l’état M2 et favorisaient un mouvement bidirectionnel : les macrophages migraient vers la tumeur, et les cellules tumorales devenaient plus invasives en réponse aux signaux émis par ces macrophages. En approfondissant, les scientifiques ont découvert que l’OPN active dans les macrophages une voie de signalisation appelée PI3K/AKT. Cette activation entraîne ensuite la libération par les macrophages de grandes quantités d’une autre molécule, le CSF1, et l’augmentation du récepteur correspondant, CSF1R, à leur surface. Le CSF1 agit alors en boucle pour renforcer l’état M2 pro-métastatique et continuer à attirer des macrophages dans la tumeur.
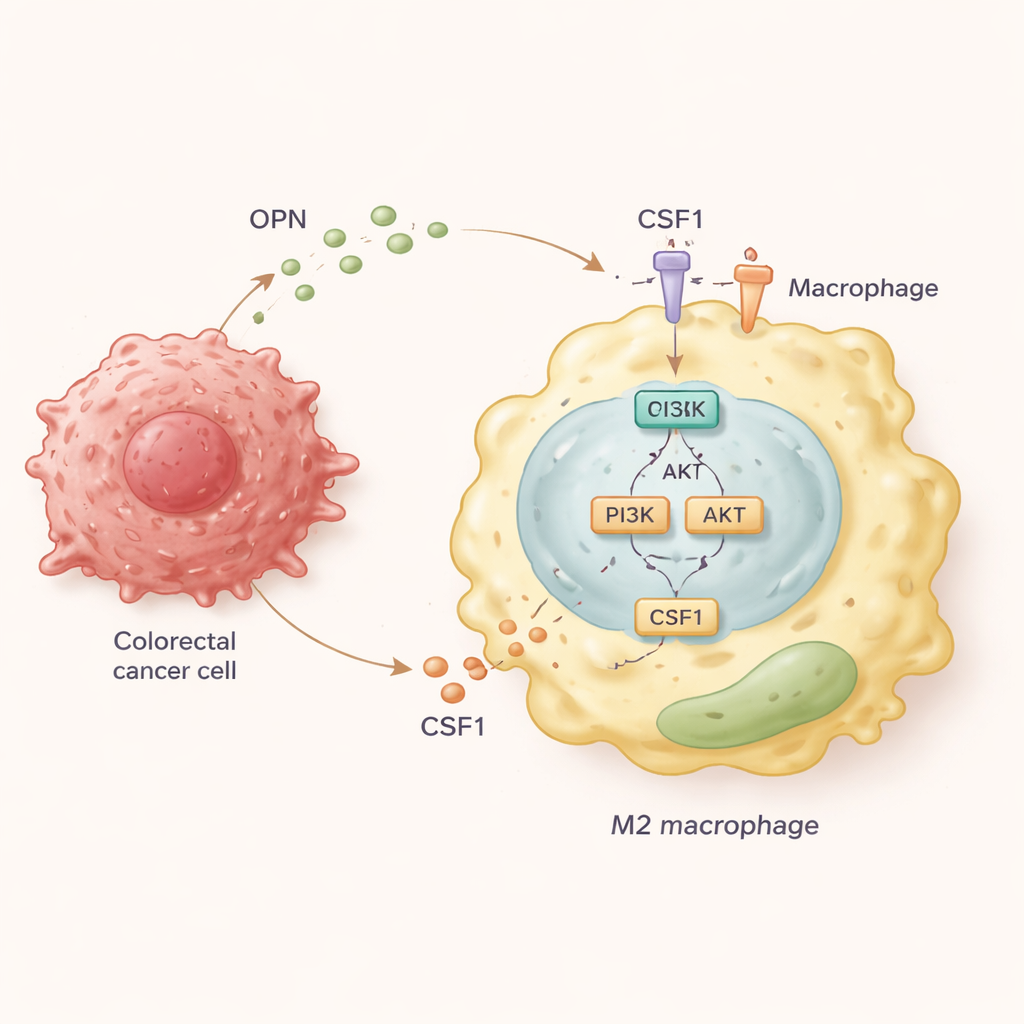
Bloquer la boucle pour ralentir la dissémination
Dans des modèles murins de cancer colorectal ayant diffusé dans l’abdomen, les chercheurs ont testé un médicament bloquant CSF1R nommé PLX3397. Les souris porteuses de tumeurs riches en OPN ont développé de nombreux nodules métastatiques, mais le traitement par l’inhibiteur de CSF1R a significativement réduit tant le nombre de métastases que la présence de macrophages de type M2 dans les tumeurs. Les cellules tumorales présentaient moins de croissance et davantage de signes d’apoptose. Il est important de noter que le médicament a principalement réduit les macrophages promoteurs de tumeur sans fortement affecter le type plus inflammatoire, ce qui suggère une manière relativement ciblée d’affaiblir le système de soutien tumoral.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, le message principal est que certains cancers colorectaux réussissent à se disséminer non seulement parce que les cellules cancéreuses sont agressives, mais parce qu’elles détournent les cellules immunitaires voisines et en font des complices. Dans cette étude, l’OPN d’origine tumorale agit comme un interrupteur maître qui reprogramme les macrophages via les voies de signalisation PI3K/AKT et CSF1/CSF1R, créant un terrain favorable aux métastases. En rompant cette chaîne — en particulier au niveau de CSF1R — les chercheurs ont pu réduire la propagation tumorale chez la souris. Cela suggère que la mesure des niveaux d’OPN pourrait aider à identifier les patients susceptibles de bénéficier de médicaments ciblant les macrophages, et que l’association de ces médicaments avec les traitements existants ou les immunothérapies pourrait offrir de nouvelles perspectives pour les personnes atteintes d’un cancer colorectal avancé.
Citation: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Mots-clés: cancer colorectal, ostéopontine, macrophages associés aux tumeurs, métastase, inhibition de CSF1R