Clear Sky Science · fr
Cibler la signalisation NXPH4/ALDH1L2 supprime la résistance à l’enzalutamide dans le cancer de la prostate
Pourquoi cela compte pour les patients atteints du cancer de la prostate
De nombreux hommes atteints d’un cancer de la prostate avancé dépendent d’un puissant médicament anti‑hormonal appelé enzalutamide. Au début il fonctionne souvent bien, réduisant les tumeurs et ralentissant la maladie. Mais chez la plupart des patients, le cancer finit par contourner le médicament et reprend sa croissance. Cette étude explore les mécanismes de cette échappée et met en lumière une nouvelle faiblesse des tumeurs résistantes — offrant une voie potentielle pour prolonger et améliorer l’efficacité des traitements existants.
Un traitement courant face à une maladie tenace
La croissance du cancer de la prostate est étroitement liée aux hormones masculines, les androgènes, qui agissent via une protéine appelée récepteur des androgènes. L’enzalutamide est conçu pour bloquer ce récepteur et constitue une thérapie standard lorsque les tumeurs ne répondent plus aux traitements traditionnels visant à abaisser les hormones. Malheureusement, de nombreuses tumeurs s’adaptent et deviennent ce que les médecins appellent un cancer de la prostate résistant à la castration. Les auteurs de ce travail ont cherché à identifier quels gènes aident les cellules cancéreuses à survivre à l’enzalutamide, en espérant que bloquer ces facilitateurs pourrait restaurer l’efficacité du traitement.
Mise en évidence d’une molécule auxiliaire surprenante
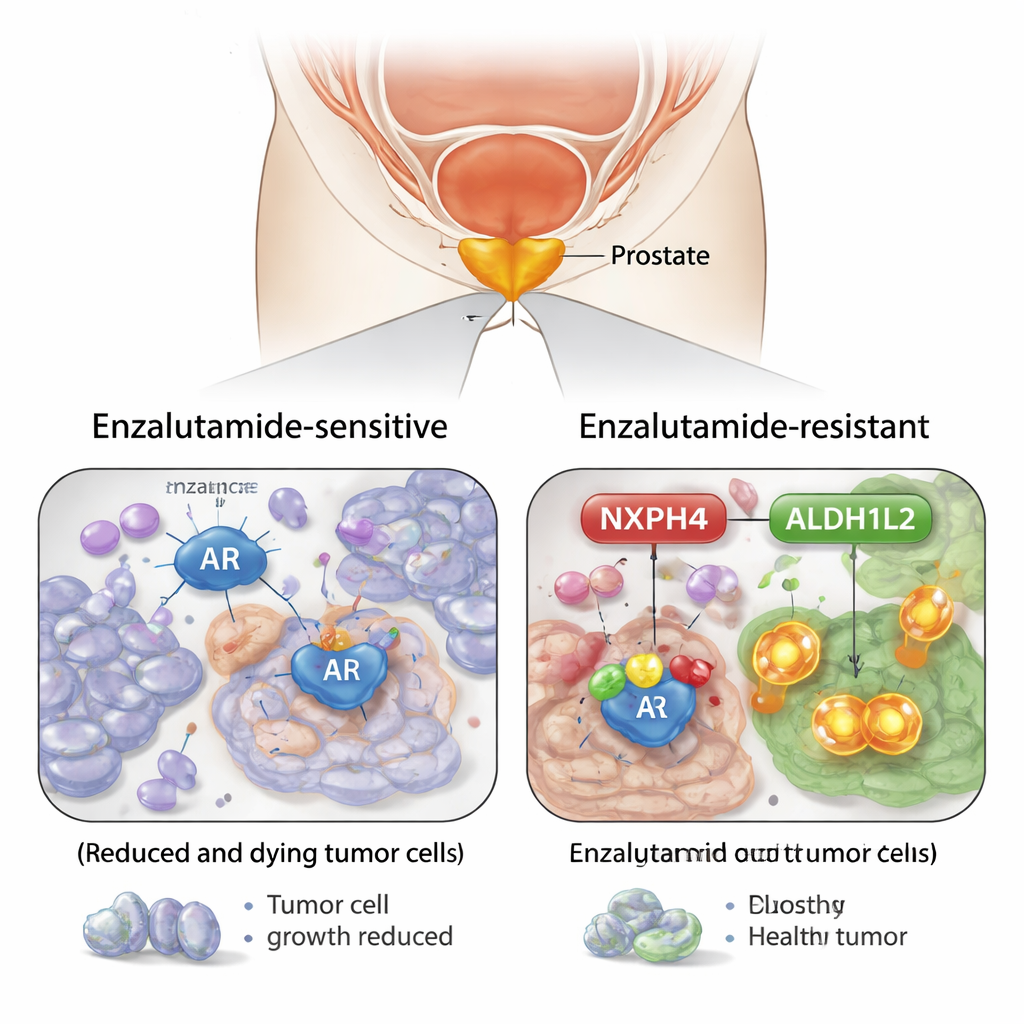
En comparant des cellules de cancer de la prostate sensibles à l’enzalutamide avec des cellules devenues résistantes, l’équipe a identifié une protéine appelée NXPH4 comme acteur clé. Les cellules résistantes produisaient beaucoup plus de NXPH4, et son niveau augmentait progressivement lorsque les cellules étaient exposées à l’enzalutamide au fil du temps. Des échantillons de tissus patients montraient le même schéma : davantage de NXPH4 dans les tumeurs plus agressives et dans les cancers qui ne répondaient plus au médicament. Lorsque les chercheurs ont réduit les niveaux de NXPH4 dans les cellules résistantes, celles‑ci sont devenues plus faciles à éliminer avec l’enzalutamide et ont formé moins de colonies, tant en culture qu’en souris. À l’inverse, forcer la production de NXPH4 rendait les cellules plus difficiles à traiter.
Comment les hormones activent NXPH4
L’étude a aussi cherché pourquoi NXPH4 est si abondant dans ces tumeurs. La réponse renvoie encore au récepteur des androgènes. Les chercheurs ont montré que lorsque les cellules étaient traitées par la dihydrotestostérone, les niveaux de NXPH4 augmentaient. En ajoutant un excès de récepteur des androgènes, NXPH4 augmentait ; en bloquant le récepteur, NXPH4 diminuait. Des expériences détaillées sur l’ADN ont confirmé que le récepteur des androgènes se lie physiquement à la région de contrôle du gène NXPH4, l’activant. Cela signifie que le même système piloté par les hormones qui alimente la croissance du cancer de la prostate prépare aussi les cellules via NXPH4, préparant le terrain pour la résistance au médicament.
Renforcer les centrales énergétiques de la cellule
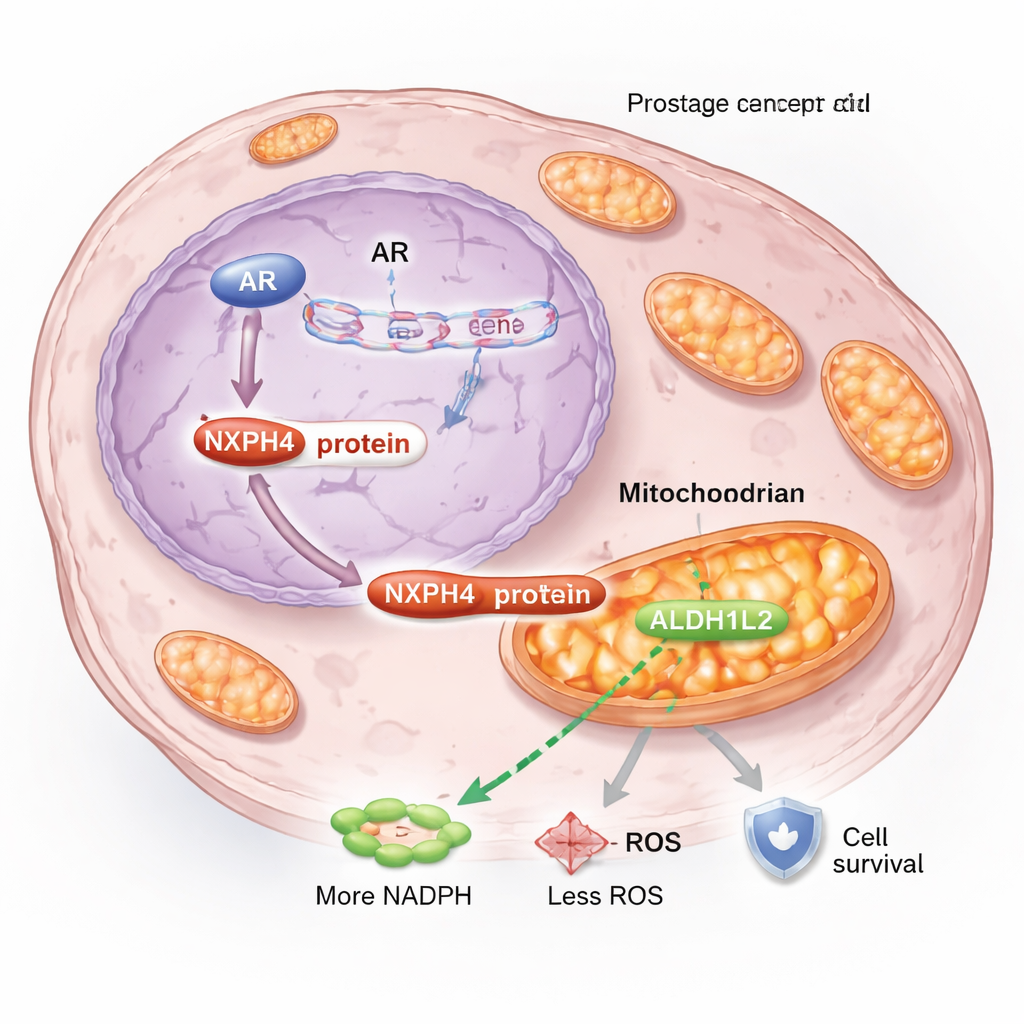
En creusant davantage, l’équipe a découvert que NXPH4 modifie la manière dont les cellules cancéreuses gèrent l’énergie et le stress au sein de leurs mitochondries, ces petites centrales de la cellule. Dans des conditions de blocage hormonal, une partie de NXPH4 migre vers les mitochondries et se lie à une autre protéine, ALDH1L2, qui est cruciale pour la production de NADPH, une molécule clé pour contrôler les espèces réactives de l’oxygène (ROS). Dans les cellules résistantes, NXPH4 et ALDH1L2 forment un complexe qui stimule la respiration mitochondriale, maintient le potentiel de membrane, augmente le NADPH et réduit les niveaux de ROS. Cette combinaison préserve la santé mitochondriale et permet aux cellules cancéreuses de supporter le stress induit par l’enzalutamide, au lieu de mourir comme elles le feraient normalement.
Rompre le circuit de résistance
Lorsque les chercheurs ont perturbé ce système de soutien mitochondrial, les résultats furent spectaculaires. L’inhibition de NXPH4 dans les cellules résistantes a réduit l’activité mitochondriale, augmenté le stress oxydatif, ralenti la croissance et rendu les cellules beaucoup plus sensibles à l’enzalutamide. Le silence d’ALDH1L2 produisait un effet similaire et annulait les bénéfices protecteurs d’un excès de NXPH4, confirmant que ces deux protéines agissent en partenariat. Chez la souris, les tumeurs dépourvues de NXPH4 croissaient plus lentement, et la combinaison de la perte de NXPH4 avec l’enzalutamide réduisait les tumeurs davantage que chaque approche prise séparément. Ces résultats suggèrent que le partenariat NXPH4–ALDH1L2 n’est pas un simple effet secondaire de la résistance mais en est un moteur.
Ce que cela pourrait signifier pour les traitements futurs
En résumé, ce travail montre que certains cancers de la prostate survivent à l’enzalutamide en reconfigurant leur approvisionnement énergétique. NXPH4, activé par le récepteur des androgènes, s’associe à ALDH1L2 dans les mitochondries pour les maintenir actives, protéger contre les dommages oxydatifs et aider les cellules tumorales à résister à la thérapie anti‑hormonale. Cibler NXPH4, ou son interaction avec ALDH1L2, pourrait affaiblir ce circuit de survie. Bien qu’il n’existe pas encore de médicaments ciblant NXPH4, l’étude souligne ce couple de molécules comme une nouvelle cible prometteuse. À l’avenir, combiner l’enzalutamide avec des médicaments perturbant la signalisation NXPH4‑ALDH1L2 pourrait aider les patients à mieux contrer la progression d’un cancer de la prostate résistant et plus durablement.
Citation: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
Mots-clés: cancer de la prostate, résistance à l’enzalutamide, métabolisme mitochondrial, NXPH4, ALDH1L2