Clear Sky Science · fr
La rottlerine déclenche une double dégradation de SLC7A11 et GPX4 pour induire la ferroptose et sensibiliser chimiquement le carcinome hépatocellulaire
Pourquoi ce composé naturel est important pour le cancer du foie
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer primitif du foie, est souvent diagnostiqué tardivement et reste difficile à traiter. Cette étude explore si une molécule d’origine végétale appelée rottlerine, connue depuis longtemps pour ses larges effets anticancéreux, peut être exploitée pour déclencher une forme plus récente de mort cellulaire appelée ferroptose dans les cellules du cancer du foie. En comprenant le mode d’action moléculaire de la rottlerine, les chercheurs espèrent ouvrir de nouvelles voies vers des traitements plus efficaces et moins facilement contournables.
Une nouvelle manière d’éliminer les cellules cancéreuses
Les médicaments anticancéreux classiques poussent généralement les cellules tumorales vers des programmes de mort bien connus, comme l’apoptose. La ferroptose est différente : c’est un processus dépendant du fer, provoqué par l’accumulation de lipides toxiques dans les membranes cellulaires. Les cellules du cancer du foie sont particulièrement vulnérables à ce type de dommage parce qu’elles dépendent fortement de systèmes antioxydants pour contenir ces toxines lipidiques. L’équipe s’est demandé si la rottlerine pouvait saboter ces défenses et ainsi forcer les cellules du foie cancéreuses à subir la ferroptose.
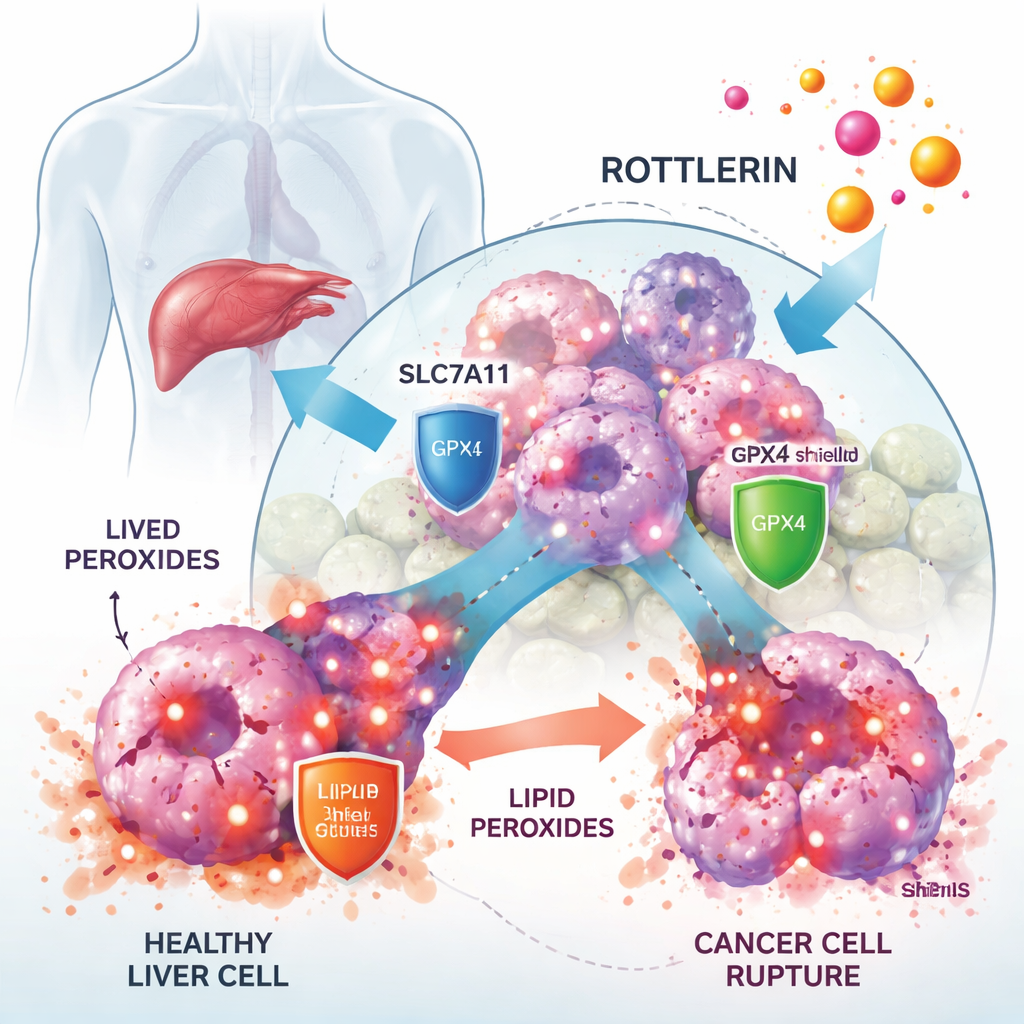
Comment la rottlerine freine la croissance tumorale
En travaillant sur des lignées cellulaires humaines de cancer du foie, les chercheurs ont montré que la rottlerine réduisait fortement la croissance des cellules cancéreuses à des doses micromolaires faibles, tandis que les cellules hépatiques normales étaient moins affectées. Lorsqu’ils ont ajouté un bloqueur spécifique de la ferroptose, le Ferrostatin‑1, une grande partie de la mortalité cellulaire induite par la rottlerine a été évitée, ce qui suggère fortement que la ferroptose était le principal mode d’action. La microscopie et des tests biochimiques confirment ces observations : les cellules traitées par la rottlerine accumulaient des niveaux élevés de peroxydes lipidiques, présentaient des mitochondries altérées et montraient des quantités réduites de glutathion, molécules antioxydantes, autant de signes caractéristiques de la ferroptose.
Désarmer les boucliers antioxydants des cellules
Les cellules du cancer du foie survivent en s’appuyant sur un axe de défense critique composé du transporteur SLC7A11 et de l’enzyme GPX4. SLC7A11 importe la cystine, un composant nécessaire à la synthèse du glutathion, tandis que GPX4 utilise le glutathion pour neutraliser les peroxydes lipidiques avant qu’ils n’endommagent les membranes. L’étude a montré que la rottlerine entraînait, au fil du temps, une diminution des niveaux protéiques de SLC7A11 et de GPX4. Ce n’était pas parce que la synthèse de ces protéines cessait, mais parce qu’elles étaient marquées par de petites étiquettes « détruisez‑moi » (ubiquitine) et envoyées dans la machinerie de dégradation des protéines de la cellule, le protéasome. Bloquer le protéasome inversait cette perte, et augmenter artificiellement SLC7A11 ou GPX4 dans les cellules les protégeait partiellement de la rottlerine. Ensemble, ces résultats montrent que la rottlerine agit comme un dégradeur double de deux défenses centrales contre la ferroptose.
Renforcer les médicaments existants contre le cancer du foie
De nombreux patients atteints d’un cancer du foie avancé reçoivent du sorafénib, un médicament de première ligne qui peut lui‑même induire la ferroptose, mais la résistance limite souvent son efficacité. Les auteurs ont testé si des doses faibles, par ailleurs inefficaces, de rottlerine pouvaient rendre les cellules tumorales plus sensibles aux médicaments inducteurs de ferroptose tels que le sorafénib et le RSL3. En culture cellulaire, la combinaison de faibles doses de rottlerine avec l’un ou l’autre de ces médicaments augmentait nettement la mortalité des cellules cancéreuses et modifiait les courbes dose‑réponse, indiquant une puissance accrue. Fait important, cet effet sensibilisant persistait même lorsque la protéine cible classique de la rottlerine, la PKCδ, était génétiquement réduite, montrant que l’action clé ne passait pas par cette kinase mais par la dégradation de SLC7A11 et GPX4. Dans des modèles murins portant des tumeurs hépatiques humaines, le traitement combiné rottlerine plus sorafénib ralentissait davantage la croissance tumorale que le sorafénib seul et abaissait encore les niveaux de SLC7A11 et GPX4 dans les tumeurs.
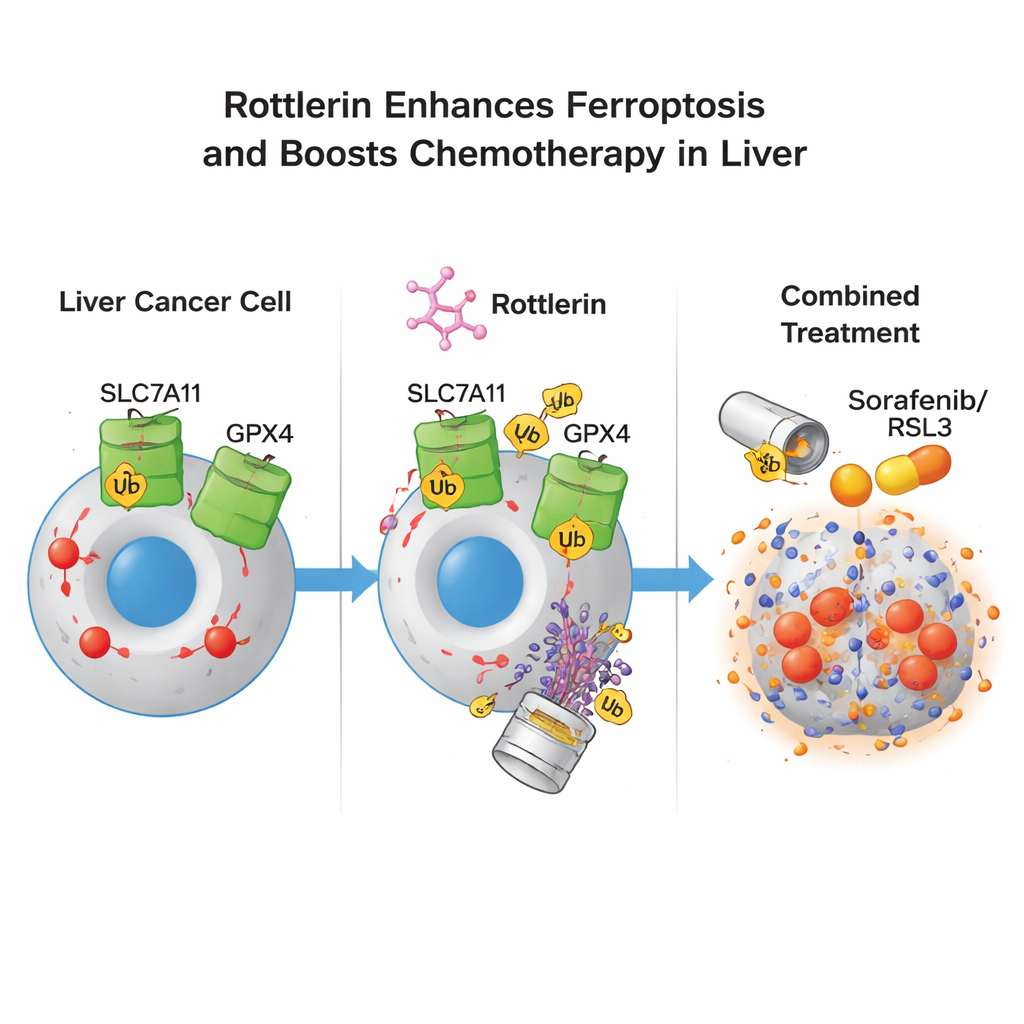
Ce que cela pourrait signifier pour les traitements futurs
Pour un public non spécialiste, le message est que la rottlerine agit comme un « pique‑serrures à deux goupilles » sur les cellules du cancer du foie : elle supprime simultanément deux verrous cruciaux—SLC7A11 et GPX4—qui protègent normalement les cellules d’une vague létale d’oxydation lipidique. Une fois ces verrous retirés, les cellules cancéreuses sont beaucoup plus susceptibles de subir la ferroptose, en particulier lorsqu’on les associe à des médicaments existants qui favorisent ce processus. Bien que des travaux supplémentaires soient nécessaires avant que la rottlerine ou des composés apparentés puissent être utilisés chez l’homme, cette stratégie de dégradation double offre une voie prometteuse pour déjouer les défenses adaptatives qui rendent souvent les tumeurs hépatiques si difficiles à traiter.
Citation: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Mots-clés: cancer du foie, ferroptose, rottlerine, SLC7A11, GPX4