Clear Sky Science · fr
Activation de GCN2 puis de la réponse au repliement des protéines par la petite molécule orale NXP800 ralentit la croissance tumorale dans l’ostéosarcome
Transformer le stress du cancer en faiblesse
L’ostéosarcome est un cancer osseux rare mais agressif qui touche principalement les enfants et les jeunes adultes. Pendant des décennies, le traitement a reposé sur des chimiothérapies intensives et la chirurgie, pourtant la survie des patients atteints de formes avancées a peu progressé. Cette étude examine une nouvelle pilule, appelée NXP800, qui cherche à exploiter une faiblesse cachée des cellules cancéreuses : leur lutte permanente contre le stress intracellulaire. En poussant ce stress au-delà d’un point critique, NXP800 pourrait forcer les cellules tumorales à s’auto-détruire tout en épargnant la plupart des cellules saines.
Un cancer osseux tenace en quête de nouvelles options
L’ostéosarcome se développe en général dans les os longs des bras et des jambes et peut se propager rapidement aux poumons. Le traitement standard associe plusieurs agents chimiothérapeutiques puissants à une chirurgie visant à retirer la tumeur. Si cette stratégie guérit de nombreux patients atteints d’une maladie localisée, les perspectives restent mauvaises pour ceux dont la tumeur récidive ou s’est déjà métastasée au moment du diagnostic. Comme les médicaments actuels ont atteint leurs limites, les chercheurs cherchent des thérapies qui attaquent l’ostéosarcome de façon totalement nouvelle, idéalement en ciblant des caractéristiques qui distinguent les cellules cancéreuses des tissus normaux.
Mettre le stress au service de l’élimination des cellules tumorales
Les cellules cancéreuses vivent sous une pression constante. Elles se divisent rapidement, consomment beaucoup d’énergie et d’oxygène, et subissent souvent des conditions difficiles comme l’hypoxie ou l’exposition à la chimiothérapie. Pour y faire face, elles s’appuient sur des systèmes d’urgence qui les aident à replier et traiter correctement les protéines et à ajuster leur métabolisme. L’un de ces systèmes est connu sous le nom de « réponse au repliement des protéines » (unfolded protein response), déclenchée lorsque l’usine à protéines de la cellule, le réticulum endoplasmique, est surchargée. Un autre, la « réponse intégrée au stress », détecte différents types de stress et ralentit la production protéique. En temps normal, ces voies aident les cellules cancéreuses à survivre — mais si elles sont trop sollicitées trop longtemps, elles peuvent basculer d’un rôle protecteur vers le déclenchement de la mort cellulaire.
NXP800 frappe un capteur clé du stress
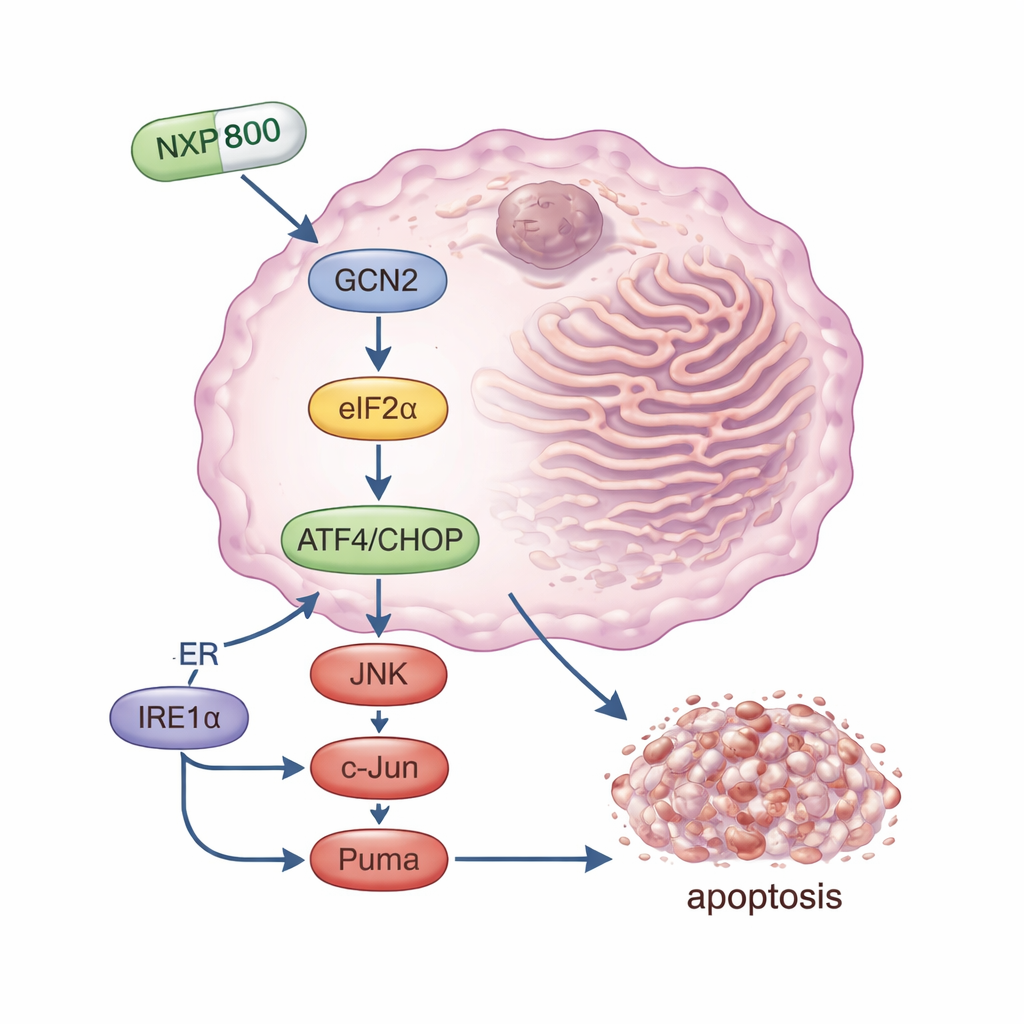
NXP800 est une petite molécule orale initialement développée pour bloquer une voie de chaleur (heat shock) impliquée dans la survie du cancer. Dans cette étude, les chercheurs ont découvert que, dans les cellules d’ostéosarcome, son effet principal est différent : elle active fortement une protéine détectrice de stress appelée GCN2. Une fois activé, GCN2 modifie un autre facteur, eIF2α, qui réduit rapidement la production protéique globale tout en augmentant les niveaux de commutateurs maîtres du stress spécifiques, en particulier la protéine ATF4 et son partenaire CHOP. Ensemble, ces molécules poussent la cellule vers la mort programmée. L’équipe a montré que lorsqu’ils bloquaient GCN2 — soit en silencant son gène soit avec un inhibiteur distinct — NXP800 ne pouvait plus déclencher efficacement cette cascade, et les cellules cancéreuses devenaient beaucoup moins sensibles au médicament. Cela identifie GCN2 comme une cible cruciale de NXP800 dans l’ostéosarcome.
Activation de plusieurs voies de mort à l’intérieur de la tumeur
Au-delà du bras GCN2 du réseau de stress, NXP800 a également activé une autre voie liée à la mort cellulaire. Il a activé un senseur nommé IRE1α, qui a à son tour stimulé les protéines de signalisation JNK et c-Jun. Cette branche favorise la production de Puma, une molécule pro-mort puissante qui endommage la machinerie de survie interne de la cellule. Dans des expériences en laboratoire, NXP800 a ralenti la croissance des cellules d’ostéosarcome, bloqué leur cycle cellulaire et activé des enzymes et modifications protéiques caractéristiques de l’apoptose, ou mort cellulaire contrôlée. Fait important, les cellules souches osseuses normales ont été beaucoup moins affectées, suggérant un certain degré de sélectivité pour les cellules tumorales déjà soumises à un stress limite.
Du banc d’essai aux modèles vivants
Pour vérifier si ces effets cellulaires se traduisaient par un contrôle tumoral réel, les chercheurs ont testé NXP800 chez des souris implantées avec des cellules humaines d’ostéosarcome près du tibia. Les souris ayant reçu NXP800 par voie orale ont développé des tumeurs qui ont crû significativement plus lentement et ont gardé à la fin de l’étude un volume d’environ moitié de celui des tumeurs chez les souris non traitées. Les échantillons tumoraux des animaux traités montraient des signes clairs du mécanisme du médicament : niveaux plus élevés des marqueurs de stress eIF2α et ATF4, moins de cellules en division active et davantage de cellules en apoptose. Des expériences séparées de sécurité chez des souris saines n’ont révélé aucun dommage majeur aux organes, et les tests hépatiques n’étaient pas aggravés, soutenant un profil de sécurité gérable aux doses utilisées.
Ce que cela pourrait signifier pour les patients
En somme, ce travail montre que NXP800 peut retarder la croissance de l’ostéosarcome en surexcitant délibérément les défenses de stress de la cellule cancéreuse jusqu’à ce qu’elles déclenchent l’autodestruction. En ciblant le capteur de stress GCN2 et des voies associées, le médicament offre une manière entièrement nouvelle d’affaiblir des tumeurs qui ont résisté à la chimiothérapie traditionnelle. Parce que NXP800 est déjà testé dans des essais cliniques précoces pour d’autres cancers, ces résultats suggèrent la possibilité de le repositionner pour l’ostéosarcome, seul ou en combinaison avec des traitements existants. Bien que des essais humains soient nécessaires pour confirmer le bénéfice et la sécurité, cette étude fournit une preuve de principe convaincante que retourner le stress cellulaire contre la tumeur pourrait ouvrir un nouveau chapitre thérapeutique pour les patients atteints de ce cancer osseux difficile.
Citation: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
Mots-clés: ostéosarcome, NXP800, réponse au stress, voie GCN2, apoptose