Clear Sky Science · fr
Cibler les vulnérabilités métaboliques : l’agoniste de REV-ERB SR9009 potentialise l’efficacité du sorafenib dans le cancer du foie
Pourquoi priver les cellules cancéreuses d’énergie compte
Le cancer du foie est l’un des cancers les plus meurtriers au monde, et de nombreux patients atteints de formes avancées reposent encore sur un médicament ancien appelé sorafenib. Si le sorafenib peut ralentir la croissance tumorale, les cellules cancéreuses s’adaptent souvent et deviennent résistantes, ce qui limite la survie des patients. Cette étude explore une nouvelle façon d’améliorer l’effet du sorafenib en attaquant la façon dont les cellules du cancer du foie se nourrissent, offrant un aperçu de traitements futurs qui pourraient frapper les tumeurs plus fort sans ajouter d’effets secondaires graves.
Les limites des traitements actuels du cancer du foie
Le sorafenib est depuis longtemps un traitement de référence pour les patients dont les tumeurs hépatiques ne peuvent pas être retirées chirurgicalement. Les nouvelles immunothérapies prolongent aujourd’hui la vie de certains patients, mais beaucoup ne peuvent pas en bénéficier ou n’y répondent pas. Pour ces patients, le sorafenib reste important, pourtant la résistance apparaît souvent en quelques mois. Les chercheurs ont posé une question simple mais puissante : quels changements au sein des cellules du cancer du foie leur permettent d’échapper aux effets du sorafenib, et ces changements peuvent-ils devenir de nouvelles faiblesses thérapeutiques ?
Les cellules cancéreuses augmentent leur centrale énergétique
Pour trouver des réponses, l’équipe a comparé des cellules de cancer du foie encore sensibles au sorafenib avec des cellules ayant appris à survivre au médicament. Grâce à un séquençage à grande échelle de l’ARN, elle a découvert que les cellules résistantes augmentaient fortement l’activité des gènes impliqués dans la phosphorylation oxydative mitochondriale — le principal mode de production d’énergie dans leurs « centrales » microscopiques, les mitochondries. D’autres gènes de protection contre le stress, notamment ceux liés à la gestion de la molécule appelée hème, étaient également augmentés. Ensemble, ces changements suggèrent que les cellules résistantes réorientent leur production d’énergie et leurs défenses contre le stress plutôt que d’ignorer simplement les cibles initiales du médicament.
Un second médicament qui coupe l’alimentation
Les chercheurs se sont ensuite tournés vers le SR9009, un composé expérimental initialement conçu pour cibler des protéines liées à l’horloge biologique appelées REV-ERB, qui participent au contrôle du métabolisme. Le SR9009 est connu pour perturber l’activité mitochondriale et être plus nocif pour les cellules tumorales que pour les cellules normales. Chez des cellules de cancer du foie de souris et d’humain, l’association du SR9009 au sorafenib a fortement réduit la survie cellulaire comparée à chaque médicament pris isolément. Les deux médicaments combinés ont presque annihilé la production d’énergie mitochondriale, forçant les cellules à dépendre de voies de substitution de glycolyse qui ne compensaient pas entièrement. Les tests en laboratoire ont montré de fortes baisses d’ATP cellulaire — la monnaie énergétique universelle — et moins de colonies de cellules cancéreuses survivantes. Fait important, les fibroblastes normaux et les cellules hépatiques non cancéreuses étaient beaucoup moins affectés, laissant entrevoir une sélectivité possible envers le tissu tumoral.
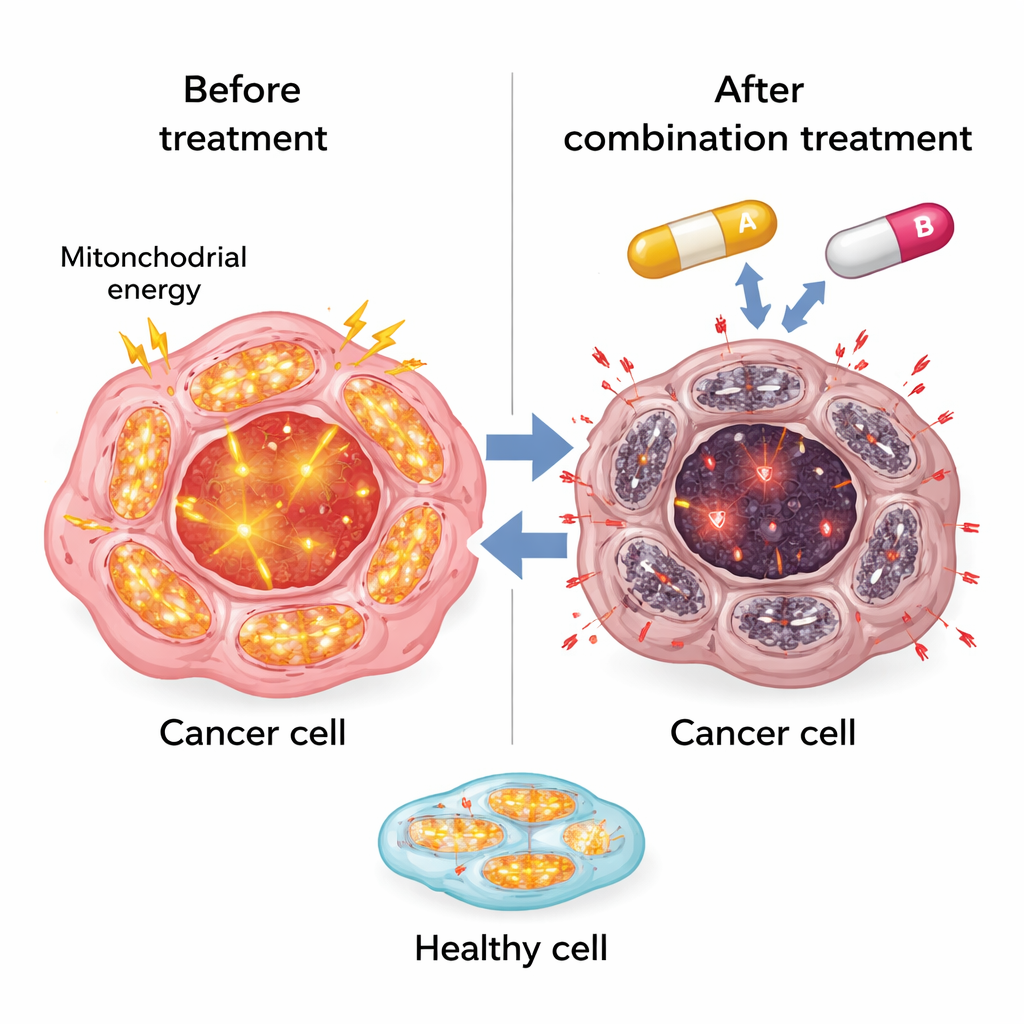
Déséquilibrer l’hème et déclencher un stress toxique
L’étude a aussi mis au jour une seconde vulnérabilité : la façon dont les cellules résistantes gèrent l’hème, une petite molécule contenant du fer essentielle pour de nombreuses enzymes, y compris celles des mitochondries. Les cellules résistantes du cancer du foie ont exprimé des niveaux élevés d’HO-1, une enzyme qui dégrade l’hème libre, et augmenté la ferritine, qui stocke l’ion fer libéré de manière sûre. Cela semblait les protéger des dommages liés à l’hème. Le SR9009 a perturbé cet équilibre. Dans les cellules résistantes, le SR9009 a augmenté les niveaux d’hème libre et les marqueurs de stress oxydatif tels que les espèces réactives de l’oxygène et les dommages lipidiques, surtout en combinaison avec le sorafenib. Parallèlement, les protéines mitochondriales diminuaient, renforçant l’idée qu’écraser les usines énergétiques et les défenses anti-stress de la cellule pousse les cellules cancéreuses au-delà d’un point de non-retour.
Un contrôle tumoral renforcé dans des modèles animaux
Pour vérifier si ces effets se traduisaient hors des boîtes de culture, l’équipe a testé l’association chez la souris. Chez des animaux portant à la fois des tumeurs hépatiques ordinaires et des tumeurs résistantes au sorafenib, seule la combinaison sorafenib plus SR9009 a réduit la taille des tumeurs résistantes. Dans un modèle distinct où des cancers du foie sont apparus spontanément après exposition à une substance cancérogène, l’ajout de SR9009 à une dose réduite de sorafenib a entraîné une régression tumorale dans plus de 90 % des nodules, tandis que les tumeurs des souris traitées avec le sorafenib seul continuaient majoritairement de croître. Fait remarquable, la combinaison n’a pas augmenté la toxicité globale : le poids corporel des souris est resté stable, les numérations sanguines sont demeurées normales et les marqueurs de lésion hépatique étaient plus faibles lorsque le SR9009 était inclus, suggérant un effet protecteur sur le foie sain.
Ce que cela pourrait signifier pour les patients
Pour un lecteur général, le message principal est que ce travail décrit une manière astucieuse d’améliorer un médicament existant contre le cancer du foie en exploitant la façon dont les tumeurs s’adaptent. Les cellules résistantes au sorafenib survivent en partie en renforçant leurs centrales énergétiques et leurs systèmes de contrôle du stress. Le SR9009 supprime ces soutiens, laissant les cellules cancéreuses affamées d’énergie et surchargées de sous-produits toxiques, tout en épargnant les cellules normales. Bien que le SR9009 ne soit pas encore un médicament approuvé et que ces résultats proviennent de modèles précliniques, l’étude trace une feuille de route : associer des médicaments standards à des agents ciblant le métabolisme propre aux tumeurs pourrait surmonter la résistance et permettre des doses plus faibles et plus sûres. À long terme, de telles stratégies combinées pourraient offrir davantage de temps et une meilleure qualité de vie aux patients atteints d’un cancer du foie avancé.
Citation: Sabbioni, S., Guerriero, P., Shankaraiah, R.C. et al. Targeting metabolic vulnerabilities: REV-ERB agonist SR9009 potentiates sorafenib efficacy in liver cancer. Cell Death Discov. 12, 86 (2026). https://doi.org/10.1038/s41420-026-02940-3
Mots-clés: cancer du foie, résistance aux médicaments, métabolisme du cancer, thérapie combinée, mitochondries