Clear Sky Science · fr
Les vésicules extracellulaires dérivées de CSM améliorent la prolifération et les métastases de l’ostéosarcome via la voie circRNA-0010220/β-caténine
Pourquoi cette histoire concernant le cancer osseux est importante
L’ostéosarcome est le cancer osseux le plus fréquent chez les enfants et les jeunes adultes, et il se propage souvent aux poumons. Même avec la chimiothérapie et la chirurgie modernes, de nombreux patients font face à des rechutes et à des métastases potentiellement mortelles. Cette étude explore les « conversations » discrètes entre les cellules cancéreuses osseuses et les cellules souches voisines de la moelle osseuse, révélant un petit messager moléculaire qui aide les tumeurs à croître et à se disséminer — et qui pourrait devenir une nouvelle cible thérapeutique.
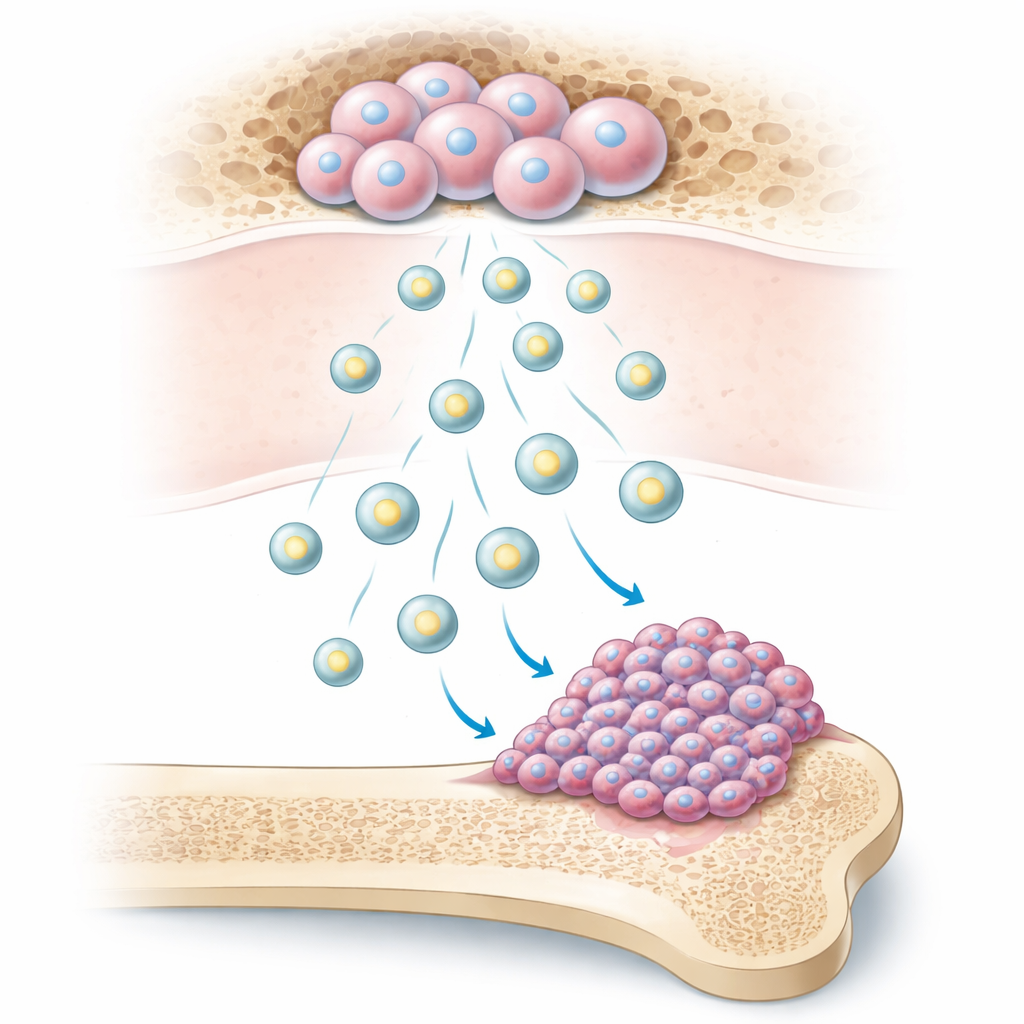
De minuscules colis à grande influence
Nos os contiennent des cellules souches mésenchymateuses de la moelle osseuse, des cellules polyvalentes qui contribuent à l’entretien et à la réparation osseuse. Ces cellules libèrent de minuscules bulles enveloppées de membrane appelées vésicules extracellulaires. Les chercheurs montrent que les cellules d’ostéosarcome absorbent facilement ces vésicules. Lorsqu’elles le font, les cellules cancéreuses se mettent à se diviser plus rapidement, à former davantage de colonies, à se déplacer plus vite à la surface et à envahir des barrières dans des tests en culture. Chez la souris, les tumeurs exposées à ces vésicules ont grossi et produit plus de métastases pulmonaires, indiquant que ces paquets microscopiques renforcent puissamment l’agressivité du cancer.
Un message circulaire qui renforce le cancer
L’équipe a ensuite examiné quels messages génétiques contenus dans les vésicules modifiaient le plus les cellules d’ostéosarcome. Ils se sont concentrés sur les ARN circulaires, une classe récemment découverte d’ARN formant des boucles fermées et remarquablement stables. Le séquençage a révélé un candidat marquant, appelé circRNA‑0010220, fortement augmenté dans les cellules d’ostéosarcome traitées par les vésicules de cellules souches et dans des échantillons tumoraux de patients. Lorsque les scientifiques ont réduit les niveaux de circRNA‑0010220 dans les cellules souches, leurs vésicules ont perdu une grande partie de leur capacité à stimuler la croissance, la migration et l’invasion des cellules cancéreuses — à la fois en culture et dans des modèles murins. Cela identifie circRNA‑0010220 comme un moteur clé des effets néfastes.
Un frein épigénétique désactivé
En approfondissant, les chercheurs ont cartographié la manière dont cet ARN circulaire reprogramme le comportement des cellules cancéreuses. À l’intérieur des cellules d’ostéosarcome, circRNA‑0010220 migre vers le noyau, le centre de contrôle cellulaire. Là, il se lie à une protéine appelée EZH2, une enzyme qui ajoute des marques chimiques aux histones — les protéines enroulées autour desquelles l’ADN est emballé. Agissant de concert, circRNA‑0010220 et EZH2 augmentent une marque spécifique connue sous le nom de H3K27me3 sur la région de contrôle de l’ADN d’un gène nommé CTNNBIP1. Cette modification compacte fortement la chromatine dans cette région, éteignant efficacement le gène. Parce que CTNNBIP1 agit normalement comme un frein sur une voie de signalisation très promotrice de croissance, sa mise hors jeu supprime une garde importante contre le comportement tumoral incontrôlé.
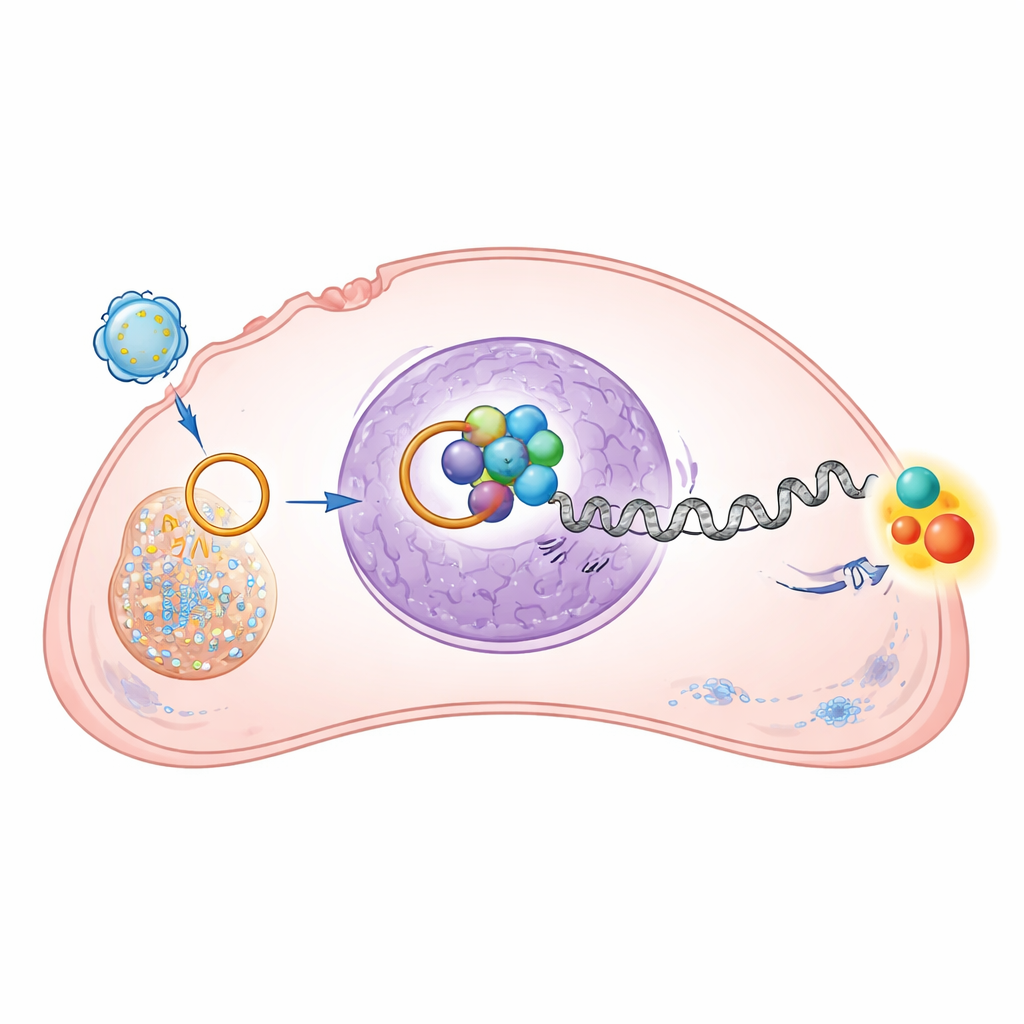
Mise en marche d’une puissante voie de croissance
CTNNBIP1 limite la voie Wnt/β‑caténine, un système de signalisation bien connu qui, lorsqu’il est hyperactif, encourage la division cellulaire, la migration et la survie. En réprimant CTNNBIP1, circRNA‑0010220 augmente indirectement les niveaux et l’activité nucléaire de la β‑caténine dans les cellules d’ostéosarcome. L’étude a montré que les gènes régulés par cette voie — liés à la progression du cycle cellulaire, aux traits de type souche et à l’invasion — devenaient plus actifs en présence du circRNA‑0010220 porté par les vésicules. Lorsque les chercheurs ont utilisé un médicament bloquant spécifiquement la β‑caténine, les effets pro‑croissance et pro‑migration de circRNA‑0010220 ont été en grande partie inversés. Cela confirme que l’ARN circulaire opère via cette voie de croissance pour propulser la progression tumorale.
Ce que cela signifie pour les traitements futurs
Pris ensemble, les travaux décrivent une chaîne d’événements complète : les cellules souches de la moelle osseuse envoient des vésicules chargées de circRNA‑0010220 aux cellules d’ostéosarcome ; l’ARN circulaire s’associe à EZH2 dans le noyau pour silencer chimiquement CTNNBIP1 ; cela relâche les freins sur la voie Wnt/β‑caténine, alimentant en fin de compte une croissance et une dissémination tumorales plus rapides. Pour les patients, cela suggère plusieurs nouvelles pistes thérapeutiques. Interrompre le transfert de vésicules, bloquer circRNA‑0010220, gêner son partenariat avec EZH2 ou atténuer la signalisation de la β‑caténine pourraient tous contribuer à ralentir la progression de l’ostéosarcome. Bien que ces idées restent à tester cliniquement, l’étude met au jour une conversation auparavant cachée dans l’environnement de la tumeur osseuse et met en évidence un ensemble concret de cibles moléculaires pour de futurs médicaments.
Citation: Pan, R., Pan, Y., Ruan, W. et al. BMSC-derived extracellular vesicles enhance osteosarcoma proliferation and metastasis via the circRNA-0010220/β-catenin pathway. Cell Death Dis 17, 376 (2026). https://doi.org/10.1038/s41419-026-08655-8
Mots-clés: ostéosarcome, vésicules extracellulaires, ARN circulaire, Wnt bêta-caténine, régulation épigénétique