Clear Sky Science · fr
La perte de DIAPH3 accélère la genèse de gliomes chez la souris
Pourquoi cette étude cérébrale est importante
Le glioblastome est l’un des cancers cérébraux les plus mortels et, malgré la chirurgie, la radiothérapie et la chimiothérapie, la plupart des patients survivent à peine un an de plus. Cette étude pose une question simple mais cruciale : quels changements précoces à l’intérieur des cellules cérébrales les poussent à devenir des tumeurs si agressives, et pourquoi ces tumeurs sont-elles si difficiles à détruire par la radiation ? En suivant une seule protéine structurelle dans les cellules cérébrales de souris, les chercheurs montrent comment sa perte déstabilise les chromosomes, accélère l’apparition des tumeurs et aide les cellules cancéreuses de type souche à résister à des radiations qui devraient les détruire.
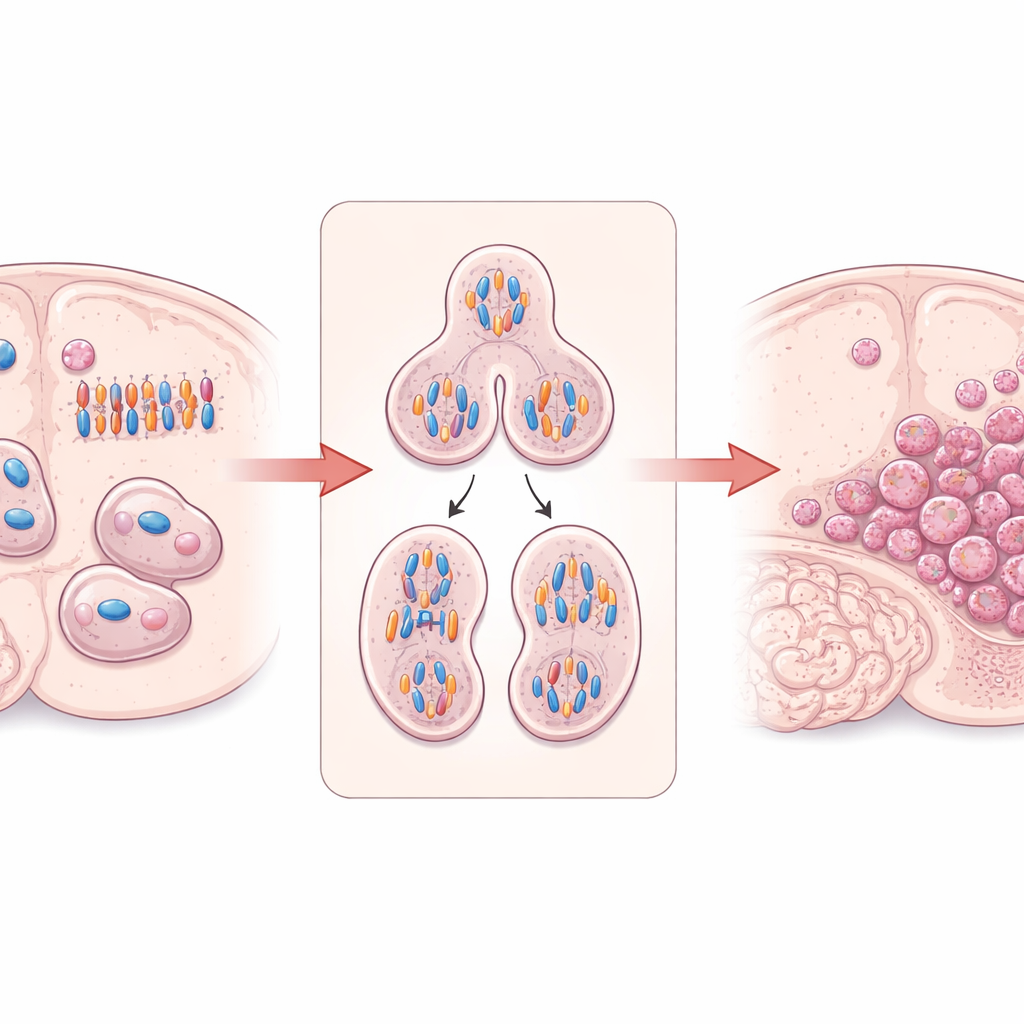
Un « constructeur » cellulaire qui maintient la division sous contrôle
Le travail se concentre sur DIAPH3, une protéine qui aide à construire et organiser l’armature interne de la cellule composée de filaments d’actine et de microtubules. Dans les cellules souches cérébrales en division, DIAPH3 est essentielle pour former un fuseau correct — la structure qui sépare les chromosomes dupliqués — et pour cliver une cellule en deux. Des travaux antérieurs avaient montré que lorsque DIAPH3 manque dans les cerveaux de souris en développement, les cellules en division manipulent souvent mal les chromosomes, conduisant à des nombres chromosomiques anormaux (aneuploïdie), à des arrêts du cycle cellulaire et à la mort cellulaire. Fait intrigant, une petite région du chromosome 13 humain contenant le gène DIAPH3 est fréquemment délétée dans le glioblastome, et des niveaux plus élevés de DIAPH3 ont été associés à une meilleure survie chez certains patients, suggérant que cette protéine pourrait agir comme suppresseur de tumeur dans le cerveau.
Générer des cerveaux de souris capables de former des tumeurs
Pour tester si la perte de DIAPH3 favorise réellement le cancer cérébral, l’équipe a créé des souris dans lesquelles deux gènes pouvaient être supprimés sélectivement dans les cellules souches formant le cortex : Diaph3 et Trp53, ce dernier codant pour le bien connu gardien du génome, p53. Les souris ne manquant que Diaph3 dans cette région n’ont pas développé de tumeurs, même après deux ans, ce qui implique que p53 peut encore éliminer les cellules fortement anormales. En revanche, les souris déficientes en Trp53 seules, ou en Trp53 et Diaph3 simultanément, ont finalement formé des gliomes diffus de haut grade ressemblant étroitement à la maladie humaine au microscope. Grâce à des IRM répétées à champ ultra‑élevé, les chercheurs ont montré que les animaux privés des deux gènes développaient des tumeurs détectables plus tôt et qu’à mi‑vie ils portaient plus souvent de grands gliomes, en particulier dans les bulbes olfactifs, que les souris ne manquant que Trp53. Le taux de croissance tumorale, une fois lancé, était similaire entre les groupes — ce qui changeait était le délai d’apparition des tumeurs.
Chaos chromosomique et réorganisation de l’activité génique
Pour comprendre pourquoi la perte de DIAPH3 accélère l’apparition des tumeurs, l’équipe a examiné l’activité génique dans les bulbes olfactifs de jeunes souris avant toute tumeur visible. Chez les animaux déficients à la fois en Diaph3 et Trp53, 126 gènes étaient exprimés à des niveaux différents par rapport aux mutants Trp53 seuls, et près de la moitié de ces gènes avaient déjà été liés au cancer. De nombreuses modifications se regroupaient dans des voies qui favorisent la croissance cellulaire, la migration et la formation de vaisseaux sanguins, notamment les voies VEGF, MAPK, RAS, Rap1 et la signalisation cAMP, ainsi que les réseaux couplés aux récepteurs G. Ce paysage moléculaire altéré suggérait que les cellules étaient poussées plus tôt vers un état de type cancéreux. L’analyse du nombre de copies sur l’ensemble du génome de tumeurs pleinement formées a révélé que la déficience en DIAPH3 n’augmentait pas fortement les petits changements d’ADN focaux, mais favorisait plutôt des gains et des pertes de chromosomes entiers — exactement l’aneuploïdie attendue d’une ségrégation chromosomique défaillante.
Dommages à l’ADN intrinsèques et cellules souches tumorales plus résistantes
Les cellules tumorales aneuploïdes présentaient davantage de dommages internes à l’ADN, détectés par des niveaux élevés du marqueur de casse d’ADN γ‑H2AX disséminé dans les noyaux. Pourtant, ces tumeurs continuaient à croître, ce qui implique qu’elles avaient acquis des moyens de tolérer ce stress. En comparant l’expression génique dans les tumeurs établies, les chercheurs ont trouvé des centaines de gènes modifiés par la perte de DIAPH3, y compris une amplification nette et une surproduction du récepteur du facteur de croissance FGFR2 dans de nombreuses tumeurs doublement mutées. On sait que FGFR2 stimule la machinerie de réparation de l’ADN dans les cellules de glioblastome, et son activation a été liée à la résistance à la radiation. L’équipe a isolé des cellules de type souche de gliome à partir de tumeurs de souris et a testé leur réponse à une dose cliniquement pertinente de radiation ionisante. Avant le traitement, la fréquence des cellules de type souche était similaire dans les deux génotypes, mais après irradiation, les cultures issues des tumeurs déficientes en DIAPH3 ont conservé environ deux fois plus de cellules souches actives que celles provenant des tumeurs Trp53 seules, démontrant une radio‑résistance accrue.
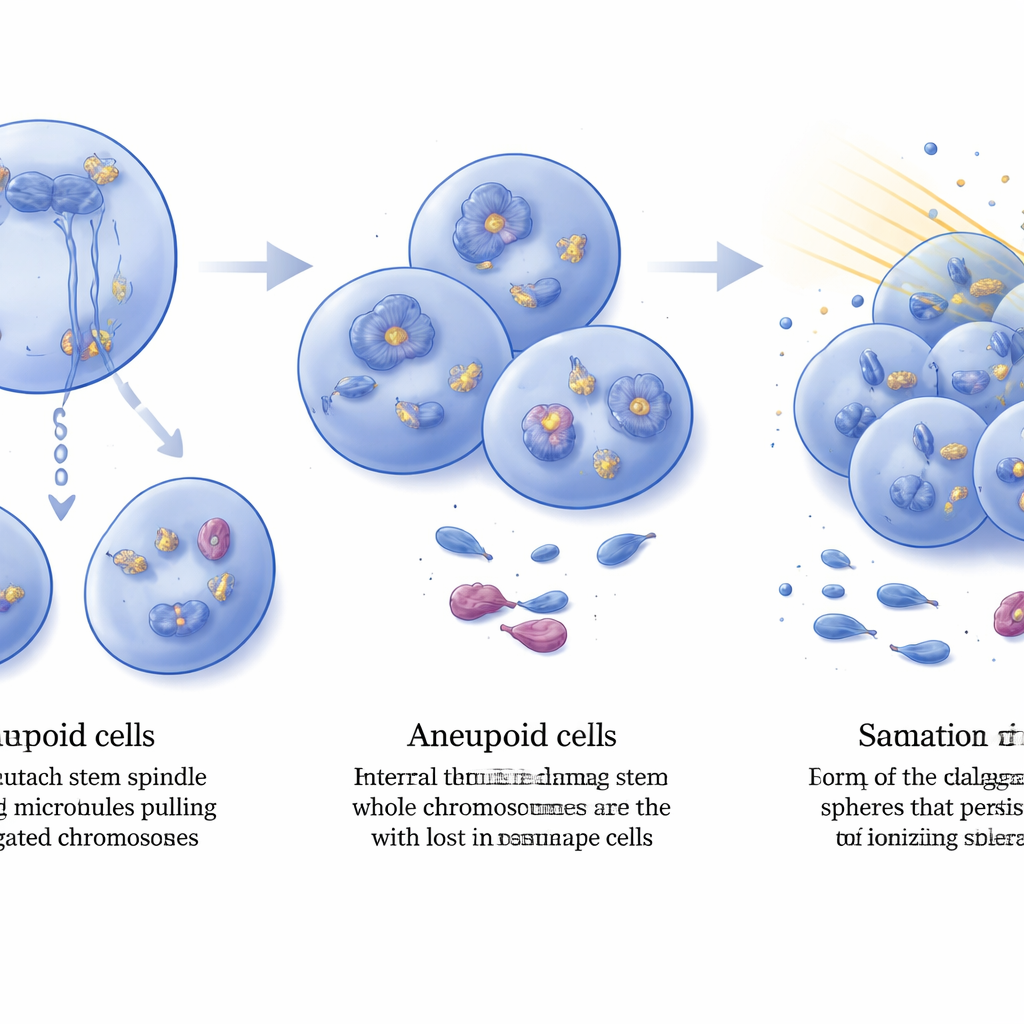
Ce que cela signifie pour le cancer cérébral
Pris ensemble, les résultats présentent DIAPH3 comme un gardien aidant les cellules souches cérébrales à se diviser avec le bon nombre de chromosomes. Lorsque DIAPH3 et p53 font tous deux défaut, la division cellulaire devient sujette aux erreurs, des chromosomes entiers sont perdus ou gagnés, et les dommages à l’ADN s’accumulent. Plutôt que de mourir, certaines cellules s’adaptent en amplifiant des facteurs liés à la réparation, tels que FGFR2, se transformant en gliomes aneuploïdes de haut grade dont les cellules de type souche sont exceptionnellement résistantes à la radiation. Bien que les modèles murins ne reproduisent pas toutes les caractéristiques du glioblastome humain, ces découvertes soutiennent DIAPH3 à la fois comme biomarqueur potentiel de pronostic et comme nœud dans le réseau de processus contrôlant l’initiation tumorale, la stabilité du génome et la réponse au traitement — ouvrant de nouvelles pistes thérapeutiques qui pourraient un jour rendre ce cancer cérébral dévastateur plus vulnérable aux traitements existants.
Citation: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Mots-clés: glioblastome, instabilité chromosomique, cellules souches tumorales cérébrales, résistance à la radiation, gènes suppresseurs de tumeur